recursos paraProfesionales
Últimas publicaciones comités científicos
CARAT: una herramienta validada para evaluar el control del asma y la rinitis alérgica en la práctica clínica
El Control of Allergic Rhinitis and Asthma Test (CARAT) es un cuestionario diseñado para evaluar el control simultáneo del asma y la rinitis alérgica (RA) en los pacientes, mediante una evaluación retrospectiva de cuatro semanas. Recientemente, un estudio ha realizado una revisión sistemática y un meta-análisis siguiendo las directrices de COSMIN, con el objetivo de evaluar sus propiedades psicométricas.
¿Por qué usar CARAT en la práctica clínica?
La evaluación del control del asma y la rinitis alérgica suele realizarse por separado, con herramientas como el Asthma Control Test (ACT) o el Allergic Rhinitis Control Test (ARCT). Sin embargo, dado que la mayoría de los pacientes con asma también padecen rinitis alérgica, surge la necesidad de una herramienta unificada. CARAT cubre esta brecha con 10 preguntas sobre síntomas de vías respiratorias superiores e inferiores, calidad del sueño, impacto en la actividad diaria y uso de medicación.
Propiedades psicométricas de CARAT
En esta revisión sistemática se incluyeron 16 estudios con los que se concluye que CARAT posee:
- Buena validez de contenido y una adecuada estructura factorial.
- Alta consistencia interna (α de Cronbach = 0.83).
- Alta fiabilidad (coeficiente de correlación intraclase = 0.91).
- Buena validez de constructo, con correlaciones significativas con otros PROMs (ej. ACT y ACQ-5).
- Buena capacidad de respuesta (cambio mínimo importante de 3.5 puntos).
Aplicación práctica
CARAT puede ser administrado en consulta mediante papel puesto que está validado al idioma castellano, pero también está disponible en formato digital a través de aplicaciones móviles como MASK-air y plataformas web, permitiendo un monitoreo continuo del paciente.
Conclusión
Esta revisión sistemática y meta-análisis refuerzan el uso de CARAT como una herramienta confiable para el control del asma y la rinitis alérgica en la práctica clínica habitual. Su implementación puede mejorar el seguimiento de los pacientes y facilitar decisiones terapéuticas más precisas
BIBLIOGRAFIA
Vieira RJ, Sousa-Pinto B, Cardoso-Fernandes A, et al. Control of Allergic Rhinitis and Asthma Test: A systematic review of measurement properties and COSMIN analysis. Clin Transl Allergy. 2022;12(9):e12194.
Diana Q, Abraham A, Yaicith A, Peter O, Juan T. Validation of the Spanish language version of the control of allergic rhinitis and asthma test. NPJ Prim Care Respir Med. 2022;32(1):47. Published 2022 Oct 29.
Sousa-Pinto B, Sá-Sousa A, Amaral R, et al. Assessment of the Control of Allergic Rhinitis and Asthma Test (CARAT) using MASK-air. J Allergy Clin Immunol Pract. 2022;10(1):343-345.e2.
CLASIFICACIÓN DE LA IT SEGÚN SU FORMULACIÓN LA IMPORTANCIA DE LOS EXTRACTOS
La Organización Mundial de la Salud (OMS) define la Inmunoterapia (IT) con alergenos como el único tratamiento que puede alterar el curso natural de la patología alérgica y prevenir el desarrollo del asma en pacientes con rinitis alérgica. Es el único tratamiento dirigido a la causa de la patología, a diferencia de los tratamientos de los síntomas, siendo fundamental que los extractos de las vacunas sean de alta calidad para que sean efectivas.1
Es importante cuando administremos dichos tratamientos tener una noción básica de los tipos de vacunas específicas de alergia. Con este documento tratamos de mostrar una clasificación breve de los tipos de IT especifica de alergia que en este momento se utilizan en su uso clínico en los servicios de alergología de nuestro país.
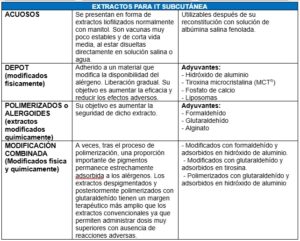
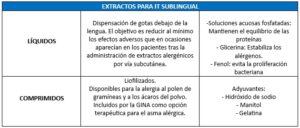
Los extractos para inmunoterapia subcutánea (ITSC) pueden ser acuosos, depot, polimerizados o modificación combinada. En la inmunoterapia sublingual (ITSL) la composición del extracto alergénico es la misma que en la ITSC, pero se modifica el excipiente. Los excipientes pueden ser líquidos o comprimidos liofilizados.
Se debe seguir las indicaciones realizadas por los laboratorios fabricantes en su forma de administración y las posibles modificaciones de la pauta que realice el clínico en atención a las características específicas de cada paciente.
Bibliografía:
- Abramson M, Puy R and Weiner J Inmunotherapy in Asthma; an update systematic review. Allergy 1999,54, 1022-1041.
Captador de la semana: Oviedo
Desde el Hospital Central de Asturias, la doctora Dolores Quiñones, alergóloga, realiza los contajes con el nuevo captador de la red de la SEAIC instalado en 2024.
Los datos de todas las estaciones aerobiológicas de la SEAIC pueden consultarse en la web www.pólenes.com
Reuniones Comité Aerobiología
A continuación se adjuntan las últimas dos reuniones del comité celebradas en Santiago de Compostela en octubre del 2023 y en Bilbao en noviembre 2024.
 Cargando...
Cargando...
 Cargando...
Cargando...
Reintroducción de la leche de vaca en bebés con alergia IgE mediada utilizando la Escalera de la Leche
¿Qué es la Escalera de la Leche?
La Escalera de la Leche es una intervención estructurada diseñada para ayudar a los bebés con alergia a la leche de vaca a reintroducirla gradualmente en su alimentación. Se inicia con alimentos que contienen pequeñas cantidades de leche bien cocida y avanza hasta productos con un mayor contenido de leche. Este enfoque progresivo busca progresar en la dieta. Desarrollada en el Reino Unido, ha sido ampliamente utilizada en alergia no IgE-mediada pero nuestro grupo ha estudiado su aplicabilidad, seguridad y eficacia en alergia a la leche IgE-mediada en lactantes recién diagnosticados de alergia a la leche.
Adaptación de la Escalera de la Leche para familias españolas:
La Escalera de la Leche original fue desarrollada por dietistas en el Reino Unido e incluye alimentos que comúnmente se consumen en ese país. Dado que los hábitos alimentarios varían según la cultura, nuestro primer objetivo fue desarrollar una versión de la Escalera de la Leche adaptada a la dieta tradicional española con recetas específicas. La versión española de la Escalera de la Leche consta de cuatro niveles, en los que se introducen alimentos con cantidades crecientes de leche de vaca y esta está progresivamente menos cocinada. El nivel inicial consiste en galletas, pan de leche y magdalenas y se progresivamente se introducen alimentos como tortitas, croquetas o bechamel. Por último, se introduce el yogurt y la leche.
Información relevante y resultados del estudio:
Este estudio se llevó a cabo de 3 hospitales de Madrid e incluyó bebés de menos de 1 año recién diagnosticados de APLV. Al cumplir los 12 meses, aquellos que seguían siendo alérgicos comenzaron la Escalera de la Leche. Los padres recibieron instrucciones y recetas para preparar los alimentos de cada nivel de la escalera. Se confirmó la tolerancia a cada nivel de la Escalera en el hospital mediante una provocación oral. Aquellos bebés que toleraban se les indicaba tomar a diario los alimentos de cada nivel y volver al cabo de 3 meses para continuar progresando en la Escalera. El 63.6% de los bebes no tuvo ninguna reacción y progresaron a lo largo de la escalera hasta conseguir reintroducir la leche y lácteos en la dieta. La mayoría de las reacciones ocurrieron en el hospital y aquellas que ocurrieron en casa fueron más leves y bien manejadas por los padres. La Escalera de la Leche fue una intervención segura para la mayoría de los pacientes, pero no está exenta de reacciones (algunas graves) por lo que requiere un control estricto por un Alergólogo.
La información completa está publicada en el artículo: Safety, Tolerability, and Feasibility of the Milk Ladder for Reintroduction of Cow’s Milk in Infants With IgE-Mediated Cow’s Milk Allergy. J Investig Allergol Clin Immunol. 2024 Dec 3;34(6):414-416.
Inmaculada Cerecedo
Allergy and Clinical Immunology Department, Cleveland Clinic Abu Dhabi, Emiratos Árabes Unidos
Sonsoles Infante
Unidad de Alergia Pediátrica, Servicio de Alergología, Hospital General Universitario Gregorio Marañón, Madrid
Belen de la Hoz
Servicio de Alergología, Hospital Universitario Ramon y Cajal, Madrid
Captador de la semana: Toledo
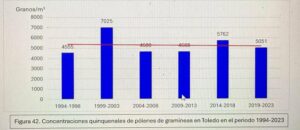
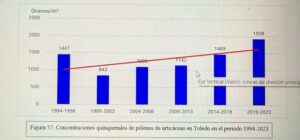
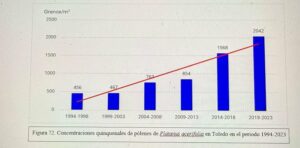
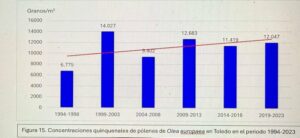
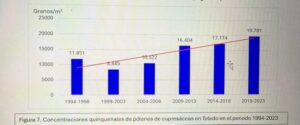
Hoy es el turno del Dr. Ángel Moral De Gregorio, expresidente del comité de Aerobiología Clínica de SEAIC, alergólogo en el Hospital Universitario de Toledo, desde donde nos proporciona los datos de pólenes.
Se instaló el primer captador en 1994, en 2016 se instaló el ciclón, han resistido todas las inclemencias incluido Filomena en 2021.
Con el Curso Avanzado de Palinología, el Dr. Ángel Moral ha impartido cursos de palinología a más de 200 alergólogos, muchos de los cuales han continuado la labor de aportar la lectura de pólenes en su zona para pólenes.com SEAIC.
Además, el Dr. Ángel Moral así como el Hospital de Toledo han contribuido ampliamente al estudio de los pólenes a lo largo de los años.


Dificultades diagnóstica en alergia a picadura de himenópteros
El diagnóstico de alergia a veneno de himenópteros consiste en identificar el veneno (o los venenos) responsable de causar reacción alérgica tras una picadura. Para este fin se cuentan con diversas técnicas diagnósticas como lo son las pruebas cutáneas, la determinación de IgE especifica, además de la información que proporciona el paciente sobre el insecto sospechoso.
Pero en ocasiones llegar a descubrir cual es el veneno responsable no es tan sencillo. Esto puede deberse a que: (1) el paciente no puede identificar el insecto que le ha picado, (2) las técnicas diagnósticas (pruebas cutáneas o la determinación de IgE especifica) son negativas, (3) presencia de resultados positivos a varios venenos y (4) discordancia entre el resultado de las pruebas cutáneas y los valores de IgE específica.
Para abordar estas dificultades es recomendable:
(1) Ampliar la historia clínica. Se debe de preguntar por la presencia de aguijón tras la picadura. Cuestionar si había alimentos cerca. Interrogar sobre el lugar donde sufrió la picadura (cerca de ríos, pantanos, lagos o piscinas). Recabar información sobre la presencia de colmenas próximas. Indagar sobre la visualización de nidos (terrestres o aéreos). Investigar sobre la profesión o “hobbies”. Es también muy importante conocer la región geográfica donde presentó la picadura.
(2) Optimizar las técnicas diagnósticas. Reducir el punto de cohorte de la IgE específica a 0,10 kU/L. Repetir las pruebas cutáneas o la determinación de IgE especifica pasados 1 a 2 meses. Ampliar el estudio a todos los venenos disponibles. Emplear otras técnicas diagnósticas más complejas.
(3) Diferenciar reactividad cruzada de doble sensibilización. Cuantificar alergenos especie específicos y alérgenos de reactividad cruzada. Establecer la ratio de antígeno 5 (en caso de resultados positivos para polistes y vespula). Identificar la presencia de CCD’s (en caso de resultados positivos para apis y vespula).
(4) Repetir estudio alergológico. Volver a realizar las pruebas cutáneas y determinación de IgE especifica. Valorar utilizar otro extracto diagnóstico al repetir las pruebas cutáneas. Aplicar plataformas multiplex.
Si tras haber completado todas las recomendaciones anteriores la identificación del veneno no es posible se puede intentar enviar suero del paciente a centros especializados que cuenten con la infraestructura y la experiencia para realizar técnicas diagnósticas más complejas (Test de activación de basófilos, Immunoblot o CAP-inhibición).
Lamentablemente enviar suero o derivar pacientes a otros centros no siempre es posible. A pesar de no poder establecer con una precisión del 100% el veneno (o los venenos) responsable de la reacción, el paciente subsidiario de beneficiarse de inmunoterapia específica para venenos debe recibirla. Si la reacción que presenta pone en riesgo su vida (anafilaxia) o implica un deterioro importante en su calidad de vida se le debe de administrar inmunoterapia específica contra todos los venenos identificados como probables responsables de la reacción.
Actualmente existen protocolos y guías clínicas que explican la forma en la que se debe de iniciar una doble inmunoterapia para veneno de himenópteros en aquellos pacientes que lo requieran. La administración de doble inmunoterapia es segura y confiere una buena protección en caso nuevas picaduras.
Federico de la Roca Pinzón
Médico Especialista en Alergología.
Miembro del comité de alergia a himenópteros.
TRATAMIENTO BIOLÓGICO EN LAS ENFERMEDADES ALÉRGICAS/ASMA GRAVE
Los medicamentos biológicos son producidos por organismos vivos o a partir de ellos (microorganismos humanos, animales o células de biotecnología) y se caracterizan por su alta especificidad y actividad terapéutica porque van dirigidos a la proteína o al receptor concreto que interviene en el proceso de la enfermedad.
Se consideran productos biológicos a las vacunas, alérgenos, antígenos, hormonas, inmunoglobulinas, citocinas, derivados de la sangre o plasma y anticuerpos monoclonales, entre otros.
Su auge se debe al gran avance de la biología molecular a través de técnicas de DNA recombinante, al conocimiento del genoma humano y de las vías de regulación de la respuesta inmune, que ha permitido identificar un variado número de dianas o puntos clave para este tipo de terapia.
El descubrimiento y producción de anticuerpos monoclonales (Ac Mo) por el Dr. Milstein en 1975 ha marcado la historia de la Medicina y Biotecnología. Inicialmente la indicación terapéutica se centró en áreas como reumatología y oncología, extendiéndose a diversas especialidades médicas como aparato digestivo, neurología, y también a la alergología.
La incorporación de anticuerpos monoclonales (Ac Mo) a la terapia alergológica ha significado un avance significativo en la medicina personalizada y de precisión, mejorando el manejo de las enfermedades alérgicas. Actúan bloqueando reguladores del sistema inmunitario claves en estas enfermedades.
Hasta el momento, en Alergología, los fármacos biológicos están indicados en:
- Asma Grave (Escalón 5-6 de la GEMA)
- Dermatitis Atópica
- Urticaria Crónica
- Esofagitis Eosinofílica, Síndrome Hipereosinofílico (SHE)
- Granulomatosis eosinofílica con poliangeítis (GEPA)
- Rinosinusitis Crónica con Poliposis Nasal (RSNCcPN)
- Angioedema Hereditario
Están en estudio algunos fármacos biológicos como tratamiento adyuvante en procesos de desensibilización con alimentos o medicamentos o inmunoterapia de alto riesgo, entre otros.
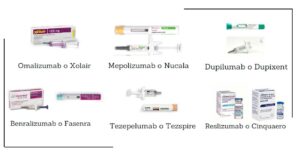 Imagen 1. Ejemplo de fármacos biológicos utilizados en alergología en la actualidad
Imagen 1. Ejemplo de fármacos biológicos utilizados en alergología en la actualidad
En general, el tratamiento biológico reduce los síntomas, disminuye el uso de glucocorticoides orales, así como los ingresos hospitalarios, lo que conlleva menos costes sanitarios. Además, mejora el control de la enfermedad y la calidad de vida del paciente.
La administración del fármaco se realiza en un centro sanitario (hospital o Centro de Salud) por enfermeras o bien se instruye y educa al paciente para que se pueda autoadministrar el fármaco en su domicilio, cuando la vía de administración es la subcutánea, ya que existen jeringas y plumas precargadas y preparadas para la inyección .
EFECTOS ADVERSOS MÁS HABITUALES
ADMINISTRACIÓN DOMICILIARIA
La enfermera, como educadora en autocuidados, es la encargada de evaluar si el perfil del paciente es adecuado para garantizar la seguridad de la administración, conservación, técnica adecuada y el cumplimiento del tratamiento en su domicilio.
Para ello, la enfermera, durante las primeras dosis administradas en el centro sanitario, educa y valora al paciente/cuidador en relación a los siguientes aspectos: Conservación, preparación, localización de la zona y la técnica correcta de inyección, efectos adversos y eliminación del residuo.
PRECAUCIONES A TENER EN CUENTA ANTES DE LA ADMINISTRACIÓN
- Mantener el medicamento fuera de la vista y del alcance de los niños.
- No utilizar el medicamento después de la fecha de caducidad que aparece en el etiquetado.
- Conservar en nevera (entre 2-8º). No congelar ni calentar.
- Conservar en el embalaje original (esto lo protege de la luz).
- El envase que contiene el dispositivo precargado puede conservarse a temperatura ambiente (25º), antes de usarlo, de horas a días en función del biológico que tenga prescrito el paciente.
- No utilizar ningún envase que esté dañado o muestre indicios de deterioro.
- Visualizar el aspecto del fármaco antes de utilizarlo (que muestre un aspecto claro sin turbideces).
- No agitar el dispositivo precargado.
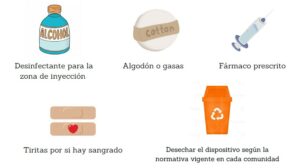
MATERIAL NECESARIO PARA LA AUTOADMINISTRACIÓN
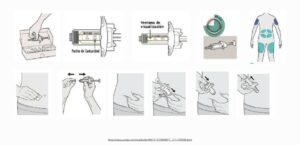
PASO A PASO AUTOADMINISTRACIÓN
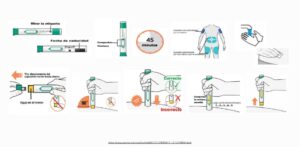
PLUMA PRECARGADA
JERINGA PRECARGADA
BIBLIOGRAFÍA
- Cuñetti L. Generalidades de los Medicamentos Biológicos [Internet]. Boletín farmacológico. 2014 [citado agosto 2024]. Disponible en: http://www.boletinfarmacologia.hc.edu.uy/index.php?option=com_content&task=view&id=104&Itemid=66
- Gema 5.4. Guía española para el manejo del asma. [Internet]. Madrid: Ed. Luzán 5; 2024. [citado agosto 2024]. Disponible en: http://.www.gemasma.com
- Iniciativa estratégica para el abordaje integral del asma: resumen ejecutivo. Disponible en : https://.seaic.org/profesionales/noticias-para-profesionales/libro-asma360.html (consultado julio 2024)
- Sabaté Brescó M, Salas Cassinello M, Sánchez Hernández MC, Sánchez Machín I, Sánchez Matas I, Sastre Domínguez J et al. El libro de las enfermedades alérgicas. [Internet]. Madrid: Fundación BBVA; 2021[citado agosto 2024]. Disponible en: https://www.fbbva.es/wp-content/uploads/2021/10/Libro-enfermedades-alergicas_FBBVA.pdf
- Delgado Romero J , Blanco-Aparicio M , Cisneros Serrano C , Díaz-Pérez D, Ferrando Piqueres R, López-Carrasco V, Merino-Bohórquez V , Soto-Retes L , Domínguez-Ortega J. Apoyo a la administración domiciliaria de terapia biológica en pacientes con asma grave: BioCart© [Internet].J Investig Allergol Clin Immunol 2022; Volumen 32(6): 482-484. Doi: 10.18176/jiaci.0786
- Ficha técnica autorizada de Xolair ® (omalizumab) (Consultado en septiembre 2024) Disponible en: https://cima.aemps.es/cima/dochtml/ft/05319008/FT_05319008.html
- Ficha técnica autorizada de Nucala® (mepolizumab) (Consultado en septiembre 2024)Disponible en: https://cima.aemps.es/cima/dochtml/ft/1151043001/FT_1151043001.html
- Ficha técnica autorizada de Fasenra ® (benralizumab) (Consultado en septiembre 2024)Disponible en : https://cima.aemps.es/cima/dochtml/p/1171252001/P_1171252001.html
- Ficha técnica autorizada de Dupixent® (dupilumab) (Consultado en septiembre 2024) Disponible en : https://cima.aemps.es/cima/dochtml/ft/1171229006/FT_117229006.html
- Ficha técnica autorizada de Tezspire® (tezepelumab) (Consultado en septiembre 2024) Disponible en: https://cima.aemps.es/cima/dochtml/ft/1221677001/FT_1221677001.html
Captador de la semana: Madrid – Clínica Subiza
Esta semana le toca el turno al Dr. Javier Subiza, primer Presidente del comité de Aerobiología Clínica, y Coordinador de la Red Nacional de Colectores de la Sociedad Española de Alergia (1993 – 2010). Creador de la primera página de la SEAIC de recuentos de pólenes. Actualmente desarrolla su actividad como alergólogo en la Clínica Subiza.


Historia de la estación de Aerobiología de Madrid (General Pardiñas 116).
En 1972, el Dr. Eliseo Subiza se desplazó a Londres al Hospital San Mary, el mismo en el que el Dr. Fleming descubrió la penicilina, para aprender la técnica que permitía hacer los recuentos de pólenes de una forma estandarizada, ese mismo año trae de allí el primer colector de pólenes volumétrico tipo Hirst que hubo en España.
En los siguientes años pudo publicar los primeros calendarios polínicos de Madrid y poco después del resto de España, gracias a que pudo instruir en esta técnica a muchos de sus colegas alergólogos(1,2).
El colector estuvo en la azotea de esta clínica desde 1973 hasta 1982, en que fue sustituido por otro colector tipo Hirst (Burkard 7 day recording volumetric spore trap). Del 2002 al 2012 fue expuesto en el museo de ciencias naturales de Valencia y desde entonces lo hemos recuperado de nuevo para exponerlo de forma permanente en nuestro centro (Clínica Subiza).
El Dr. Javier Subiza ha seguido los pasos de su padre, coordinando desde 1994 hasta el 2010, la red de colectores de la Sociedad Española de Alergología e Inmunología Clínica, creando en 1995 de forma pionera para visualizarse en Internet, la primera página oficial de recuentos de pólenes de la SEAIC (www.polenes.com). Otros logros, junto con su equipo, han sido descubrir por primera vez un método fiable que permite predecir en una gran parte de España los recuentos de pólenes de gramíneas con dos meses de antelación y que se sigue utilizando hasta la fecha (3).
Otros logros importantes han sido descubrir en la década de los 90, la capacidad alergénica de algunos pólenes de árboles, tales como los de Platanus hispanica y Cupresáceas, desconocidos hasta entonces, como causa importante de polinosis en España y que se han convertido en la actualidad, en una causa importante de polinosis de invierno e inicio de la primavera, en muchas de las áreas de nuestro país (4,5).
En 2021 dimos a conocer junto con nuestra colega la Dra Martha Cabrera la presencia de Phl p 1 clínicamente relevante, en periodos sin granos de pólenes atmosféricos, fuera de la estación de gramíneas (6).
Recientemente hemos podido dar a conocer como el cambio climático, ha producido en Madrid un incremento de 1,3° en los últimos 45 años. Ello parece haber contribuido a un adelanto de la estación y un incremento muy importante de los pólenes atmosféricos, especialmente los de invierno, lo que a su vez parece haber condicionado un aumento de la prevalencia de sensibilización, a Cupressus, Platanus y Quercus, este último coincidiendo con los hallazgos previamente encontrados por la Dra María Pedrosa (7,8).
Referencias
1) Subiza Martín E. Incidencia de granos de pólenes en la atmósfera de Madrid. Método volumétrico. Allergol et immunopatol. Supplementum VII, 1980.
2) Subiza E. Informe de 17 estaciones de España (método volumétrico). Incidencia de pólenes. En: XIV Congreso Nacional de la SEA. Madrid: Alergia e Inmunología Abelló, 1984; 41-43.
3) Subiza J, Masiello JM, Subiza JL, Jerez M, Hinojosa M, Subiza E. Prediction of annual variations in atmospheric concentrations of grass pollen. A method based on meteorological factors and grain crop estimates. Clin Exp Allergy. 1992 May;22(5):540-6.
4) Subiza J, Jerez M, Jiménez JA, Narganes MJ, Cabrera M, Varela S, Subiza E. Allergenic pollen pollinosis in Madrid. J Allergy Clin Immunol. 1995 Jul;96(1):15-23.
5) Varela S, Subiza J, Subiza JL, Rodríguez R, García B, Jerez M, Jiménez JA, Panzani R. Platanus pollen as an important cause of pollinosis. J Allergy Clin Immunol. 1997 Dec;100(6 Pt 1):748-54. 6) Cabrera M, Subiza J, Fernández-Caldas E, Garzón García B, Moreno-Grau S, Subiza JL. Influence of environmental drivers on allergy to pollen grains in a case study in Spain (Madrid): meteorological factors, pollutants, and airborne concentration of aeroallergens. Environ Sci Pollut Res Int. 2021 Oct;28(38):53614-53628.
7) Pedrosa M, Guerrero-Sanchez VM, Canales-Bueno N, Loli-Ausejo D, Castillejo MÁ, Quirce S, Jorrin-Novo JV, Rodriguez-Perez R. Quercus ilex pollen allergen, Que i 1, responsible for pollen food allergy syndrome caused by fruits in Spanish allergic patients. Clin Exp Allergy. 2020 Jul;50(7):815-823.
8) Subiza J, Cabrera M, Jm CR, Jc C, Mj N. Influence of climate change on airborne pollen concentrations in Madrid, 1979-2018. Clin Exp Allergy. 2022 Apr;52(4):574-577.
Captador de la semana: Almería
Desde el comité de Aerobiología Clínica vamos a ir presentando semanalmente todos los captadores que forman parte de la red de captadores de la SEAIC.
Esta semana le toca el turno al Dr. Juan José Zapata Yébenes, conocido alergólogo por ser el presidente del comité de Aerobiología, y que desarrolla su labor asistencial en Almería. El doctor Juan José Zapata siempre ha sido consciente de la importancia del estudio de la aerobiología en cada área de influencia para la comprensión, el diagnóstico y el tratamiento de la polinosis, y es el responsable de la estación aerobiológica de Almería, realizando los contajes en un área geográfica compleja con un alto índice de desertificación.


Acta reunión Noviembre 2024
Nuevos horizontes en la inflamación alérgica para explicar los fenotipos graves de alergia
En las últimas décadas, la prevalencia y la complejidad de las patologías alérgicas han aumentado significativamente. Este incremento se observa no solo en el número de pacientes, sino también en la aparición de casos con perfiles complejos, como los pacientes polisensibilizados, aquellos con remodelado epitelial y quienes muestran una respuesta insuficiente a los tratamientos convencionales. El manejo de estos pacientes representa un desafío para los especialistas en alergología (1).
Entre ellos, un grupo considerable presenta formas graves de alergia. La gravedad no se limita únicamente a aquellos que desarrollan reacciones anafilácticas, que representan un riesgo de vida evidente, sino también a aquellos que experimentan reacciones exacerbadas, como en el caso del asma alérgico grave, caracterizado por su difícil control y alta morbilidad (1). Nuestro grupo de investigación lleva más de una década estudiando los mecanismos subyacentes a estos fenotipos graves de alergia con un doble objetivo: 1) Identificar potenciales dianas terapéuticas para el manejo y control de estos pacientes y 2) la identificación y clasificación de estos pacientes.
Son pacientes que por sus características no responden a la mayoría de los tratamientos disponibles, que no suelen tolerar el tratamiento con AIT, tiene una baja calidad de vida y que, además, al tratarse de pacientes crónicos con muchos años de evolución suponen una importante carga económica para el Sistema Nacional de Salud.
Las características geográficas y climatológicas de nuestro país han permitido el estudio detallado de perfiles graves a lo largo de la geografía española. En Extremadura existe un porcentaje significativo de pacientes con alergia al polen de gramíneas que desarrollan reacciones graves a profilina (2); en Córdoba pacientes con alergia al polen de olivo sensibilizados a alergenos menores como Ole e 7 (3) o en las Islas Canarias, pacientes alérgicos a ácaros que además desarrollan reacciones graves (4) al entrar en contacto con harinas contaminadas con ácaros. Todos estos fenotipos alérgicos comparten características comunes: una respuesta inflamatoria persistente y exacerbada.
La inflamación persistente y no resuelta es un factor subyacente común observado en varias enfermedades humanas aparentemente no relacionadas, incluidas las enfermedades cardiovasculares y neurodegenerativas (5).
Algunos de los mecanismos asociados con la respuesta inflamatoria y que hemos demostrado en pacientes con alergia respiratoria grave son: Metabolismo de Warburg, aumento del metabolismo de los esfingolípidos y lisofosfolipidos, potenciación de las células T efectoras, desregulación de las células T reguladoras y cambios en las características biológicas de las plaquetas (4, 6, 7,8).
Estos hallazgos no solo abren nuevas vías de investigación en el campo de la alergia, facilitando una mejor comprensión de los procesos en estos pacientes, sino que también son relevantes para entender mecanismos subyacentes en otras patologías inflamatorias, como la artritis reumatoide o incluso la esclerosis múltiple, que comparten algunas de estas características inflamatorias. Es por este motivo que en España contamos con la Red de Enfermedades Inflamatorias (REI), financiada por el ISCII, que se dedica a la identificación y traslación de biomarcadores dirigidos a implantar estrategias de medicina personalizada en patologías inflamatorias, incluyendo las alérgicas. Su objetivo es proporcionar nuevas herramientas a los profesional para el tratamiento de estos pacientes y optimizar el uso de recursos de forma efectiva.
- Clin Exp Allergy. 2024 Aug;54(8):550-584. doi: 10.1111/cea.14517.
- J Allergy Clin Immunol. 2019 Feb;143(2):681-690.e1. doi: 10.1016/j.jaci.2018.03.013.
- 2019 Nov;74(11):2261-2265. doi: 10.1111/all.13860
- 2022 Jun;77(6):1772-1785. doi: 10.1111/all.15192
- Nat Rev Immunol . 2021 Nov;21(11):739-751. doi: 10.1038/s41577-021-00538-7
- 2018 Nov;73(11):2137-2149. doi: 10.1111/all.13563.
- 2023 May;78(5):1319-1332. doi: 10.1111/all.15621.
- Int J Mol Sci. 2024 Aug 30;25(17):9425. doi: 10.3390/ijms25179425
Grupos de trabajo del Comité de Asma SEAIC
Los grupos de trabajo del Comité de Asma de la SEAIC abordan áreas clave de la enfermedad con el objetivo de avanzar en el conocimiento, mejorar la atención clínica y promover la formación e investigación en asma desde un enfoque multidisciplinar y colaborativo:
- Grupo de relación con Atención Primaria – Coordinadores Ibon Eguiluz y Manuel Pajarón
- Grupo de Asma Grave – Coordinadores Julio Delgado y Javier Domínguez
- Grupo de Comunicación: redes sociales, web y medios de comunicación – Coordinadoras Lorena Soto y Paula Galván
- Grupo de relación con Pacientes y Enfermería – Coordinadora Virginia Bellido
- Grupo de Asma Infantil – Coordinadoras Remedios Cárdenas y Alicia Habernau
- Grupo de Procedimientos en Asma – Coordinadora Mª del Mar Fenández Nieto
- Grupo de Inmunoterapia en Asma – Coordinadora Lorena Soto
- Grupo de relación con el Comité de Rinoconjuntivitis (especial interés en RSCcPN) – Coordinador Ismael García
- Grupo de Investigación y relación con PII de SEPAR – Coordinadores Juan Carlos Miralles e Ismael García
- Grupo Comisión Acreditación UAG – Coordinadora Alícia Habernau
- Grupo de Tos Crónica – Coordinadores Manuel Rial y Paula Galván
TERAPIA INHALADA: INHALADORES DE POLVO SECO
La administración de fármacos por vía inhalatoria contribuye a la mejoría de las personas
con enfermedades en las vías aéreas. Con esta forma de administrar la medicación se
consigue un efecto rápido y eficaz, directamente en el sistema respiratorio.
Los inhaladores contienen en su interior la medicación y a través de una técnica adecuada
de administración se consigue que ésta llegue directamente hasta los pulmones.
Existen dos tipos de inhaladores: presurizados y de polvo seco.
Los inhaladores de polvo seco: a diferencia de los presurizados, no requieren una
sincronización de la inspiración con la liberación de la dosis, puesto que la propia
inspiración activa el depósito. En este tipo de dispositivos el principio activo se encuentra en
forma de polvo.
Como principales ventajas presentan:
– Mayor eficacia que los pMDI convencionales.
– Son de menor tamaño, para manejar con más facilidad y discreción.
– Más fácil la coordinación de pulsación e inhalación.
– No se utilizan gases propelentes contaminantes.
– Muestran las dosis restantes.
– La dosis que se libera en cada dosis es uniforme.
– Lo pueden utilizar pacientes larigectomizados y traqueostomizados.
Como limitaciones tienen las siguientes:
– Precisa una inspiración voluntaria y flujos más altos que los pMDI.
– Tiene mayor impacto orofaríngeo.
– Si no se usa correctamente, se puede perder la dosis preparada.
– Son más caros que los Pmdi.
– No se pueden utilizar en pacientes con ventilación mecánica.
Dentro de los inhaladores de polvo seco, podemos encontrar dos tipos:
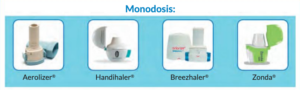
1. Inhaladores de polvo seco monodosis
En este tipo de inhaladores el fármaco se encuentra alojado en forma de polvo seco
en el interior de cápsulas que se guardan en blisters que se dispensan por separado
del dispositivo. Requieren de flujos inspiratorios más elevados que los sistemas
multidosis, por lo que la técnica de inspiración ha de ser más profunda, o si se
precisa se puede hacer dos maniobras de inspiración, para asegurar que se
administra la dosis correcta.
Existen 4 tipos de inhaladores unidosis.
- Aerolizer: De aspecto externo presenta una boquilla tipo chimenea y con un giro lateral se puede acceder a la base. En la base del inhalador dispone de dos pestañas que se han de pulsar simultáneamente para poder perforar la cápsula que conlleva la medicación y liberar la dosis.
- Handihaler: Presenta forma ovoide y consta de 3 piezas unidas por un sistema de bisagra y una tapa que hay que desplazar de forma lateral para colocar la cápsula. Una vez cargada la capsula, hay que volver a encajar la boquilla y pulsar para perforar la capsula y que se libere la medicación con la inhalación. Este inhalador además dispone de una ventana que nos permite comprobar que la cápsula esta bien colocada.
- Breezhaler: Se trata de un dispositivo semejante al aerolizer, con la diferencia de que se la boquilla se abre doblándose sobre el propio dispositivo. Dispone de un tapón protector. Para liberar la dosis hay que pulsar simultáneamente sobre las dos pestañas que tiene en la base.
- Zonda: Presenta un diseño de boquilla que permite que la inhalación sea más sencilla. Dispone de tapa que se abre de forma lateral y esta unida al dispositivo. Además lleva una cápsula transparente que permite comprobar si el paciente ha inhalado correctamente el fármaco
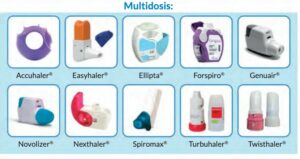
2. Inhaladores de polvo seco multidosis:
- Accuhaler: es un dispositivo con 60 dosis en un blíster enrollado dentro del propio inhalador en forma de disco. Se abre girando la carcasa, y deja al aire una palanca para cargar la dosis y la boquilla a través de la cual se inhala. Al pulsar la palanca, se desliza el obturador de la boquilla y queda al aire la dosis. Tras la inhalación, basta con girar la carcasa en sentido opuesto (no hay que mover la palanca).
- Ellipta: este dispositivo se carga automáticamente al abrirlo. Como ventaja cuenta de contador de dosis que va de 10 en 10.
- Easyhaler: Tiene una carga de 200 dosis, marcando en rojo las últimas 20 dosis. Este dispositivo consta de un depósito, un pulsador, un cilindro dosificador y una boquilla. Además consta de un sistema de seguridad por el cuál ni se puede cargar una dosis con ella cerrado, ni puede cargarse doble dosis. Es el único de este tipo de dispositivos con el que hay que hacer agitado previo.
- Forspiro: El fármaco está en un blíster. Se carga abriendo la boquilla y levantándola, y se carga bajando la boquilla. También tiene contador de dosis, y una ventana por la que se puede ver el blíster y así comprobar que se han realzado las inhalaciones diarias.
- Novolizer: Tiene un depósito de carga de 200 dosis. Se carga cuando presionas un botón de la parte superior. Tiene un indicador que se pone verde o rojo en función de si se ha inspirado correctamente el fármaco. Se puede recargar el cartucho sin tirar el dispositivo cuando se acaba. Tiene una triple comprobación cuando se hace, y es verlo, oírlo y el sabor tras realizarlo(debido a la presencia de lactosa).
- Genuair: el mecanismo es parecido al Novolizer pero con alguna modificación de seguridad como es el de evitar cargar doble dosis y se bloquea cuando está vacío para evitar hacer dosis sin fármaco.
- Nexthaler: Tiene contador de dosis. Se carga la dosis abriendo la tapa. Se trata de un dispositivo más compacto y con partículas extrafinas. Tiene un elemento auditivo, ya que se escucha un click cuando se hace correctamente. Si no se hace la dosis cargada, al cerrar el dispositivo, vuelve al reservorio.
- Spiromax: Tiene contador de dosis y capacidad para 200dosis. Al abrir la tapa, una bomba de aire transfiere el fármaco del depósito a la zona de dosificación. El dispositivo tiene lactosa (que se separa del fármaco por el flujo de inspiración del paciente y aporta sabor).
- Turbuhaler: Tiene contador de dosis y las últimas 20 se marcan en rojo. Se carga girando la rosca, y para ello debe hacerse en un ángulo mayor a 45º de la horizontal. Una vez cargado se puede accionar en cualquier posición al inspirar. La mayoría de sus presentaciones tiene como vehículo la lactosa.
- Twishthaler: Tiene contador de dosis y una forma similar al turbuhaler. Se carga al abrirlo pero debe hacerse en vertical. Se bloquea tras la última dosis.
CALIDAD DE VIDA EN LA ALERGIA A VENENOS DE HIMENÓPTEROS
La calidad de vida de los pacientes con enfermedades alérgicas se suele ver afectada ya que estas patologías generan tanto un impacto social y laboral como gastos directos e indirectos. Actualmente hay múltiples cuestionarios de calidad de vida validados para cada enfermedad en los que se constata el deterioro que causan en la vida de los enfermos que las padecen.
La alergia a venenos de himenópteros genera ansiedad y miedo por el riesgo a sufrir una reacción anafiláctica con un potencial riesgo de desenlace fatal. En Europa las anafilaxias por picaduras de himenópteros suponen el 48,2% de las anafilaxias sufridas en pacientes adultos y el 20,2% de las que padecen los niños. Existen cuestionarios específicos, como por ejemplo el HiCaVi, que valoran la calidad de vida en estos pacientes. El HiCaVi consta de 14 preguntas que valora la afectación de la calidad de vida en diferentes ámbitos en los pacientes mayores de 14 años. Por el momento, este cuestionario no se encuentra validado para pacientes pediátricos ni para apicultores.
Mención especial requieren los pacientes apicultores que sufren reacciones con las picaduras de himenópteros, en los que es considerada enfermedad profesional. En estas personas la calidad de vida se ve aún más mermada ya que influye de forma directa en el ámbito del trabajo y puede tener repercusiones laborales y económicas. Por este motivo, por lo que el HiCaVi no se encuentra validado para los apicultores.
Existen numerosos estudios en los que se valora la modificación de la calidad de vida en pacientes con alergia a himenópteros tras facilitarles autoinyectores de adrenalina y tras administrar inmunoterapia específica. En los pacientes a los que exclusivamente se les daba el autoinyector de adrenalina no se objetivó una mejoría en la calidad de vida a pesar de que la mortalidad por anafilaxia tras picadura desciende de forma importante. Los pacientes suelen percibir dicho tratamiento como molesto ya que hay que llevarlo consigo siempre. Esta percepción negativa favorece la falta de adherencia al mismo. En cambio, en los pacientes en los que se administró inmunoterapia específica, tras solo un año de vacunación el cuestionario de calidad de vida mostró ya una mejoría con respecto al inicial previo. De igual forma, se ha comprobado que en los pacientes en los que se sometieron al tratamiento de inmunoterapia, realizar una repicadura controlada mejoraba los resultados del cuestionario de calidad de vida ya que disminuye el estrés y la ansiedad debidas a la incertidumbre de sufrir una nueva picadura espontánea.
Por lo tanto, podemos ver cómo la alergia a venenos de himenópteros supone una disminución de la vida de los pacientes que la sufren y cómo esta puede mejorar sustancialmente con los tratamientos que existen actualmente para dicha enfermedad, en concreto la inmunoterapia específica.
María Dolores Rodríguez Bote.
Médico Especialista en Alergología. Miembro del comité de alergia a himenópteros.
Referencias:
1. Bemaniyan MH, Heidari M, Tavakol M, Nabavi M, Ramezani Kashal F, Gholami M, et al. A Quality-of-life Study in Patients with Anaphylaxis to Hymenoptera Venom in Iran. Iran J Allergy Asthma Immunol. 11 de febrero de 2024;23(1):59-68.
2. Alfaya T, Vega A, Domínguez-Noche C, Ruiz B, Marqués L, Sánchez-Morillas L. Longitudinal Validation of the Spanish Version of the Health-Related Quality of Life Questionnaire for Hymenoptera Venom Allergy (HRQLHA). J Investig Allergol Clin Immunol. 2015;25(6):426-30.
3. Oude Elberink JNG, van der Heide S, Guyatt GH, Dubois AEJ. Immunotherapy improves health-related quality of life of adult patients with dermal reactions following yellow jacket stings. Clin Exp Allergy J Br Soc Allergy Clin Immunol. junio de 2009;39(6):883-9.
Nuevos horizontes en la alergia a alimentos: el rol de los biológicos
La prevalencia de alergia a alimentos ha ido en aumento en las últimas décadas tanto en España como a nivel global, hasta hace unos años no existía otra recomendación más que la de evitar el alimento al que el paciente es alérgico, lo cual en ocasiones lleva a una dieta muy restrictiva y un empeoramiento en la calidad de vida. Por lo tanto, existe la necesidad de ofrecer nuevos tratamientos más allá de las dietas de evitación.
Una alternativa de tratamiento en auge es la inmunoterapia oral (ITO), la cual consiste en administrar dosis crecientes del alimento al que el paciente es alérgico para aumentar su tolerancia. Esta es generalmente efectiva, pero tiene varias limitaciones como la larga duración del tratamiento durante el cual se pueden presentar reacciones graves y otros efectos adversos, ser específica para cada alimento, no estar estandarizada y no estar disponible en todos los centros ni para todos los alimentos.
Otra alternativa emergente en la alergia a alimentos es el uso de fármacos biológicos. Un fármaco biológico es un medicamento producido a partir de organismos vivos o componentes de estos, como células, tejidos, proteínas o anticuerpos. Estos medicamentos están diseñados para actuar sobre procesos biológicos específicos. Ejemplos comunes incluyen vacunas, hormonas y moduladores inmunitarios. En el campo de la alergología se dirigen contra moléculas concretas de la respuesta inmune de tipo alérgico, es por este motivo que los fármacos biológicos han revolucionado el manejo de enfermedades alérgicas e inflamatorias como el asma, urticaria y la dermatitis atópica, especialmente en casos severos que no responden a terapias convencionales y se muestran prometedores en el tratamiento de alergia alimentaria.
Una aplicación destacada es el uso del biológico Omalizumab, que bloquea la IgE, utilizado desde hace años en asma y urticaria y recientemente aprobado por la FDA para reducir las reacciones alérgicas a alimentos en pacientes con múltiples alergias alimentarias (febrero de 2024), basado en estudios como el OUTMATCH. Aunque no está aprobado específicamente para su uso en combinación con la ITO, múltiples ensayos clínicos han explorado esta combinación con resultados alentadores. Incluso consensos de expertos recomiendan el uso de Omalizumab como adyuvante de la ITO. Esta combinación permitiría aumentar las dosis del alimento en ITO de manera más rápida y segura.
Otro biológico en investigación en alergia alimentaria es el Dupilumab que bloquea ciertas moléculas que participan en la señalización de la respuesta alérgica (IL4 e IL13) y que cuenta ya con eficacia demostrada en múltiples patologías alérgicas como dermatitis atópica, asma grave, poliposis nasosinusal y este mes de noviembre ha sido aprobado por la EMA como el primer y único tratamiento biológico para la esofagitis eosinofílica en pacientes de >1 año de edad. En alergia alimentaria su uso sólo o en combinación con ITO aún está en etapas iniciales de investigación, pero los resultados preliminares son prometedores.
Actualmente están en investigación varios fármacos biológicos dirigidos frente a diferentes moléculas involucradas en la respuesta alérgica y su posible uso en alergia alimentaria, sin embargo, se encuentran todavía en etapas preliminares.
El desarrollo de terapias biológicas ofrece esperanza para muchos pacientes que hasta hace poco no tenían opciones viables pero hace falta más investigación para optimizar su aplicación y establecer guías clínicas claras.
María Carabel Lahera. Clínica Universidad de Navarra (Madrid).
Rosialzira Vera Berrios. Hospital Clínico San Carlos, IdISSC (Madrid).
Bibliografía:
Mutarelli A, Giavina-Bianchi B, Arasi S, Cafarotti A, Fiocchi A. Biologicals in IgE-mediated food allergy. Curr Opin Allergy Clin Immunol. 2023 Jun 1;23(3):205-209. doi: 10.1097/ACI.0000000000000900. Epub 2023 Mar 28. PMID: 37185824.
Sindher SB, Hillier C, Anderson B, Long A, Chinthrajah RS. Treatment of food allergy: Oral immunotherapy, biologics, and beyond. Ann Allergy Asthma Immunol. 2023 Jul;131(1):29-36. doi: 10.1016/j.anai.2023.04.023. Epub 2023 Apr 25. PMID: 37100276; PMCID: PMC10330596.
Sindher SB, Fiocchi A, Zuberbier T, Arasi S, Wood RA, Chinthrajah RS. The Role of Biologics in the Treatment of Food Allergy. J Allergy Clin Immunol Pract. 2024 Mar;12(3):562-568. doi: 10.1016/j.jaip.2023.11.032. Epub 2023 Nov 25. PMID: 38013157; PMCID: PMC11104487.
Wood RA, Chinthrajah RS, Rudman Spergel AK, Babineau DC, Sicherer SH, Kim EH, Shreffler WG, Jones SM, Leung DYM, Vickery BP, Bird JA, Spergel JM, Kulis M, Iqbal A, Kaufman D, Umetsu DT, Ligueros-Saylan M, Uddin A, Fogel RB, Lussier S, Mudd K, Poyser J, MacPhee M, Veri M, Davidson W, Hamrah S, Long A, Togias A; OUtMATCH study team. Protocol design and synopsis: Omalizumab as Monotherapy and as Adjunct Therapy to Multiallergen OIT in Children and Adults with Food Allergy (OUtMATCH). J Allergy Clin Immunol Glob. 2022 Jul 21;1(4):225-232. doi: 10.1016/j.jacig.2022.05.006. PMID: 37779534; PMCID: PMC10509974.
Zuberbier T, Muraro A, Nurmatov U, Arasi S, Stevanovic K, Anagnostou A, Bonaguro R, Chinthrajah S, Lack G, Fiocchi A, Le TM, Turner P, Lozano MA, Angier E, Barni S, Bégin P, Ballmer-Weber B, Cardona V, Bindslev-Jensen C, Cianferoni A, de Jong N, de Silva D, Deschildre A, Galvin AD, Ebisawa M, Fleischer DM, Gerdts J, Giovannini M, Gradman J, Halken S, Arshad SH, Khaleva E, Lau S, Loh R, Mäkelä MJ, Marchisotto MJ, Morandini L, Mortz CG, Nilsson C, Nowak-Wegrzyn A, Podestà M, Poulsen LK, Roberts G, Rodríguez Del Río P, Sampson HA, Sánchez A, Schnadt S, Smith PK, Szajewska H, Mitrevska NT, Toniolo A, Venter C, Warner A, Wong GWK, Wood R, Worm M. GA2LEN ANACARE consensus statement: Potential of omalizumab in food allergy management. Clin Transl Allergy. 2024 Nov;14(11):e70002. doi: 10.1002/clt2.70002. PMID: 39506193; PMCID: PMC11540805.
PICADURAS Y MORDEDURAS DE ANIMALES INVERTEBRADOS TERRESTRES Y MARINOS
Algunos invertebrados frecuentes en nuestro medio pueden producir picaduras o mordeduras en el ser humano, como mecanismo defensivo. Principalmente la ejercen sobre la piel y pueden inyectar diferentes sustancias tóxicas propias de cada uno de ellos. Su identificación es muy importante para poder establecer el tratamiento adecuado y las medidas preventivas de cara a futuras picaduras.
Los animales que con más frecuencia producen este tipo de lesiones son los siguientes:
-Insectos: Himenópteros (avispas, abejas y abejorros), dípteros (moscas y mosquitos) y lepidópteros (orugas).
– Arácnidos: Arañas, escorpiones y garrapatas.
– Quilópodos (ciempiés): Escolopendra.
– Medusas.
– Algunos peces: Rayas.
Vamos a explicar algunas características de los que no son himenópteros.
DÍPTEROS
Las picaduras de mosquitos suelen extraer sangre e inoculan veneno de la saliva. La mayoría de las reacciones son locales y leves y se caracterizan por una pápula de aparición inmediata rodeada de enrojecimiento, que alcanza su máxima intensidad a los 20 minutos. Puede seguir una reacción tardía a las 24-36 horas que desaparece en unos 7-10 días. A veces, algunas de estas reacciones locales pueden ir asociadas a la aparición de vesículas o ampollas. Con mucha frecuencia las picaduras son múltiples. El tratamiento consiste en utilizar lociones contra el picor y antihistamínicos orales. En el caso de viajar a países tropicales es muy importante utilizar repelentes en la ropa. De forma muy excepcional puede haber reacciones generalizadas, que incluyen urticaria y muy raramente anafilaxia. En este último caso sería muy conveniente descartar otras enfermedades relacionadas con la alergia, como es la mastocitosis.
LEPIDÓPTEROS
Las picaduras de orugas suelen ser por contacto directo del insecto o por dispersión en el aire de algunos fragmentos procedentes de los árboles donde se encuentran, como es el caso de la procesionaria del pino (Thaumetopoea pityocampa). Suelen producir reacciones muy pruriginosas en las que luego aparecen lesiones papulosas y enrojecidas por el rascado.
ARAÑAS
El veneno de las mordeduras de arañas tiene componentes que pueden desintegrar a los glóbulos rojos, a determinadas proteínas o afectar al sistema nervioso. La mayoría de las especies distribuidas por España solo suelen causar dolor y molestias locales. Solo la denominada viuda negra (Latrodectus tredecimguttatus) puede producir una toxicidad generalizada del sistema nervioso, con espasmos en niños o ancianos.
ESCORPIONES
El escorpión más común de toda la península ibérica se llama Buthus occitanus. La picadura suele ser en el pie o en las manos al levantar piedras donde se cobijan. Suele haber un intenso dolor local, con un edema progresivo en la zona de la inoculación y alrededor de ella. Los síntomas suelen empezar de forma inmediata y alcanzan su máxima intensidad aproximadamente a las 5 horas. El tratamiento consiste en limpiar la picadura con antisépticos y tratar el dolor con analgésicos. En el caso de dolor muy importante, se debe infiltrar la picadura con anestésicos locales o utilizar opiáceos para controlarlo. Se puede considerar administrar profilaxis antitetánica.
GARRAPATAS
Son arácnidos que se alimentan de sangre. Las reacciones más habituales tras su picadura suelen consistir en dolor local, edema y picor en el punto de anclaje de la garrapata. Si no se extrae correctamente, pueden aparecer cuadros alérgicos de tipo anafiláctico o bien parálisis tóxica, por lo que es muy importante su manejo y retirada. También pueden ser transmisoras de infecciones. Además, la mordedura de garrapata puede generar de forma indirecta alergia a las carnes rojas, a las gelatinas o al medicamento Cetuximab, que se utiliza para tratar algunos tipos de cánceres. Esto se conoce como el síndrome de alergia a alfa-gal y se genera por la semejanza entre algunas proteínas (reactividad cruzada). El alfa-gal es una molécula de tipo oligosacárido que está en los mamíferos no primates y puede producirse una sensibilización a esta a través de la picadura de una garrapata. Con frecuencia, esta reacción incluye anafilaxias tardías tras haber comido carnes de mamíferos o gelatinas o después de haber recibido el Cetuximab.
ESCOLOPENDRAS
Las mordeduras suelen ser venenosas. Las escolopendras se encuentran por todo el mundo, principalmente en climas cálidos. Se les puede encontrar entre la corteza de los árboles o debajo de las piedras, e inyectan el veneno a través de dos colmillos en la zona bucal. Sus mordeduras son muy dolorosas, con dos punciones hemorrágicas, edema e inflamación local y, en ocasiones, con necrosis en el área afectada.
MEDUSAS
Estos invertebrados marinos tienen tentáculos largos donde se encuentran los nematocistos, que son una especie de cápsulas rellenas de veneno dotadas de un filamento en forma de arpón. En una sola picadura se descargan miles de éstos, lo que explica su gran efecto. La mayoría de las medusas solo causan síntomas locales, con dolor y/o ardor intenso en la zona de la picadura seguido de lesiones lineales con la impronta de los tentáculos. En casos más graves aparecen vesículas, equimosis y necrosis cutánea. Las manifestaciones generalizadas incluyen debilidad, náuseas, cefaleas, mialgias, alteraciones cardiacas o pulmonares. Los casos mortales son poco frecuentes. El tratamiento de las reacciones locales leves consiste en evitar la fricción en la zona, eliminar los restos de los tentáculos que puedan quedar adheridos, aclarar con agua salina y sumergir la zona afectada en agua caliente para aliviar el dolor.
RAYAS
Las rayas son un tipo de pez que poseen una cola en forma de látigo. Cuando una persona se adentra en aguas poco profundas y pisa una de ellas, el animal, como mecanismo de defensa, reacciona curvando su cola hacia arriba y hacia adelante, incrustando el aguijón y liberando el veneno. En general, la herida que produce la púa es irregular y sangra abundantemente. El dolor es inmediato e intenso y va disminuyendo gradualmente en un periodo de 6 horas a 2 días. La mayoría de las personas que sufren este tipo de herida manifiestan desvanecimiento, debilidad, náuseas y ansiedad por la intensidad del dolor. El tratamiento consiste en eliminar los residuos si los hay, aclarar con agua salina, inmersión en agua caliente para alivio del dolor, medicación analgésica si precisa y cura de la herida abierta.
Bibliografía: Comité de Alergia a Himenópteros de la SEAIC. Picaduras y mordeduras de invertebrados terrestres (insectos, arañas, garrapatas y ciempiés) y marinos (medusas y peces). En: Alergia a Himenópteros: Recomendaciones y algoritmos de práctica clínica de la Sociedad Española de Alergología e Inmunología Clínica. Actualización. Majadahonda (Madrid): ERGON; 2021. 41-50. ISBN: 978-84-18576-24-9
Jesús Macías Iglesias
Médico Especialista en Alergología
Miembro del Comité de Alergia a Himenópteros y Mastocitosis de la SEAIC
Consejos para un Halloween seguro para personas con alergias alimentarias
La tradición de celebrar Halloween cada 31 de octubre se está popularizando en España, con niños y adultos disfrutando de disfraces y recogiendo dulces. La noche de Halloween es una oportunidad para disfrutar, pero para las personas con alergias alimentarias, tanto niños como adultos, puede suponer un riesgo importante si no se toman precauciones. Las reacciones alérgicas van desde síntomas leves, como picor y vómitos, hasta la anafilaxia, una reacción grave que puede ser mortal Desde el Comité de Alergia Alimentaria de la Sociedad Española de Alergología e Inmunología Clínica (SEAIC), te ofrecemos algunas recomendaciones clave para que esta festividad sea segura y divertida.
1. Opta por actividades alternativas sin comida
En lugar de centrar la celebración en el típico "truco o trato", organiza actividades sin alimentos, como concursos de disfraces, manualidades o juegos. Repartir juguetes pequeños, lápices o calcomanías puede ser una opción divertida y segura para todos los niños.
2. Lee siempre las etiquetas de los productos
Asegúrate de leer con cuidado las etiquetas de los dulces y alimentos que se intercambien. Deshecha aquellos que no tengan una etiqueta clara o los que puedan contener alérgenos comunes como leche, frutos secos o huevo. Considera llevar tus propias golosinas seguras para intercambiarlas y evitar cualquier riesgo.
3. Lleva contigo medicación de rescate
No olvides llevar siempre contigo la medicación indicada por tu alergólogo, incluyendo la adrenalina autoinyectable si es necesaria.
En caso de que tu hijo sea alérgico, y disfrute del día con autonomía, aAsegúrate de que reconoce los síntomas, los comunique bien y si hay algún adulto que los acompañe rápidamente en caso de una reacción.
4. Evita la contaminación cruzada
Si organizas una fiesta, pregunta a los invitados sobre posibles alergias y ofrece opciones aptas para todos. Separa los alimentos seguros de aquellos que puedan contener alérgenos y
usa recipientes bien identificados.
5. Cuidado con los disfraces y el maquillaje
Muchos disfraces y maquillajes de Halloween pueden contener látex, al cual algunas personas alérgicas a alimentos también pueden ser sensibles. Opta por materiales alternativos y evita el uso de máscaras que puedan dificultar la identificación de una reacción alérgica o causar problemas respiratorios.
6. Educación y prevención en el colegio
Si tus hijos celebran Halloween en el colegio, asegúrate de que los profesores y monitores estén informados sobre las alergias alimentarias y sepan cómo actuar en caso de emergencia. Si se van a compartir dulces, es recomendable que lleves opciones seguras identificadas para evitar cualquier incidente.
7. En caso de emergencia, actúa rápido
Comprueba antes de salir que llevas toda la medicación de rescate que tu alergólogo/a te ha recomendado, especialmente la adrenalina autoinyectable.
Ante cualquier síntoma de reacción alérgica, como picor, hinchazón o dificultad para respirar, mantén la calma y sigue las indicaciones de tu especialista: pedir ayuda si estás solo, administrar la medicación, acudir al centro sanitario más próximo o llamar al 112. Si no sabes en ese momento cómo usar el autoinyector de adrenalina, llama al 112 explica la situación y te ayudarán.
Siguiendo estos consejos, puedes disfrutar de una noche de Halloween divertida y segura, evitando sustos relacionados con las alergias alimentarias.
¡Feliz Halloween!
Sofía Carreras Katcheff
¿En qué situaciones debo firmar un consentimiento informado(CI)?
Nosotros, como pacientes, tenemos derecho a ser informados y a preguntar acerca de los procedimientos a los que vamos a ser sometidos.
Según la Ley de Derechos del Usuario de Servicios de Salud (Ley 29414), se debe facilitar CI de manera obligatoria:
• Intervenciones quirúrgicas u otros procedimientos invasivos que conlleven un riesgo para la salud.
• Cuando se realice una exploración, tratamiento o fotografías del paciente con fines docentes.
• Cuando el paciente vaya a participar en estudios de investigación.1
• Si el paciente se negase a recibir o continuar con el tratamiento. EXCEPTO si es una emergencia (en este caso se aplica la doctrina de la presunción del consentimiento) o si pone en riesgo la salud pública. La renuncia al tratamiento se considera legalmente el desenlace natural del proceso de la enfermedad. Si la renuncia al tratamiento pone en riesgo a otras personas o en caso de menores de edad o adultos dependientes, los médicos suelen realizar consultas legales y judiciales, o consultas con personas expertas en cuestiones éticas.2
Cuando el paciente es menor de edad o no puede tomar una decisión de forma consciente será el padre, la madre o el tutor/representante legal quien firme el CI.3
Cada vez es más frecuente el uso de las PDA, Patient Decision Aids, para ayudar al paciente a tomar decisiones. Estas son gráficos, fotografías, vídeos, diagramas o programas interactivos que proporcionan al paciente información necesaria para la toma de decisiones e incluso asesoramiento personal.2
¿En qué situaciones no es necesario la firma de un CI?
• En procedimientos habituales, como pueden ser las extracciones y canalizaciones de vías venosas, el consentimiento está implícito, ya que el paciente acomoda su cuerpo para la realización de tal procedimiento (p. ej., estirar el brazo).
El personal sanitario debe asegurarse como mínimo, que los pacientes comprendan los siguientes puntos:
• Su estado actual y su evolución si rechazase el tratamiento.
• El pronóstico del tratamiento.
• La opinión del profesional médico y la mejor alternativa.
• Que puede formular todas las preguntas que le puedan surgir y éstas ser atendidas por el profesional adecuado.4
EN RESUMEN…
Lo normal es que el CI se pida de forma verbal, exceptuando ciertos casos que será necesario recabarlo por escrito como son:
1. Intervenciones quirúrgicas.
2. Procedimientos diagnósticos y terapéuticos invasivos, presentes en el documento RESCAL (Recomendaciones de Seguridad y Calidad en Alergología).
3. En procedimientos que supongan un riesgo potencial para el paciente o, en caso de mujeres embarazadas, para el feto.
4. Si el paciente va a participar en procedimientos de carácter experimental y proyectos docentes o de investigación.
Bibliografía.
- Consentimiento informado: ¿Qué es y en qué situaciones debe solicitarse? | Conexión ESAN [Internet]. www.esan.edu.pe. Available from: https://www.esan.edu.pe/conexion-esan/consentimiento-informado-que-es-y-en-que-situaciones-debe-solicitarse.
-
Stacey D, Lewis KB, Smith M, Carley M, Volk R, Douglas EE, et al. Decision aids for people facing health treatment or screening decisions. The Cochrane library [Internet]. 2024 Jan 29;2024(1). Available from: https://www.cochranelibrary.com/cdsr/doi/10.1002/14651858.CD001431.pub6/full
-
Pope TM. Consentimiento informado [Internet]. Manual MSD versión para público general. Manuales MSD; 2023 [cited 2024 Nov 3]. Available from: https://www.msdmanuals.com/es/hogar/fundamentos/asuntos-legales-y-%C3%A9ticos/consentimiento-informado?ruleredirectid=760
-
Guía de Consentimiento Informado [Internet]. Available from: https://www.saludcastillayleon.es/profesionales/es/bioetica/guias-bioetica-castilla-leon.ficheros/1266525-Guia%20de%20Consentimiento%20Informado.pdf
La dermatitis atópica no sólo afecta a la piel
La dermatitis atópica (DA) es un proceso inflamatorio de la piel caracterizado por un intenso prurito (picor) y piel seca, que presenta una evolución crónica y que cursa en forma de brotes. Es la enfermedad crónica de la piel más común en la infancia, aunque puede iniciarse a cualquier edad. Su desarrollo se debe a interacciones complejas entre la disfunción de la barrera cutánea, alteraciones de la microbiota de la piel e intestinal, desregulación del sistema inmunológico y susceptibilidad genética.
La DA se ha asociado a diferentes enfermedades (comorbilidades) tanto alérgicas como no alérgicas, aunque los mecanismos exactos de estas asociaciones no se conocen por completo. En algunos casos, estas asociaciones podrían ser coincidentes y no una consecuencia directa de la DA.
Recientemente, ha sido publicado un estudio coreano que ha analizado las enfermedades que se asocian a la DA, en más de 67.000 niños con esta enfermedad y que han sido evaluados desde el nacimiento hasta los 15 años de edad. A continuación, detallaremos las comorbilidades encontradas en este estudio 1.
Enfermedades alérgicas:
La DA se asocia con diferentes enfermedades alérgicas como la alergia alimentaria y el asma y rinitis alérgicas, dentro de lo que se conoce como “la marcha atópica”. Este término se refiere a este conjunto de enfermedades alérgicas que, por este orden, se suceden a medida que avanza la edad del paciente. Sin embargo, en algunos casos, esta secuencia no se cumple y las enfermedades alérgicas aparecen de manera independiente y en cualquier etapa de la vida. Posiblemente esto se deba al solapamiento que se produce entre la susceptibilidad genética y los factores ambientales que están involucrados en el desarrollo de las comorbilidades alérgicas.
Enfermedades no alérgicas extracutáneas:
Enfermedades psiquiátricas y neurológicas:
En cuanto a las comorbilidades no alérgicas, las más destacadas son las enfermedades psiquiátricas y neurológicas. Estos autores identifican una asociación entre la DA y la hiperactividad con déficit de atención (TDAH), desórdenes del sueño, alteraciones de la conducta o emocionales, así como con la convulsión febril y las cefaleas. Estas comorbilidades psiquiátricas pueden interrelacionarse, lo que podría jugar un papel importante en la asociación de estas enfermedades con la DA. Por lo tanto, es importante considerar los efectos de las comorbilidades de la DA en las enfermedades psicológicas, pero también el efecto de estas comorbilidades psicológicas en la DA.
Procesos infecciosos cutáneos y extracutáneos:
Los niños con DA presentan infecciones cutáneas más frecuentemente, como cabe esperar al tratarse de una piel alterada. Este estudio también reveló un incremento en las infecciones del tracto respiratorio y gastrointestinal, así como una mayor prevalencia de amigdalectomía. La desregulación inmunológica y la disfunción de la barrera, no sólo a nivel cutáneo sino también en otros órganos, podría contribuir al aumento en el riesgo a infecciones en órganos sistémicos, particularmente en una edad en la que las infecciones son muy comunes. Por otro lado, las infecciones fuera de la piel pueden exacerbar la DA y factores asociados al tratamiento de la DA podrían estar también relacionados con un incremento en el riesgo de infección.
Alteraciones gastrointestinales:
Se identificó una relación entre la DA y alteraciones gastrointestinales como el reflujo esofágico sin esofagitis, el estreñimiento o enfermedades hepáticas. Estas asociaciones podrían deberse a que comparten regulación inmunológica, en el eje intestino-piel a través de la microbiota intestinal, junto con la interrelación con otras comorbilidades de la DA.
Anemia por déficit de hierro:
También se encontró un incremento de la anemia de origen nutricional, posiblemente relacionado con dietas restrictivas injustificadas o a la malabsorción de nutrientes como resultado de la activación inmunológica. El estreñimiento es una comorbilidad de aparición más precoz que la anemia, lo que incrementaría la posibilidad de desarrollarla, dado que el enlentecimiento del tránsito intestinal puede ocasionar pérdida de apetito, dificultar la absorción de nutrientes y aumentar la excreción de hierro. Además, el estreñimiento interrumpe el equilibrio de la microbiota intestinal, afectando al metabolismo nutricional, pudiendo ocasionar también esta pérdida de hierro.
Enfermedades no alérgicas cutáneas:
Además de las comorbilidades fuera de la piel, la DA aumenta el riesgo de enfermedades cutáneas. Las enfermedades autoinmunes, incluyendo el vitíligo, la dermatitis herpetiforme y la psoriasis, comparten fisiopatología en aspectos como la disfunción de la barrera cutánea, la desregulación inmunológica, factores propios del paciente y factores ambientales.
Otros estudios han encontrado asociación entre la DA y la urticaria crónica, que podría explicarse por la desregulación inmunológica, factores genéticos compartidos y el estrés oxidativo.
Riesgo y cronología
El estudio concluye que tanto la edad de aparición como la gravedad de la DA influyen en el número de comorbilidades asociadas. La presencia de comorbilidades fue más frecuente en los niños con un inicio más precoz de la DA, en los varones y en aquellos con dermatitis más grave (medida por un mayor número de ingresos hospitalarios y mayores tasas de prescripción de corticoides tópicos).
La presencia de rinitis y asma alérgicas, principalmente las de inicio en preescolar, se asociaba, en este estudio, a la presencia de varias comorbilidades en el niño mayor y, el asma en concreto, tenía un efecto significativo en las alteraciones psiquiátricas y neurológicas. Sin embargo, la aparición de enfermedades autoinmunes no estaba influida por estas comorbilidades.
En resumen, los niños con DA pueden presentar varias comorbilidades. Reconocerlas a tiempo puede ayudar a mejorar los síntomas y reducir las complicaciones y el impacto tanto de las comorbilidades como de la propia DA.
Dra. Eva María Lasa Luaces. Unidad de Alergología Infantil del Hospital Universitario Donostia. Comité de Alergia Infantil SEAIC.
- Kim JH, Lee E, Ha EK, Shin J, Lee GC, Rha YH, Han MY. Cascade of atopic dermatitis comorbidities in children after birth for 15 years. 2024 Jan;79(1):153-163. doi: 10.1111/all.15917. Epub 2023 Oct 16. PMID: 37843069.