resultados de la búsqueda: profesionales/aviso-importante/wp-content/uploads/logos/Sitio web no disponible/inicio/cme-jiaci
Acta Reunión Comité Alergia Cutánea. San Sebastián 2016
![]() Contenido disponible sólo para socios.
Contenido disponible sólo para socios.
Congreso Zaragoza 2021
Estimados socios:
Nos ponemos en contacto con todos ustedes para informarles que después del éxito obtenido en la pasada edición del 33º Congreso de la Sociedad Española de Alergología e Inmunología Clínica en Zaragoza y tras recibir varias solicitudes de participantes que no pudieron asistir por los problemas derivados del Covid, se abre la posibilidad de poder conectarse ONLINE a las Sesiones que hubo.
Todos aquellos que tuvieran la inscripción confirmada, podrán acceder al enlace https://www.e-congress.events/seaic2021.
Este enlace ONLINE estará operativo durante los próximos 4 meses y podrán acceder todas las veces que lo necesiten.
Deberán acceder con la dirección de correo electrónico a donde se les confirmó la inscripción, así como la contraseña.
Si no recuerdan la contraseña se podrá generar una nueva contraseña entrando en la web del congreso https://www.congresoseaic.org/SEAIC2021. Deberán hacer clic arriba a la derecha en «¿Ha olvidado su contraseña?» y podrán crear una nueva siguiendo las instrucciones. Una vez realizado el cambio, con su dirección de correo electrónico y la nueva contraseña podrán acceder al formato online.
Asimismo, aquellos que no tuvieran Inscripción hecha están a tiempo de Inscribirse en el formato online en la página web del congreso. El precio por inscripción ONLINE para socios de la SEAIC es de 120 euros.
No duden en ponerse en contacto al correo seaic.inscripciones@viajeseci.es para más información.
Asthma Night Live
El próximo 19 de mayo de 2022 tendrá lugar el evento web «Asthma Night Live», con la intervención de los doctores García-Cosío, Canónica y Bobolea. Este seminario web cuenta con la colaboración de Sanofi y el aval de la SEAIC.
XIII Reunión CYNA
Hoy se ha abierto la web de la XIII Reunión CYNA, que se celebrará en Madrid los días 27 y 28 de enero de 2017. A través de esta web, los socios que lo deseen, podrán solicitar su inscripción en el evento.
¿Cómo saber si soy alérgico a las picaduras de abejas y avispas?
La alergia al veneno de himenópteros (abejas, avispas, etc.) no es una enfermedad genética o de nacimiento, sino que se puede desarrollar a lo largo de la vida tras haber sufrido picaduras de estos insectos y haberse sensibilizado a ellos. El estudio alergológico está indicado en pacientes que, o bien han sufrido una reacción generalizada con alguna de estas picadura, o que presentan reacciones locales extensas y tienen una alta exposición o mala calidad de vida, con el objetivo de demostrar la presencia de sensibilización específica mediada por IgE frente al veneno del insecto responsable y valorar si son candidatos a recibir una inmunoterapia con alérgenos (vacuna). Por lo tanto, no está indicado el estudio predictivo ni preventivo en pacientes con miedo a las reacciones o con antecedentes familiares de esta alergia.
Para realizar un diagnóstico correcto, se disponen de una serie de procedimientos que explicamos a continuación:
Historia clínica
Es la herramienta fundamental. Los síntomas presentados con la picadura permiten conocer el tipo de reacción sufrida. Es decir, si se trató de una reacción local normal, local extensa, sistémica o incluso si pueden existir otras enfermedades asociadas como los síndromes de activación mastocitaria. Debe recogerse el número y la zona de las picaduras recibidas, el intervalo de tiempo entre la picadura y el inicio de los síntomas y el tratamiento que se administró en ese momento. Otro aspecto muy importante es la identificación del insecto picador. En algunas ocasiones puede parecer más evidente, aunque en otras es posible que sea ambiguo o realmente difícil. El entorno en el que se produce la picadura puede ayudar a ello, sobre todo con respecto al lugar donde sucedió, época del año, comportamiento del insecto, alimentos cercanos, persistencia del aguijón tras la picadura o presencia cercana de nidos o de colmenas. Es posible que esta información pueda sugerir el género del himenóptero, si se trataba de una avispa (Vespula, Dolichovespula, Vespa, Polistes), una abeja (Apis) o un abejorro (Bombus), entre los más habituales. Incluso, en el caso de que se pudiera haber recogido el insecto que picó, se podría aportar el ejemplar en la consulta.
El cuestionario de calidad de vida (HiCaVi), validado por nuestro comité de la SEAIC, permite evaluar este aspecto en este grupo de pacientes y apoyar la indicación de tratamiento con inmunoterapia en algunos casos.
Pruebas cutáneas
Se realizan de dos tipos: Intraepidérmicas o skin prick test, que son similares a las que se hacen en el estudio de pólenes y de otros alérgenos respiratorios ; e intradérmicas, a concentraciones crecientes seriadas. Su positividad es suficiente para demostrar sensibilización.
Pruebas de laboratorio
Mediante una analítica de sangre se pueden medir las IgE específicas frente a venenos completos, que son los anticuerpos que una persona puede generar después de recibir picaduras. Se consideran positivas a partir de 0,1 kUA/L.
El conocido como diagnóstico molecular permite detectar anticuerpos frente a alérgenos concretos para conocer la clase de proteínas que han podido causar la alergia. Es útil en el caso de que varios venenos sean positivos, con el fin de poder diferenciar entre si estamos sensibilizados de forma primaria a uno solo, a varios a la vez (cosensibilización) o si es por el fenómeno de reactividad cruzada (que es la positividad de varios pero por la composición parecida entre ellos).
El uso de otras técnicas de laboratorio más complejas como el CAP-Inhibición o el test de activación de basófilos (TAB) permiten aumentar la precisión y poder llegar a un diagnóstico definitivo.
Además, en todo paciente que haya sufrido una anafilaxia debe solicitarse una triptasa basal, que es una proteasa que puede estar elevada en algunas patologías del sistema inmunitario.
La prueba de exposición mediante repicadura controlada con el propio insecto no está indicada como método diagnóstico por motivos éticos, pero sí es un procedimiento utilizado en pacientes que ya están recibiendo una vacuna y que tiene como objetivo comprobar la eficacia de este tratamiento.
En el caso de pacientes con una historia de una reacción sistémica y un estudio temprano negativo, hay que repetir las pruebas aproximadamente 1-2 meses después, ya que existe un periodo de tiempo en el que pueden darse falsos negativos. Sin embargo, en un 15% de los pacientes con una historia sugerente de alergia no se llega a detectar IgE específica frente a venenos. Igualmente, es importante señalar que los resultados de estas pruebas no se correlacionan con la gravedad de la picadura ni con el riesgo de tener una nueva reacción generalizada posterior.
Finalmente y teniendo en cuenta lo anterior, queda de manifiesto la relevancia de ser valorado por un médico alergólogo, quien brindará a sus pacientes el diagnóstico más preciso y los mejores cuidados.
Jesús Macías Iglesias
Médico Especialista en Alergología
Miembro del Comité de Alergia a Himenópteros y Mastocitosis de la SEAIC
Bibliografía: Comité de Alergia a Himenópteros de la SEAIC. Algoritmo básico: Alergia al veneno de los himenópteros. En: Alergia a Himenópteros: Recomendaciones y algoritmos de práctica clínica de la Sociedad Española de Alergología e Inmunología Clínica. Actualización. Majadahonda (Madrid): ERGON; 2021. 11-21. ISBN: 978-84-18576-24-9
La alergia a veneno de himenópteros, ¿se cura?
Se estima que entre el 56-94 % de la población general padecerá una picadura de himenóptero (abejas y avispas). Según algunos estudios epidemiológicos, en Europa entre el 0,3 y el 7,5 % de la población adulta, y el 3,4 % de los niños, puede padecer una reacción alérgica generalizada tras la picadura de un avispa o abeja, y entre el 2,4-26,4% podrían presentar reacciones alérgicas locales. La población rural presenta un riesgo superior por el hecho de estar más expuesta a las picaduras de estos insectos.
El tratamiento principal para las personas alérgicas es la inmunoterapia (IT) con veneno de himenóptero, también conocida como “vacuna para la alergia”. La IT consiste en administrar de forma subcutánea pequeñas cantidades del alérgeno de forma gradual (fase de inicio y de mantenimiento) para que el sistema inmunológico se “acostumbre” y reduzca su reacción.
La eficacia de la inmunoterapia específica, o vacunación con extractos de veneno de himenópteros, está ampliamente demostrada. La IT a veneno de himenópteros es muy efectiva para reducir los síntomas alérgicos y mejorar la calidad de vida de las personas sensibilizadas alérgicas a estos insectos. Actualmente es el único tratamiento capaz de prevenir futuras reacciones sistémicas, y está indicada en niños y adultos que hayan padecido alguna reacción generalizada moderada o grave, con síntomas cutáneos y respiratorios o cardiovasculares, y siempre que se demuestre un mecanismo dependiente de la Inmunoglobulina E (IgE). La IT también se puede considerar en adultos con solo síntomas cutáneos, pero con alto riesgo de exposición y/o empeoramiento de su calidad de vida. La duración convencional del tratamiento es de 3 a 5 años. La eficacia de la inmunoterapia varía de persona a persona, pero en general se ha demostrado que es altamente efectiva hasta en un 97% de los casos, consiguiendo la reducción de los síntomas y prevención de reacciones graves. El efecto terapéutico es duradero, de modo que incluso 10 años después de la finalización de la IT alrededor del 90 % de los pacientes sigue estando protegido.
Es importante tener en cuenta que la IT es un tratamiento a largo plazo que requiere un compromiso y seguimiento adecuados. Debe ser administrada bajo la supervisión de alergólogos en una unidad de inmunoterapia y se realiza en etapas, comenzando con dosis bajas e incrementándolas gradualmente hasta llegar al mantenimiento (dosis fija mensual o cada dos meses). Además, es fundamental seguir tomando precauciones para evitar picaduras, como usar ropa protectora y evitar áreas donde suelen encontrarse estos insectos. Sin embargo lo más importante es portar un kit de emergencia con adrenalina auto inyectable hasta que se alcance el mantenimiento con la vacuna.
Javier Pereira
Médico Especialista en Alergología
Miembro del Comité de Alergia a Himenópteros y Mastocitosis de la SEAIC
Administración de inmunoterapia subcutánea: mucho mas que una inyección subcutánea: La Enfermera de Alergología te lo explica.
Cuantas veces nos han preguntado “¿Eres la enfermera/o de alergia? ¿La que pone las vacunas no?”.
 Pues bien, es el momento de afirmar, que la administración de inmunoterapia (IT) subcutánea no solo consiste en el procedimiento de administración del alérgeno en dosis crecientes al paciente por vía subcutánea, sino que es un proceso donde se realiza previamente una valoración integral del paciente.
Pues bien, es el momento de afirmar, que la administración de inmunoterapia (IT) subcutánea no solo consiste en el procedimiento de administración del alérgeno en dosis crecientes al paciente por vía subcutánea, sino que es un proceso donde se realiza previamente una valoración integral del paciente.
El paciente acude a nuestra consulta con la incertidumbre ante lo desconocido, a pesar de haber recibido información el día de la prescripción del tratamiento por el alergólogo/a, sobre el procedimiento y sus riesgos.
Es importante que nos presentemos, que conozca nuestro nombre, y le indiquemos que somos las enfermeras/os responsables de la administración del tratamiento. Es muy importante que el paciente se encuentre tranquilo.
Así mismo, procederemos a resolver aquellas dudas que pueda tener acerca de la inmunoterapia (IT) específica de alergia, además de informarle que este tratamiento consta de dos fases:
- Fase de Inicio: Donde se irá incrementando de forma periódica la dosis/concentración de la vacuna, comprobando la tolerancia a la misma. En esta fase deberemos preguntar siempre si han tolerado bien la dosis anterior y si han sufrido algún tipo de reacción en su domicilio (reacción tardía).
- Fase de Mantenimiento: Donde se habrá alcanzado la dosis terapéutica que se continuará administrando de forma periódica.
Respecto a la administración del tratamiento, como responsables de su administración, deberemos comprobar siempre: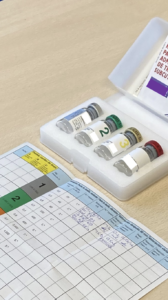
- Que la vacuna que nos entrega el paciente es la que ha prescrito su alergólogo.
- Que corresponde con el nombre del paciente, ya que están identificadas nominalmente.
- La fecha de caducidad.
- Que se ha conservado en nevera (entre 2 y 8 ºC teniendo especial cuidado que no se congele, pues se inactiva y pierde sus propiedades terapéuticas), y trasportada en bolsa térmica .
Procederemos a realizar la valoración de enfermería, recogiendo información sobre su estado de salud:
- Si se encuentra sin síntomas de infección activa (fiebre).
- Si no está presente un episodio agudo (crisis) de su enfermedad alérgica: asma mal controlada o rinoconjuntivitis alérgica.
- Si se encuentra en tratamiento con antibióticos. En cuyo caso se postpondrá la administración hasta su recuperación .
- Si ha recibido en los últimos 7-10 dias vacunas de virus atenuados (gripe, covid…). Como norma general es el intervalo de tiempo mínimo que se recomienda para la administración de la IT específica de alergia.
A continuación procederemos a la toma de constantes vitales (tensión arterial, frecuencia cardiaca, saturación de oxígeno y temperatura) y a la administración del tratamiento de IT específica de alergia siguiendo el protocolo establecido.
Los pacientes deben saber:
- Que tras la administración de su vacuna deben estar un tiempo mínimo de 30 minutos en nuestro servicio de alergia (o Centro de Salud), con el fin de comprobar que ha tolerado bien su IT, y que no han aparecido reacciones adversas inmediatas (por su seguridad).
- Que las reacciones adversas más frecuentes que pueden aparecer son: Enrojecimiento y picor (prurito) en la zona de administración.
- La presencia de síntomas como tos, falta de aire (disnea), aparición de eritemas (zonas enrojecidas en la piel), picor en palma de manos o síntomas exacerbados de su alergia deben ser comunicados inmediatamente para actuar de manera precoz.
- Que la IT especifica de alergia NO sustituye al tratamiento pautado por su alergólogo/a en referencia a antihistamínicos, colirios, inhaladores o nebulizadores nasales. Es un tratamiento conjunto.
- Que no deben practicar ejercicio físico intenso, coger peso, ir a saunas/piscinas cubiertas (ambientes húmedos y cargados) al menos en las 4 primeras horas de la administración de ITSC.
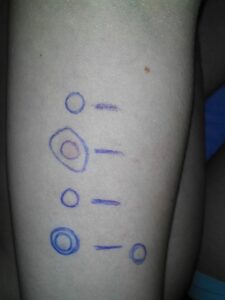
- Que deben informar de la aparición de reacciones tardías (en su domicilio): Aumento de eritema en zona de administración (recomendaremos que se realicen fotos), o cualquier otro síntoma que hayan podido experimentar.
- Que los beneficios de la IT específica de alergia se consiguen a medio/largo plazo y por ello, es necesario que los pacientes acudan a las revisiones programadas por sus alergólogos/as, para valorar la evolución con del tratamiento y si es oportuno continuar con el tratamiento o suspenderlo.
Enterocolitis por proteínas de la dieta en adultos, ¿es realmente una entidad poco frecuente?
En los últimos años asistimos a un incremento muy importante en el diagnóstico y conocimiento de la enterocolitis inducida por proteínas de la dieta (FPIES, del acrónimo en inglés). Aunque se trata de una entidad inicialmente descrita en la edad pediátrica, cada vez observamos más casos en la población adolescente y adulta. En una encuesta realizada en EEUU en el año 2019, se observó que esta entidad puede afectar al 0.22% de la población adulta de este país, si bien desconocemos los datos en nuestro entorno.
En la población pediátrica, el cuadro clínico se caracteriza por la aparición entre 1-4 horas después de la ingesta de vómitos repetitivos, diarrea, decaimiento, flacidez, letargo y en casos severos puede acompañarse de deshidratación y shock. Los alimentos implicados habitualmente en la edad infantil son la leche soja, huevo y cereales. Sin embargo, esto varía en función de la localización geográfica ya que depende mucho de los hábitos dietéticos, por ejemplo, en nuestro país uno de los alimentos más frecuentes, después de la leche y el
huevo, es el pescado.
Por lo que respecta a la población adulta, vemos cada vez con mayor frecuencia en las consultas de Alergología, pacientes que tras la ingesta de marisco, pescado o huevo refieren la presencia de dolor abdominal de tipo cólico, acompañado de diarrea, vómitos y en ocasiones, decaimiento. En muchos casos los enfermos son diagnosticados erróneamente de gastroenteritis aguda o intoxicación alimentaria.
El hecho de que el estudio alergológico (pruebas cutáneas y determinaciones analíticas) sea negativo, así como un periodo de latencia entre la ingesta y la aparición de síntomas más largo que en la alergia mediada por IgE (alergia
típica) junto con la ausencia de síntomas cutáneos y respiratorios, hace que sea difícil su diagnóstico. A esto se suma, que en muchas ocasiones el paciente se limita a evitar la ingesta del alimento implicado y no solicita
valoración médica. Estamos por tanto, ante una entidad infradiagnosticada, en la que la prevalencia es mucho mayor de la que se presupone.
A toda esta complejidad se suma el hecho de que muchos pacientes presentan síntomas con distintos grupos de alimentos (por ejemplo: marisco y pescado, leche y huevo, etc.).
La evolución también varía en función de la edad de presentación. Si el inicio es en la infancia, la evolución es favorable alcanzando la tolerancia con el paso del tiempo, sin embargo, cuando este cuadro aparece en la edad adulta tiende a la cronificación.
En la actualidad no existen biomarcadores que apoyen el diagnóstico, por lo que este se realiza en base a unos determinados síntomas (que varían en función de la edad de presentación) con un amplio diagnóstico diferencial.
Debido a esto, es muy importante que el médico sea conocedor de esta patología para poder llegar a un diagnóstico correcto. En los casos en los que el diagnóstico no esté claro, se puede recurrir al test de exposición controlado,
que debe realizarse siempre en un medio hospitalario con el material necesario y personal entrenado, prácticas habituales en las Consultas de Alergología.
El tratamiento se basa en la evitación del alimento o alimentos implicados y para el episodio agudo se recomienda la reposición de líquidos (en muchos casos por vía intravenosa) y el ondasetrón, que al ser un antagonista selectivo del receptor de la serotonina (5-HT3) en el intestino resulta muy eficaz para paliar los vómitos y la diarrea. La adrenalina no está indicada porque el mecanismo inmunológico subyacente no está mediado por la IgE.
Además, se recomienda seguimiento alergológico para valorar la posible aparición de nuevos alimentos implicados o confirmar si se ha alcanzado la tolerancia, a través de los test de exposición controlada.
Aunque en los últimos años ha aumentado considerablemente el número de publicaciones científicas sobre esta patología, son necesarios más estudios que ayuden a confirmar la verdadera prevalencia de esta entidad, así como para conocer los mecanismos inmunológicos subyacentes y el desarrollo de biomarcadores diagnósticos.
Ana Entrala Bueso. Hospital Paz Research Institute (IdiPaz). Madrid
Purificación Gonzalez-Delgado. Hospital General Universitario. Alicante
Recomendaciones para niños alérgicos y con inmunodeficiencias durante la pandemia COVID-19
En el número especial del Pediatric Allergy and Immunolgy del mes de abril de 2020, a causa de la pandemia COVID-19, aparece esta revisión firmada por destacados especialistas en alergia pediátrica con una serie de recomendaciones a tener en cuenta de cara al manejo del paciente alérgico y/o asmático pediátrico en esta pandemia mundial: Brough, H.A., Kalayci, O., Sediva, A., Untersmayr, E., Munblit, D., Rodriquez del Rio, P., Vazquez‐Ortiz, M., Arasi, S., Alvaro‐ Lozano, M., Tsabouri, S., Galli, E., Beken, B. and Eigenmann, P.A. (2020), Managing childhood allergies and immunodeficiencies during respiratory virus epidemics – the 2020 COVID‐19 pandemic. Mas información aquí
Aunque cualquier persona es susceptible de contagiarse de COVID-19, la edad es el principal factor de riesgo para desarrollar una infección grave1. Afortunadamente, los niños son el rango de población menos afectada2, pero debe garantizarse la atención de otras patologías que puedan presentar.
Las enfermedades alérgicas y el asma son las enfermedades crónicas más comunes en la población infantil3. Con los datos publicados hasta el momento, no hay evidencias de que la alergia aumente el riesgo de enfermedad grave, y solo las inmunodeficiencias y el asma grave mal controlada son factores de riesgo4, por lo que el control del asma tiene que ser óptimo.
Estos son los 6 puntos a tener en cuenta en el manejo del paciente pediátrico con alergia o inmunodeficiencia que expone la revisión citada:
- El alergólogo/a debe buscar el mejor control de los síntomas, instruir al paciente en las recomendaciones de higiene y aislamiento social, y guiar y apoyar al paciente y su familia ante esta situación de incertidumbre.
- Cuando sea posible, deben evitarse los desencadenantes de los síntomas. La alergia estacional que se presentan en primavera puede cursar con asma. A partir del 26 de abril se permita la salida al exterior de niños hasta 14 años de edad, y es aconsejable que en estas salidas los alérgicos al polen de gramíneas eviten zonas ajardinadas.
- Es importante diferenciar los síntomas de alergia de los signos de inicio de infección. Cuando los síntomas se deben a la alergia predominan el picor nasal, ocular, estornudos… Estos empeoran al contactar con el desencadenante y suelen remitir con antihistamínicos. No hay fiebre salvo complicaciones como sinusitis aguda. El asma tampoco cursa con fiebre, y suele mejorar con broncodilatadores.
Sin embargo, en la infección por COVID-19 hay síntomas generales como fiebre, malestar, abatimiento, problemas digestivos y suelen aparecer de manera más progresiva.
- Tratamiento de acuerdo con las guías habituales. No hay evidencia de que el tratamiento habitual de la alergia y el asma (antihistamínicos, broncodilatadores o antileucotrienos) aumenten el riesgo de enfermedad grave. Por lo tanto, se recomienda mantener el tratamiento que tengan indicado para lograr un adecuado control de síntomas.
En el caso del tratamiento con corticoides inhalados, no existen datos de que este tratamiento modifique la susceptibilidad ni la gravedad del COVID-19. Los niños padecen frecuentemente infecciones respiratorias por otros virus como VRS o rinovirus, que predisponen a la hiperreactividad bronquial, y se tratan con corticoides inhalados de forma habitual, sin haberse observado aumento de neumonías o empeoramiento del pronóstico.
Cabe destacar que los fármacos biológicos se han convertido en terapias habituales en muchos pacientes. Aunque no existe una actuación común, el grupo de expertos de la EAACI recomienda mantener el tratamiento biológico en pacientes sanos, y suspenderlo en paciente infectados por COVID-19 hasta la resolución del cuadro.
Se debe evitar la utilización de nebulizadores, ya que generan aerosoles que pueden provocar la difusión del virus. La administración de broncodilatadores debe realizarse usando dispositivos MDI presurizados con espaciador.
5.- Los niños con inmunodeficiencias tienen un riesgo potencial de padecer una enfermedad más grave. En ellos es aún más importante mantener su tratamiento crónico, incluso el inmunosupresor, y extremar las medidas de higiene y distanciamiento social.
6.- Las guías están sujetas a cambios. El conocimiento de esta infección por COVID-19 aumenta día a día, y aunque no se espera que el riesgo en niños crezca, hay que ser flexibles y estar abiertos nuevas evidencias científicas.
Olaya Alvarez García
Sección de Alergoloxía. Complexo Hospitalario Universitario de Ferrol
Comité de Alergia Infantil de la SEAIC
BIBLIOGRAFÍA
- Wu Z, McGoogan JM. Characteristics of and Important Lessons From the Coronavirus Disease 2019 (COVID-19) Outbreak in China: Summary of a Report of 72 314 Cases From the Chinese Center for Disease Control and Prevention. JAMA Published Online First: 24 February 2020. doi:10.1001/jama.2020.2648.
- CDCMMWR. Coronavirus Disease 2019 in Children — United States, February 12–April 2, 2020. MMWR Morb Mortal Wkly Rep 2020: 69. doi:10.15585/mmwr.mm6914e4.
- ENSE Encuesta Nacional de Salud España 2017 Madrid, Ministerio de Sanidad, Consumo y Bienestar Social.
- Garg S, Kim L, Whitaker M et al. Hospitalization Rates and Characteristics of Patients Hospitalized with Laboratory-Confirmed Coronavirus Disease 2019 — COVID-NET, 14 States, March 1–30, 2020. MMWR Morb Mortal Wkly Rep 2020: 69:458–464
CARAT: una herramienta validada para evaluar el control del asma y la rinitis alérgica en la práctica clínica
El Control of Allergic Rhinitis and Asthma Test (CARAT) es un cuestionario diseñado para evaluar el control simultáneo del asma y la rinitis alérgica (RA) en los pacientes, mediante una evaluación retrospectiva de cuatro semanas. Recientemente, un estudio ha realizado una revisión sistemática y un meta-análisis siguiendo las directrices de COSMIN, con el objetivo de evaluar sus propiedades psicométricas.
¿Por qué usar CARAT en la práctica clínica?
La evaluación del control del asma y la rinitis alérgica suele realizarse por separado, con herramientas como el Asthma Control Test (ACT) o el Allergic Rhinitis Control Test (ARCT). Sin embargo, dado que la mayoría de los pacientes con asma también padecen rinitis alérgica, surge la necesidad de una herramienta unificada. CARAT cubre esta brecha con 10 preguntas sobre síntomas de vías respiratorias superiores e inferiores, calidad del sueño, impacto en la actividad diaria y uso de medicación.
Propiedades psicométricas de CARAT
En esta revisión sistemática se incluyeron 16 estudios con los que se concluye que CARAT posee:
- Buena validez de contenido y una adecuada estructura factorial.
- Alta consistencia interna (α de Cronbach = 0.83).
- Alta fiabilidad (coeficiente de correlación intraclase = 0.91).
- Buena validez de constructo, con correlaciones significativas con otros PROMs (ej. ACT y ACQ-5).
- Buena capacidad de respuesta (cambio mínimo importante de 3.5 puntos).
Aplicación práctica
CARAT puede ser administrado en consulta mediante papel puesto que está validado al idioma castellano, pero también está disponible en formato digital a través de aplicaciones móviles como MASK-air y plataformas web, permitiendo un monitoreo continuo del paciente.
Conclusión
Esta revisión sistemática y meta-análisis refuerzan el uso de CARAT como una herramienta confiable para el control del asma y la rinitis alérgica en la práctica clínica habitual. Su implementación puede mejorar el seguimiento de los pacientes y facilitar decisiones terapéuticas más precisas
BIBLIOGRAFIA
Vieira RJ, Sousa-Pinto B, Cardoso-Fernandes A, et al. Control of Allergic Rhinitis and Asthma Test: A systematic review of measurement properties and COSMIN analysis. Clin Transl Allergy. 2022;12(9):e12194.
Diana Q, Abraham A, Yaicith A, Peter O, Juan T. Validation of the Spanish language version of the control of allergic rhinitis and asthma test. NPJ Prim Care Respir Med. 2022;32(1):47. Published 2022 Oct 29.
Sousa-Pinto B, Sá-Sousa A, Amaral R, et al. Assessment of the Control of Allergic Rhinitis and Asthma Test (CARAT) using MASK-air. J Allergy Clin Immunol Pract. 2022;10(1):343-345.e2.
Acta final TC Webex GEAB – 10 febrero 2020
Voto on-line Renovación Junta Directiva 2018
Estimados socios
Se ha abierto el plazo para la emisión de voto on-line para la renovación de cargos de la Junta directiva de la SEAIC en la página web: https://www.seaic.org/profesionales/votaciones-seaic.
Página de acceso para asociados a la SEAIC
Instrucciones
Todos los socios disponen de una cuenta de usuario con una contraseña para acceder a los contenidos de esta página web.
¿Cómo cambiar o recuperar la contraseña?
- Si olvida su contraseña, puede obtener una nueva haciendo click en el texto «Recuperar su contraseña» que encontrará en esta página.
- Atención: para recuperar una contraseña es necesario haber actualizado previamente la dirección de correo electrónico desde el perfil de usuario.
¿Cómo acceder al perfil?
- Al entrar con su contraseña, en lugar del texto «Acceso para asociados» encontrará la opción “perfil” junto a su nombre de usuario en la portada de profesionales.
¿Qué opciones encontraré en mi perfil?
- Nombre de usuario: para evitar duplicados, su «nick» no puede ser modificado pero sí puede cambiar su nombre y apellidos, así como la forma en la que los demás le verán.
- Información de contacto: aquí podremos introducir o modificar nuestra dirección de correo electrónico (imprescindible para recuperar automáticamente su contraseña).
- Quién soy: desde aquí también podremos modificar nuestra contraseña.
Voto on-line renovación de la Junta Directiva
Estimados socios
Se ha abierto el plazo para la emisión de voto on-line para la renovación de cargos de la Junta directiva de la SEAIC en la página web: https://www.seaic.org/profesionales/votaciones-seaic.
Acta del Comité de Asma. Pamplona Octubre 2012
![]() Contenido disponible sólo para socios.
Contenido disponible sólo para socios.
Acta Comité Alergia cutánea 24/10/2019
Acta de Reunión Comité de Alergia cutánea (CAC)
24 Octubre 2019
Maspalomas (Gran Canaria)
![]() Contenido disponible sólo para socios.
Contenido disponible sólo para socios.
Análisis de documentos
ChatGPT
Descripción general: ChatGPT es un modelo de lenguaje basado en inteligencia artificial desarrollado por OpenAI, capaz de analizar, resumir y extraer información clave de textos y documentos en diversos formatos.
Ventajas destacadas:
- Capacidad para comprender y sintetizar información compleja en lenguaje natural.
- Admite múltiples formatos y temas, desde textos científicos hasta documentos técnicos y literatura general.
- Interactividad que permite consultas personalizadas y profundización en temas específicos según las necesidades del usuario.
- Multilingüe, ofreciendo análisis y resúmenes en diversos idiomas.
Desventajas:
- No puede acceder directamente a documentos protegidos o restringidos sin que sean proporcionados.
- Puede tener limitaciones en la interpretación de textos con información altamente técnica o contextos muy específicos.
- La precisión del análisis depende de la claridad y calidad del texto proporcionado.
Modelo de acceso: Acceso gratuito en versiones limitadas, con opciones de suscripción a servicios avanzados (por ejemplo, ChatGPT Plus).
URL de acceso: https://chat.openai.com.
NotebookLM
Descripción general: NotebookLM es una herramienta de toma de notas e investigación desarrollada por Google que utiliza inteligencia artificial para ayudar a los usuarios a analizar, resumir y extraer información clave de documentos cargados, facilitando la comprensión y gestión de grandes volúmenes de información.
Ventajas destacadas:
- Procesa documentos para generar resúmenes, identificar temas clave y sugerir preguntas, permitiendo una comprensión rápida del contenido.
- Proporciona respuestas con citas en línea vinculadas directamente a secciones relevantes de los documentos originales, asegurando precisión y transparencia.
- Acepta diversos tipos de archivos, incluyendo Google Docs, PDFs, presentaciones, URLs de sitios web, videos de YouTube y archivos de audio, ofreciendo flexibilidad en la gestión de información.
- Permite compartir cuadernos y resúmenes de audio, facilitando el trabajo en equipo y la colaboración en proyectos.
Desventajas:
- Cada cuaderno puede contener hasta 50 fuentes, lo que podría ser insuficiente para proyectos de gran envergadura.
- Algunas características aún están en desarrollo y pueden presentar limitaciones o no estar completamente optimizadas.
- Inicialmente, NotebookLM está disponible solo en ciertas regiones, lo que restringe su acceso global.
Modelos de acceso: NotebookLM es una herramienta gratuita que requiere una cuenta de Google para su uso. Los usuarios interesados deben registrarse a través de Google Labs para obtener acceso, ya que actualmente se encuentra en fase experimental.
URL de acceso: https://notebooklm.google.
Humata
Descripción general: Humata es una herramienta de inteligencia artificial diseñada para facilitar la comprensión y el análisis de documentos PDF, permitiendo a los usuarios realizar consultas, obtener resúmenes y extraer información clave de manera eficiente.
Ventajas destacadas:
- Procesamiento rápido de documentos, ofreciendo respuestas instantáneas a consultas específicas.
- Capacidad para resumir textos extensos, facilitando la comprensión de contenido complejo.
- Interfaz intuitiva que permite una navegación sencilla y eficiente.
- Soporte para múltiples idiomas, incluyendo español.
Desventajas:
- La versión gratuita tiene limitaciones en el número de páginas procesadas mensualmente.
- Al ser una herramienta en constante desarrollo, podría presentar limitaciones en la precisión de algunos resultados.
Modelo de acceso: Ofrece una versión gratuita con funcionalidades básicas y planes de suscripción que amplían las capacidades y el acceso a características avanzadas.
URL de acceso: https://www.humata.ai.
Smallpdf AI
Descripción general: Smallpdf AI es una herramienta que utiliza inteligencia artificial para resumir documentos PDF largos, facilitando la comprensión de contenido extenso de manera rápida y eficiente.
Ventajas destacadas:
- Resúmenes concisos y precisos de documentos extensos.
- Interfaz intuitiva y fácil de usar, accesible para cualquier usuario.
- Compatible con múltiples formatos de documentos, más allá de solo PDFs.
- Gratuito para funciones básicas, sin necesidad de instalación adicional.
Desventajas:
- La funcionalidad gratuita puede estar limitada a cierto número de páginas o documentos procesados.
- No ofrece personalización avanzada en los resúmenes generados.
- Depende de la calidad del texto en el PDF; puede no funcionar bien con documentos escaneados o mal estructurados.
Modelo de acceso: Gratuito con funcionalidades básicas; opciones de pago disponibles para características avanzadas.
URL de acceso: https://smallpdf.com/es/ia-pdf.
Soda PDF AI
Descripción general: Soda PDF AI es una herramienta que utiliza inteligencia artificial para interactuar con documentos PDF, permitiendo a los usuarios leer, resumir y explicar el contenido de manera eficiente.
Ventajas destacadas:
- Genera resúmenes concisos de documentos extensos, facilitando la comprensión rápida del contenido.
- Permite realizar consultas específicas sobre el documento, proporcionando respuestas precisas y detalladas.
- Interfaz intuitiva que mejora la experiencia del usuario al interactuar con archivos PDF.
- Accesible desde cualquier dispositivo con conexión a internet, sin necesidad de instalaciones adicionales.
Desventajas:
- La versión gratuita puede tener limitaciones en el tamaño de los archivos y en la cantidad de usos diarios.
- La precisión de los resúmenes y respuestas puede variar según la complejidad y calidad del documento original.
- Al ser una herramienta en constante desarrollo, algunas funcionalidades avanzadas podrían no estar disponibles o completamente optimizadas.
Modelo de acceso: Ofrece una versión gratuita con funcionalidades básicas y planes de suscripción que amplían las capacidades y el acceso a características avanzadas.
URL de acceso: https://www.sodapdf.com/es/chatpdf-ai.
MyMap AI
Descripción general: MyMap AI es una herramienta impulsada por inteligencia artificial que convierte ideas textuales en representaciones visuales, como mapas mentales y presentaciones, facilitando la organización y comunicación de información compleja.
Ventajas destacadas:
- Transforma texto en visuales atractivos, mejorando la comprensión y retención de información.
- Interfaz de chat intuitiva que simplifica la interacción con la herramienta.
- Soporta múltiples formatos visuales, incluyendo mapas mentales y presentaciones.
- Facilita la colaboración en tiempo real, permitiendo a los equipos trabajar conjuntamente en proyectos.
Desventajas:
- Puede requerir conectividad a internet para una funcionalidad completa.
- El contenido generado por IA puede necesitar revisión humana para precisión.
- Posible curva de aprendizaje para usuarios no familiarizados con herramientas de IA.
Modelo de acceso: Ofrece una versión gratuita con funcionalidades básicas y planes de suscripción para acceder a características avanzadas.
URL de acceso:https://www.mymap.ai.
HIX ChatPDF
Descripción general: HIX ChatPDF es una herramienta de inteligencia artificial que permite a los usuarios interactuar con documentos PDF, DOC y TXT, facilitando la comprensión y análisis del contenido mediante conversaciones en tiempo real.
Ventajas destacadas:
- Permite resumir, reescribir, explicar o traducir archivos al instante, agilizando el trabajo con documentos extensos.
- Interfaz intuitiva que facilita la carga y gestión de documentos sin necesidad de registro.
- Soporta múltiples formatos de archivo y ofrece respuestas instantáneas y resúmenes precisos.
- Acceso gratuito sin necesidad de iniciar sesión, con opciones de suscripción para funciones avanzadas.
Desventajas:
- La versión gratuita puede tener limitaciones en el tamaño de los archivos y en la cantidad de usos diarios.
- Al ser una herramienta en constante desarrollo, algunas funcionalidades avanzadas podrían no estar completamente optimizadas.
- La precisión de los resúmenes y respuestas puede variar según la complejidad y calidad del documento original.
Modelo de acceso: Ofrece una versión gratuita con funcionalidades básicas y planes de suscripción que amplían las capacidades y el acceso a características avanzadas.
URL de acceso: https://chat.hix.ai/es/chatpdf.
HiPDF AI Reader
Descripción general: HiPDF AI Reader es una herramienta en línea que utiliza inteligencia artificial para interactuar con documentos PDF, permitiendo a los usuarios resumir, reescribir, explicar y realizar consultas sobre el contenido de manera eficiente.
Ventajas destacadas:
- Genera resúmenes concisos de documentos extensos, facilitando la comprensión rápida del contenido.
- Permite reescribir y explicar secciones específicas del texto, mejorando la claridad y adaptabilidad de la información.
- Ofrece la funcionalidad de realizar preguntas directas al documento, obteniendo respuestas precisas y contextualizadas.
- Interfaz intuitiva y fácil de usar, accesible desde cualquier dispositivo con conexión a internet.
Desventajas:
- La versión gratuita puede tener limitaciones en el tamaño de los archivos y en la cantidad de usos diarios.
- La precisión de los resúmenes y respuestas puede variar según la complejidad y calidad del documento original.
- Al ser una herramienta en constante desarrollo, algunas funcionalidades avanzadas podrían no estar completamente optimizadas.
Modelo de acceso: Ofrece una versión gratuita con funcionalidades básicas y planes de suscripción que amplían las capacidades y el acceso a características avanzadas.
URL de acceso: https://www.hipdf.com/es/ai-read-pdf.
Monica ChatPDF
Descripción general: Monica ChatPDF es una herramienta de inteligencia artificial que permite a los usuarios interactuar con documentos PDF, facilitando la comprensión y análisis del contenido mediante conversaciones en tiempo real.
Ventajas destacadas:
- Genera resúmenes concisos de documentos extensos, mejorando la eficiencia en la revisión de información.
- Permite realizar consultas específicas sobre el contenido del PDF, proporcionando respuestas precisas y contextualizadas.
- Soporta más de 100 idiomas, ampliando su accesibilidad a una audiencia global.
- Interfaz intuitiva que facilita la navegación y el análisis de información.
- Disponible en múltiples plataformas, incluyendo aplicaciones móviles y de escritorio, así como extensiones de navegador.
Desventajas:
- La versión gratuita puede tener limitaciones en el número de consultas o en el tamaño de los archivos procesados.
- Al ser una herramienta en constante desarrollo, algunas funcionalidades avanzadas podrían no estar completamente optimizadas.
- La precisión de los resúmenes y respuestas puede variar según la complejidad y calidad del documento original.
Modelo de acceso: Ofrece una versión gratuita con funcionalidades básicas y planes de suscripción que amplían las capacidades y el acceso a características avanzadas.
URL de acceso: https://monica.im/es/webapp/doc-chat.
Responsabilidad Social Corporativa – Solidaria
| Presidenta: | Dra. María José Pascual Miravalles |
| Secretario: | Don. Agustín Frades Rodríguez |
| Vocales: | Dr. Darío Antolín Amérigo Dra. Carmen Arrieta Pey Dra. Montserrat Bosque García Dra. María Socorro Bustamante Pérez Dra. Inmaculada Pérez Rangel Dr. Tito Rodríguez Bouza Dra. Inmaculada Sánchez Machín Dra. Cesárea Sánchez Hernández Dra. Soledad Terrados |
Colabora con una donación
Objetivos
- Desarrollar y promover prácticas encaminadas a mejorar el bienestar social y sanitario de los grupos humanos sobre los que recae su actividad directa o indirectamente (profesionales médicos, pacientes y sus familiares). La mayoría de los objetivos ya se vienen desarrollando en la Sociedad:
- Apoyar a los socios en el ámbito del conocimiento científico y promover su desarrollo laboral dentro de las competencias de la SEAIC
- Fomentar campamentos de verano para niños asmáticos, alérgicos a alimentos o con reacciones anafilácticas
- Promover programas de educación para el paciente
- Promover programas de educación en las escuelas
- Campañas de Seguridad alimentaria
- Vigilancia de niveles de polen
- Sobre el medio ambiente y la Sociedad en general: Objetivo Solidaridad
- Colaborar en proyectos de Cooperación internacional al desarrollo para lograr la plena realización del derecho a la salud como dimensión básica de una vida digna.
- Con el fin de fomentar la autosuficiencia y la propia capacidad de desarrollo. Aumentando la dignidad y la autoestima de la comunidad a través de un desarrollo sostenible y de una participación activa en la toma de decisiones.
Actualizado el día 11/12/2024
Formación continuada
Proyecto de Desarrollo Profesional Continuado de la SEAIC
Estimado compañero:
La finalidad del proyecto de DPC se basa en el propósito de la Junta Directiva de ofertar desde la propia sociedad por un lado, una serie de actividades formativas de calidad, estructuradas de forma que abarquen la mayor parte de las áreas competenciales del alergólogo y continuadas en el tiempo, y por otro, que el cumplimiento de las mismas sirva para acreditar a los socios con una certificación en la que la SEAIC, al igual que lo implementado por otras Sociedades Científicas, corrobora que el profesional que ha superado el proceso se encuentra actualizado en las competencias exigibles de la especialidad que además podrá constituir la futura base de la recertificación del Alergólogo (ver información adicional en esta misma página).
El proyecto de DPC se ha estructurado en dos niveles: básico y avanzado (ver sección «Actividades»).
— El nivel básico se corresponde con actividades formativas “clásicas” en forma de cursos, talleres o seminarios que a su vez se impartirán en forma on line o presencial, cada vez con mayor protagonismo de la forma on line a través de la plataforma MOODLE en la que la SEAIC ha creado una sección de formación en Alergología.
— El nivel avanzado consistirá en actividades formativas de tipo intensivo, a través de estancias formativas en centros de excelencia en diferentes áreas de la Especialidad.
Con el fin de que la SEAIC pueda proceder a la validación o acreditación del DPC, se ha establecido un baremo, de modo que para acreditar a un profesional en el nivel básico será preciso completar 9 puntos (de un total de 10 posibles) obtenidos en función del número de actividades formativas superadas. El mismo baremo se ha adoptado en el caso del DPC avanzado (ver información adicional).
El período estimado para cumplimentar tanto el DPC básico como avanzado se ha establecido en 5 años, pudiéndose certificar tras la aprobación de los diferentes comités científicos de la SEAIC, las actividades formativas similares a las propuestas realizadas en los últimos 5 años.
- Dr. Manuel Alcántara Villar. Presidente de la Comisión de Formación Continuada y Desarrollo Profesional (CFC)
- Dr. Ignacio Dávila González. Presidente de la SEAIC
Para inscribirse en el proyecto o para consultar sobre cualquier duda al respecto, los socios pueden contactar utilizando el siguiente formulario. Rogamos la comprobación de los datos antes de enviar el mensaje. Una vez enviado y antes de responder a la solicitud, desde Secretaría se comprobará la veracidad del nombre como miembro de la SEAIC y es posible que se requieran datos de confirmación.
| Formulario de contacto |
|
Actualizado el día 01/12/2025
ALFA TRIPTASEMIA HEREDITARIA (HaT), UNA ENTIDAD EMERGENTE EN ANAFILAXIA.
ALFA TRIPTASEMIA HEREDITARIA (HaT), UNA ENTIDAD EMERGENTE EN ANAFILAXIA.
La alfa triptasemia hereditaria es un rasgo genético que ha supuesto un nuevo biomarcador a tener en cuenta, sobre todo entre los pacientes que tienen anafilaxia.
Sin embargo, su diagnóstico está limitado a algunos centros especializados y sus implicaciones clínicas continuan en exploración.
- TRIPTASA.
La actividad tripsina-like se describió por primera vez en mastocitos (MC) en 1960 empleando técnicas histoenzimáticas.(1) Posteriormente, en 1981, se demostró esta misma actividad en los MC humanos de tejido pulmonar,(2) se aisló la enzima con una pureza en torno al 90% y se denominó triptasa (EC 3.4.21.59). La triptasa es producida y almacenada principalmente por los MC, y en una mínima cantidad por los basófilos.(3)
Las protriptasas (α y β) son enzimáticamente inactivas y se liberan de forma constitutiva al plasma, constituyen lo que se determina como triptasa sérica basal (sBT). Tras un proceso de maduración, se producen las triptasas maduras (tetrámeros enzimáticamente activos que forman complejos con la heparina), que se acumulan en los gránulos de los MC. Los tetrámeros activos de β-triptasa y α/β triptasa, se liberan al medio extacelular tras la desgranulación secundaria a la activación mastocitaria, y su determinación resulta de gran utilidad en el diagnóstico de anafilaxia.(4)
Los tetrámeros de β-triptasa madura se comportan como serín proteasas, que actuando sobre el complemento, algunas citoquinas, el fibrinógeno, el cininógeno, prostromelisina y los receptores activados por proteasas (PAR), pueden inducir los siguientes efectos: la proliferación de fibroblastos y músculo liso, la degradación de la matriz extracelular, el reclutamiento de eosinófilos y neutrófilos, la estimulación de células nerviosas y epiteliales, la angiogénesis y la fibrinogenolisis.(5) Sin embargo, los tetrámeros de α-triptasa madura son inactivos.(5,6)
Los heterotetrámeros de α/β triptasa madura, también tienen actividad peptidolítica, siendo su diana los PAR2 presentes en células endoteliales e induciendo extravasación in vitro; y los EMR2 (like module–containing mucin-like hormone receptor-like 2) receptores (proteínas G mecanosensitivas) presentes en la superficie de los MC. La unión de los heterotetrámeros de triptasa madura a este receptor inducen la escisión de la subunidad α del EMR2, y desencadenan la desgranulación mastocitaria(5), mecanismo que se ha relacionado con la urticaria vibratoria.(7) El incremento del número de copias de α-triptasa aumenta la proporción de heterotetrámeros frente a los homotetrámeros llevando a una sobre activación de estos receptores.(8)
La técnica comercial actualmente disponible para la detección de triptasa (ThermoFisher Scientific) es un inmunoensayo que utiliza dos anticuerpos anti-triptasa (el B12 que se emplea para la captura y el G4 para el revelado) siendo el límite inferior de detección de la técnica de 0,5 ng/mL. Esta técnica cuantifica la triptasa total sin distinguir entre formas maduras o precursores, ni isoformas α y β en los fluidos biológicos. El punto de corte establecido para los valores séricos basales de triptasa (sBT) en sujetos sanos es de 11.4 ng/mL.(4)
- ALFA TRIPTASEMIA HEREDITARIA (HαT).
La triptasa en humanos se codifica por 4 genes parálogos TPSG1 (alelos γ), TPSB2 (alelos β2 y β3), TPSAB1 (alelos α y β1), y TPSD1 (alelos δ) localizados en el cromosoma 16p13.3. Presenta diferentes isoformas: α-triptasa, β-triptasa, δ-triptasa y γ-triptasa. El genotipo normal para α y β triptasa contiene 4 copias de los genes, incluyendo estas variaciones 0α:4β, 1α:3β y 2α:2β.(4,9)
También se han descrito variaciones en el número de copias que codifican la β-triptasa, sobre todo en algunos grupos raciales, pero estas variaciones no se asocian con elevaciones de la sBT en las familias. Mientras que, los valores elevados de sBT heredados con patrón dominante en una familia, se asocian con un alelo portador de un gen TPSAB1 que codifica α-triptasa, y se trata de HαT incluso aunque se detecten copias extra de β-triptasa. (4) (Figura 1).
La alfa triptasemia hereditaria (HaT) fue descrita en 2016.(10) Se caracteriza por presentar un número aumentado de copias del gen TPSAB1 que codifica la α-triptasa, tiene un patrón autosómico dominante, se ha descrito en el 4-7% de donantes sanos,(4,6) y asocia un leve predominio entre el género femenino.(11) Los pacientes con HαT suelen tener cifras basales de triptasa (sBT) >11.4 ng/mL; aunque existen casos con valores normales de triptasa (raramente <8 ng/mL). Se recomienda realizar el estudio de HaT en aquellos individuos con sBT >8 ng/mL;(12–14) este punto de corte ha demostrado una sensibilidad del 94% y una especificidad del 100% para detectar copias extra del gen TPSAB1.(12)
Se ha detectado una relación entre el número de copias extra del alelo α del gen TPSAB1 (hasta 4 copias extra) y los niveles de sBT, en familias con HαT+. Parece seguir un patrón por el cual las duplicaciones implican unos niveles de sBT de 15 ± 5 ng/mL, las triplicaciones de 24 ± 6 ng/mL, y las cuadruplicaciones de 37 ± 14 ng/mL.(4)
Además, los valores elevados de sBT se pueden encontrar en otras patologías como las mastocitosis sistémicas (MS), neoplasias mieloides e insuficiencia renal.(7) También se ha publicado en varios estudios, la relación entre los niveles elevados de sBT con la prevalencia y la gravedad de anafilaxia, sin embargo, estos datos deben interpretarse con cautela ya que en muchos de ellos no se ha valorado la presencia concomitante de MC clonales ni de HαT+.(4) En cambio, sí que resulta clara la relación entre HαT+ y las anafilaxias graves desencadenadas por veneno de himenóptero, otras alergias IgE mediadas, así como la asociación con MS.(4)
- GENOTIPADO DE HαT MEDIANTE PCR DIGITAL.
Las PCR (reacción en cadena de la polimerasa) digital, es una tecnología de última generación que se emplea para la cuantificación de ADN de forma reproducible y sensible, y se recomienda para analizar la variación del número de copias. Para llevar a cabo las mediciones, la muestra se divide en particiones, de forma que en cada una de ellas haya cero, una o varias moléculas diana presentes en cada reacción individual. Cada partición es analizada después de un ciclado de PCR en punto final para detectar la presencia (reacción positiva) o ausencia (reacción negativa) de una señal de fluorescencia. Finalmente, se calcula el número absoluto de moléculas presentes en la muestra, sin que los resultados dependan de una curva estándar, de este modo se reduce el error y se incrementa la precisión.(15) Existen en el mercado dos tipos de PCR digital: “Dropled digital PCR (ddPCR)” y “arraybased PCR”. La diferencia principal entre los dos modelos se debe a la estrategia diseñada para la división de la muestra: mediante la formación de gotas tipo emulsión, o mediante el uso de chips compuestos por micropocillos.(16)
Esta técnica detecta las secuencias α y β en los locus de TPSAB1 y TPSB2, a partir de DNA genómico (gDNA) se puede extraer tanto de sangre periférica como de MO.(6) Existe un KIT comercial para conseguir el DNA a partir de un “swab bucal”(17) y posteriormente proceder al estudio de las variaciones en el número de copias de TPSAB1; sin embargo, puede ocurrir que este método se encuentre limitado por problemas de daños y contaminación de las muestras.
- FENOTIPOS DE HαT.(18)
La expresión clínica de HαT puede ser muy variable, desde sujetos asintomáticos (descrito en el 4% de donantes sanos de población española(6), y 1/3 de los portadores) hasta cuadros de anafilaxia grave.(11)
En una reciente revisión, se ha descrito que los síntomas que con mayor frecuencia presentan los pacientes con HαT incluyen: 1) síntomas neuropsiquiátricos (depresión 59%, alteraciones del sueño 69% y alteraciones de memoria 59-68%); 2) síntomas gastrointestinales (colon irritable 30%-60%, nauseas 51%, y reflujo 49%-77%); 3) síntomas secundarios a la liberación de mediadores mastocitarios (flushing 47%, prurito 69%, urticaria 37%, y anafilaxia 14-28%); 4) hiperlaxitud articular 28%; 5) disfunción del sistema autónomo 34% (hipotensión ortostática, palpitaciones, taquicardia, presincope, síncope), y 6) síntomas constitucionales (dolor crónico, astenia 85%).(18,19)
Algunos de los síntomas descritos, aunque se encuentren con una elevada prevalencia, son difíciles de validar como secundarios a HαT+.(18)
Además, los síntomas de HαT+, en muchas ocasiones se pueden superponer con lo que se producen por activación mastocitaria. En este sentido, hay que tener en cuenta que los fenotipos hasta ahora asociados a HαT+ son muy heterogéneos, y que la mayoría de los casos descritos provienen de centros monográficos en patología mastocitaria y/o síndromes genéticos, por lo que es probable la existencia de sesgos en los datos obtenidos a partir de estas poblaciones.(4)
Sí que ha sido validado que los individuos con HαT+ tienen una mayor prevalencia de reacciones de hipersensibilidad inmediata sistémicas. (18)
4.1 HαT Y ANAFILAXIA
La elevación aguda de triptasa es un biomarcador de anafilaxia. El aumento de los valores de sBT triptasa en un 20 % + 2 ng/ml sobre el valor basal de cada individuo en el periodo comprendido entre 1-4 horas desde el inicio del cuadro agudo, es el criterio para confirmar activación mastocitaria y anafilaxia.(20) Esta fórmula tiene una elevada sensibilidad y es útil para identificar anafilaxia en los individuos con exposición parenteral al alérgeno.(21) Sin embargo, se encuentra limitada en algunas circunstancias como en la población pediátrica con alergia a alimentos, y pacientes con reacciones no IgE mediadas. Además, la variabilidad de los niveles de sBT en cada individuo a lo largo del tiempo no está bien estudiada.(22)
Por otra parte, diferentes estudios han identificado los niveles de sBT como un biomarcador asociado con el aumento en la prevalencia y la gravedad de la anafilaxia tras picaduras de insectos (sobre todo himenópteros),(4) y en alergia alimentaria infantil.(23)
HαT+ es el primer modificador genético hereditario descrito para la anafilaxia, que se asocia con un incremento en el riesgo para reacciones alérgicas graves al veneno de himenóptero con un riesgo relativo=2; así como un incremento del riesgo para la anafilaxia idiopática grave(12) y la anafilaxia grave desencadenada por alimentos en niños.(24)
Se ha estimado una prevalencia de HαT+ ≥8.5% en los pacientes con anafilaxia por veneno de himenóptero (HVA) en los que se ha descartado una patología mastocitaria clonal. Además, HαT+ no parece influir en la frecuencia de sensibilización al veneno de himenóptero, sólo influye en la gravedad de la reacción entre los individuos sensibilizados.(25)
También se ha descrito una mayor prevalencia de HαT+ en la anafilaxia idiopática (17%)(25) y en la anafilaxia desencadenada por alimentos en población infantil.(24)
4.2 HαT Y PATOLOGÍA MASTOCITARIA.
HαT+ está asociado a la presencia de patología mastocitaria clonal, encontrándose entre el 12-21% de los pacientes con síndrome de activación mastocitaria clonal (cSAM) y/o MS, sobre todo con formas no avanzadas de la enfermedad -MS indolentes (MSI) y MS quiescentes-.(11)
Un estudio realizado en población adulta española, ha descrito la prevalencia de HαT+ en el 29% de SAM no clonales (ncSAM) y el 18% de las mastocitosis. Entre los casos con mastocitosis, la detección de HαT+ es significativamente más frecuente (21% vs. 10%) entre los casos con la mutación D816V de KIT restringida a mastocitos vs. los casos con la mutación D816V de KIT multilineal. Además, entre los pacientes con mastocitosis, su cuadro clínico debutó con anafilaxia en el 76% vs. 65% (p = 0.18) de los HαT+ vs. HαT–.(6)
El mecanismo subyacente entre ambas entidades no es conocido, pero se ha planteado la hipótesis de que pudiera ser secundario al efecto de mitógeno del exceso de triptasa sobre el microambiente de la médula ósea (MO), promoviendo la selección de los clones aberrantes de MC.(11)
Los pacientes HαT+ con MS tienen una frecuencia de HVA del 30%, y una prevalencia de anafilaxia grave con síntomas cardiovasculares del 35.5%.(11) Así mismo, en población española se ha descrito que los pacientes con mastocitosis tienen una frecuencia de anafilaxia por alimentos del 15% en HαT+ vs. 5% en HαT– (p=0.013).(6)
Si se valora la patología mastocitaria global (clonal y no clonal), se ha descrito que la frecuencia de anafilaxia aumenta progresivamente desde los casos que no tienen alelos para α-triptasa (58%), los que tienen 1 alelo (65%), quienes tienen 2 alelos (72%) y aquellos que tienen ≥3 copias de este alelo (84%). En este estudio, también se describe, que si se analizan sólo los casos HαT+, la frecuencia de anafilaxia es mayor en los que tienen ≥3 copias vs. 2 copias de α-triptasa (82% vs. 61%; p=.017).(6)
- MANEJO DE HAT
Actualmente, para controlar los síntomas que habitualmente presentan los pacientes HAT+, se recomienda emplear el tratamiento antimediador que se suele emplear en la patología mastocitaria.(4) Se ha empleado con éxito el Omalizumab en casos plurisintomáticos complejos, consiguiendo la resolución de la urticaria y de la anafilaxia en el 94% de los pacientes.(13)
MTPS9579A, es un anticuerpo monoclonal humanizado IgG4 anti-triptasa, que inhibe selectivamente la actividad de la triptasa al disociar los tetrámeros activos en monómeros. Este anticuerpo anti-triptasa reduce la gravedad de la anafilaxia IgE mediada en un modelo murino humanizado.(26) Además, se ha desarrollado un modelo farmacocinético/farmacodinámico (PK/PD) para elegir la dosis de anticuerpo anti-triptasa MTPS9579A en pacientes con asma moderado-grave que permite predecir el nivel de exposición y de supresión de la triptasa en los tejidos diana.(27)
Otros estudios, describen anticuerpos monoclonales dirigidos a los receptores inhibidores de los mastocitos, como Siglec-8 (sialic acid-binding immunoglobulin-like lectin 8) [Lirentelimab/AK002], Siglec-6 [AK006], y CD200R [LY3454738].(28)
La eficacia y seguridad de Lirentelimab ha sido evaluado en ensayos clínicos con diferentes patologías en las que participan los mastocitos (incluyendo MSI, urticaria crónica espontanea, dermografismo sintomático, y conjuntivitis alérgica); en todos ellos los pacientes refieren mejoría se los síntomas.(28)
LY3454738 no demostró superioridad frente a placebo en un estudio fase II de urticaria crónica, por lo que esta línea de investigación se ha cerrado. Sin embargo, está pendiente de publicarse sus resultados en un estudio fase I en dermatitis atópica.(28)
AK006 inhibe la anafilaxia IgE mediada en modelos murinos.(28)
Todos estos anticuerpos, podrían abrir líneas de tratamiento de la anafilaxia y de los síntomas de HαT+ en el futuro.
FIGURAS.
Figura. Genotipos de triptasa codificados por TPSAB1 y TPSB2. (18)
BIBLIOGRAFÍA
- Glenner GG, Cohen LA. Histochemical demonstration of a species-specific trypsin-like enzyme in mast cells. Nature. 19 de marzo de 1960;185:846-7.
- Schwartz LB, Lewis RA, Seldin D, Austen KF. Acid hydrolases and tryptase from secretory granules of dispersed human lung mast cells. J Immunol Baltim Md 1950. abril de 1981;126(4):1290-4.
- Castells MC, Irani AM, Schwartz LB. Evaluation of human peripheral blood leukocytes for mast cell tryptase. J Immunol Baltim Md 1950. 1 de abril de 1987;138(7):2184-9.
- Wu R, Lyons JJ. Hereditary Alpha-Tryptasemia: a Commonly Inherited Modifier of Anaphylaxis. Curr Allergy Asthma Rep. 10 de mayo de 2021;21(5):33.
- Lyons JJ. Inherited and acquired determinants of serum tryptase levels in humans. Ann Allergy Asthma Immunol Off Publ Am Coll Allergy Asthma Immunol. octubre de 2021;127(4):420-6.
- González-de-Olano D, Navarro-Navarro P, Muñoz-González JI, Sánchez-Muñoz L, Henriques A, de-Andrés-Martín A, et al. Clinical impact of the TPSAB1 genotype in mast cell diseases: A REMA study in a cohort of 959 individuals. Allergy. 11 de octubre de 2023;
- Khoury P, Lyons JJ. Mast cell activation in the context of elevated basal serum tryptase: genetics and presentations. Curr Allergy Asthma Rep. 27 de noviembre de 2019;19(12):55.
- Zhang H, Zeng X, He S. Evaluation on potential contributions of protease activated receptors related mediators in allergic inflammation. Mediators Inflamm. 2014;2014:829068.
- Caughey GH. Tryptase genetics and anaphylaxis. J Allergy Clin Immunol. junio de 2006;117(6):1411-4.
- Lyons JJ, Yu X, Hughes JD, Le QT, Jamil A, Bai Y, et al. Elevated basal serum tryptase identifies a multisystem disorder associated with increased TPSAB1 copy number. Nat Genet. diciembre de 2016;48(12):1564-9.
- Kačar M, Rijavec M, Šelb J, Korošec P. Clonal mast cell disorders and hereditary α-tryptasemia as risk factors for anaphylaxis. Clin Exp Allergy. 2023;53(4):392-404.
- Robey RC, Wilcock A, Bonin H, Beaman G, Myers B, Grattan C, et al. Hereditary Alpha-Tryptasemia: UK Prevalence and Variability in Disease Expression. J Allergy Clin Immunol Pract. 2020;8(10):3549-56.
- Giannetti MP, Weller E, Bormans C, Novak P, Hamilton MJ, Castells M. Hereditary alpha-tryptasemia in 101 patients with mast cell activation-related symptomatology including anaphylaxis. Ann Allergy Asthma Immunol Off Publ Am Coll Allergy Asthma Immunol. junio de 2021;126(6):655-60.
- Valent P, Akin C, Nedoszytko B, Bonadonna P, Hartmann K, Niedoszytko M, et al. Diagnosis, Classification and Management of Mast Cell Activation Syndromes (MCAS) in the Era of Personalized Medicine. Int J Mol Sci. 27 de noviembre de 2020;21(23):9030.
- dPCR para principiantes [Internet]. Disponible en: https://www.qiagen.com/es-es/applications/digital-pcr/beginners
- Pérez-Barrios, C. PCR digital en la monitorización de la respuesta al tratamiento del paciente oncológico. En: Aplicaciones clínicas de lsa técnicas actuales de Biología Molecular. Cont. Lab. Clin.; 2018. p. 52-8.
- Weiler CR, Austen KF, Akin C, Barkoff MS, Bernstein JA, Bonadonna P, et al. AAAAI Mast Cell Disorders Committee Work Group Report: Mast cell activation syndrome (MCAS) diagnosis and management. J Allergy Clin Immunol. 2019;144(4):883-96.
- Lyons JJ. Hereditary Alpha Tryptasemia: Genotyping and Associated Clinical Features. Immunol Allergy Clin North Am. 2018;38(3):483-95.
- von Bubnoff D, Koch D, Stocker H, Ludwig RJ, Wortmann F, von Bubnoff N. The Clinical Features of Hereditary Alpha-Tryptasemia—Implications for Interdisciplinary Practice. Dtsch Arzteblatt Int. 22 de marzo de 2024;(Forthcoming):arztebl.m2023.0287.
- Valent P, Bonadonna P, Hartmann K, Broesby-Olsen S, Brockow K, Butterfield JH, et al. Why the 20% + 2 Tryptase Formula Is a Diagnostic Gold Standard for Severe Systemic Mast Cell Activation and Mast Cell Activation Syndrome. Int Arch Allergy Immunol. 2019;180(1):44-51.
- Baretto RL, Beck S, Heslegrave J, Melchior C, Mohamed O, Ekbote A, et al. Validation of international consensus equation for acute serum total tryptase in mast cell activation: A perioperative perspective. Allergy. diciembre de 2017;72(12):2031-4.
- Mateja A, Wang Q, Chovanec J, Kim J, Wilson KJ, Schwartz LB, et al. Defining baseline variability of serum tryptase levels improves accuracy in identifying anaphylaxis. J Allergy Clin Immunol. marzo de 2022;149(3):1010-1017.e10.
- Sahiner UM, Yavuz ST, Buyuktiryaki B, Cavkaytar O, Yilmaz EA, Tuncer A, et al. Serum basal tryptase may be a good marker for predicting the risk of anaphylaxis in children with food allergy. Allergy. febrero de 2014;69(2):265-8.
- Lang A, Kubala S, Grieco MC, Mateja A, Pongracic J, Liu Y, et al. Severe food allergy reactions are associated with α-tryptase. J Allergy Clin Immunol. octubre de 2023;152(4):933-9.
- Lyons JJ, Chovanec J, O’Connell MP, Liu Y, Šelb J, Zanotti R, et al. Heritable risk for severe anaphylaxis associated with increased α-tryptase-encoding germline copy number at TPSAB1. J Allergy Clin Immunol. febrero de 2021;147(2):622-32.
- Maun HR, Jackman JK, Choy DF, Loyet KM, Staton TL, Jia G, et al. An Allosteric Anti-tryptase Antibody for the Treatment of Mast Cell-Mediated Severe Asthma. Cell. 3 de octubre de 2019;179(2):417-431.e19.
- Rymut SM, Henderson LM, Poon V, Staton TL, Cai F, Sukumaran S, et al. A mechanistic PK/PD model to enable dose selection of the potent anti-tryptase antibody (MTPS9579A) in patients with moderate-to-severe asthma. Clin Transl Sci. abril de 2023;16(4):694-703.
- Metz M, Kolkhir P, Altrichter S, Siebenhaar F, Levi-Schaffer F, Youngblood BA, et al. Mast cell silencing: A novel therapeutic approach for urticaria and other mast cell-mediated diseases. Allergy. enero de 2024;79(1):37-51.