resultados de la búsqueda: asma/wp-content/uploads/logos/Sitio web no disponible/profesionales/aviso-importante/wwwww/inicio/cme-jiaci
ESOFAGITIS EOSINOFÍLICA EN PACIENTES PEDIÁTRICOS
La esofagitis eosinofílica (EoE) se considera una enfermedad crónica emergente; en la actualidad, ha pasado a ser una de las condiciones más comunes en la valoración y diagnóstico de problemas alimentarios en niños así como en la evaluación de disfagia y/o impactación en la edad adulta.
Se ha estudiado más extensamente en países occidentales, pero, aunque existen datos de prevalencia, se precisan estudios más amplios para consensuar datos epidemiológicos reales. Una revisión sistemática reciente mostró que la prevalencia poblacional de esofagitis eosinofílica en niños es 19,1 casos por 100.000 niños/año (1), con gran variabilidad de los datos según la localización geográfica y, probablemente, de otros factores como el diseño del estudio, los criterios diagnósticos utilizados, etc.
Fisiopatogénicamente se caracteriza por una inflamación Th2 en la que intervienen mecanismos mixtos mediados y/o no mediados por IgE dando lugar a una inflamación eosinofílica en el epitelio esofágico que origina una disfunción del mismo, dando lugar a los síntomas clínicos característicos.
En la población pediátrica los síntomas más prevalentes son los vómitos, dolor abdominal, disfagia, odinofagia e impactación del bolo alimenticio. Estas características clínicas difieren también según la edad del niño, siendo en niños más pequeños (2-8 años) más frecuente: el fallo de medro, rechazo del alimento, dolor abdominal, vómitos, trastornos del sueño, etc. En niños mayores y adolescentes los síntomas se asemejan más a los adultos, presentando disfagia, impactación, odinofagia, regurgitación, etc.
La prueba de oro para el diagnóstico es la toma de biopsias tanto de esófago proximal como distal (aumentando así el rendimiento del estudio) mediante una endoscopia digestiva. Esta técnica precisa de la sedación del paciente, lo que supone un “inconveniente” sobre todo en población pediátrica. Por ello se están estudiando otras técnicas menos invasivas como:
– Prueba del hilo esofágico (EST: esophageal string test), técnica basada en cápsulas que capturan las proteínas asociadas a los eosinófilos de la luz esofágica.
–Citoesponja: tecnología basada también en cápsulas, diseñada originalmente para la evaluación de la mucosa esofágica en el esófago de Barrett.
– Endoscopia transnasal sin sedación.
Estas técnicas y algunas otras en estudio también, podrían tener un papel importante en el control regular de la esofagitis, pero es muy poco probable que reemplacen la confirmación de un diagnóstico dudoso y/o actos terapéuticos realizables durante una endoscopia convencional como una dilatación.
Las opciones terapéuticas, ambas consideradas de primera línea son: tratamiento dietético y farmacológico:
– Terapias dietéticas: la fórmula de aminoácidos se describe como una terapia eficaz en niños con EoE, lo que indica la implicación de antígenos dietéticos en su patogenia. Se han descrito diversos enfoques dietéticos: dieta elemental, dieta dirigida según sensibilización alergénica, dietas empíricas, etc. La dieta de eliminación es una opción no farmacológica de primera línea para el manejo de la EoE; sin embargo, el orden y el número de antígenos específicos a evitar, así como su posterior reintroducción sigue siendo un área activa de investigación.
– Corticoides tópicos: este tipo de fármaco actúa a diversos niveles en esta patología: vías/genes inducidos por IL-13, reducción de la eosinofilia esofágica e infiltración mastocitaria, regulación a la baja de los genes de los mastocitos, reducción de células T y citocinas proinflamatorias como el factor de necrosis tumoral (TNF), etc. Los metanálisis realizados utilizando fluticasona o budesonida demuestran la superioridad de los corticoides frente a placebo para la eosinofilia esofágica, los hallazgos endoscópicos y los síntomas tanto en pacientes adultos como pediátricos. No están exentos de efectos adversos como puede ser la candidiasis, insuficiencia suprarrenal, etc. Los estudios abogan por una terapia que debe ser mantenida a largo plazo por la alta tasa de recaídas tras su retirada. Sigue en estudio la dosis y duración óptima de cada terapia.
– Tratamiento con inhibidores de la bomba de protones (IBP): la tasa de respuesta varía ampliamente desde un 30 a un 70%.Están en estudio las posibles diferencias fisiopatológicas entre la EoE sensible y/o resistente a los IBP. Algunos ejemplos incluyen:
– Técnicas de biología molecular demuestran que la expresión del transcrito para el canal de potasio Kir2.1 (gen KCNJ2) es menor en los pacientes que responden a los IBP. Si se valida, esto podría proporcionar una detección potencial para terapias personalizadas.
– Los pacientes con rinitis alérgica y metabolizadores rápidos CYP2C19 tienen un mayor riesgo de pérdida del control de la EoE a pesar de la terapia continua con IBP.
– Dilatación esofágica: destinada a aliviar complicaciones como la estenosis; técnica destinada a modificar cambios estructurales sin alivio histológico.
– Terapias emergentes:
* Nuevas formulaciones de esteroides: budesonida viscosa, budesonida en comprimidos bucodispersables, etc.
* Tratamientos biológicos: ANTICUERPOS MONOCLONALES
Anti-L5: benralizumab, mepolizumab, reslizumab. Se están realizando estudios para valorar la mejoría tanto clínica como histológica de estos tratamientos, por la involucración de la IL-5 en la infiltración y supervivencia del eosinófilo, sin resultados científicamente concluyentes aún.
Anti-IL13: la IL-13 es un mediador claramente implicado en la patogénesis de la EoE, mediante la activación y quimiotaxis de los eosinófilos a través del aumento de los niveles de eotaxina-3 y periostina. El anticuerpo QAX576 parece reducir los síntomas pero no se ha demostrado efecto significativo en la actividad clínica de la enfermedad; mientras que RPC4046 consigue una reducción significativa de la eosinofilia esofágica y la actividad de la enfermedad endoscópica así como en la reducción de síntomas.
Anti-IL4 y Anti-IL-13: Dupilumab (aprobado por la FDA en > 12 años). Se están llevando a cabo ensayos que parecen demostrar mejoría sintomática, endoscópica e histológica significativa.
Anti-IgE (omalizumab) y Anti-TNF (infliximab). No existe ningún ensayo clínico con evidencia científica que apoye su uso en la EoE.
*Otras dianas moleculares en estudio: Integrina α4β7, Siglec 8, TSLP, TGFβ, canales de calcio, IL- 9, 15 y 33, receptor de eotaxina anti CCR3.
Dra. Guacimara Hernández Santana, Hospital Universitario Nuestra Señora de la Candelaria en Santa Cruz de Tenerife. Comité de Alergia Infantil SEAIC
BIBLIOGRAFÍA:
- Arias A, Perez-Martinez I, Tenias JM, Lucendo AJ. Systematic review with meta-analysis: the incidence and prevalence of eosinophilicesophagitis in children and adults in population-based studies. Aliment Pharmacol Ther 2016; 43(1): 3-15.
- Alfredo J Lucendo (2019): Pharmacological treatments for eosinophilic esophagitis: current options and emerging therapies, Expert Review of Clinical Immunology, DOI:10.1080/1744666X.2019.1705784
- Nirmala P. Gonsalves, Seema S. Aceves. Diagnosis and Treatment of Eosinophilic Esophagitis. J Allergy Clin Immunol. 2020 January ; 145(1): 1–7.
- Thomas Greuter, Ikuo Hirano, Evan S. Dellon. Emerging therapies for eosinophilic esophagitis. J Allergy Clin Immunol. 2020 January ; 145(1): 38–45.
- Arianna De Matteis et al. Eosinophilic Esophagitis in Children: Clinical Findings and Diagnostic Approach.Current Pediatric Reviews, 2020, 16, 206-214.
¿Qué es la anafilaxia?
En esta primera entrada del blog del Comité de Anafilaxia parece lógico que hablemos acerca de lo que es la anafilaxia.
La anafilaxia es una respuesta inmunológica extrema del sistema inmunitario ante una sustancia alergénica a la que el paciente ha desarrollado alergia.
En esta reacción se libera una gran cantidad de histamina y otras sustancias químicas en el cuerpo, lo que causa una serie de síntomas graves, de instauración rápida y potencialmente mortales, especialmente si no se reconocen los síntomas a tiempo y no se actúa rápidamente.
En este caso la reacción alérgica afecta a todo el organismo, y puede manifestarse con síntomas variados y simultáneos en diversos sistemas; por tanto, sus síntomas pueden variar ampliamente, pero comúnmente incluyen síntomas sugestivos de alergia que afectan a la vez la piel, el aparato respiratorio, el tracto digestivo o sistema cardiovascular.
La afectación de la piel, con urticaria, enrojecimiento, picor o hinchazón, es la manifestación más frecuente en la anafilaxia; está presente en el 80 % de los casos.
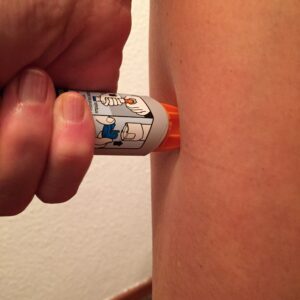
La anafilaxia es una emergencia médica que requiere atención inmediata. El tratamiento principal es la inyección precoz de adrenalina intramuscular en el muslo.
Es crucial, una vez tratado el cuadro, identificar y evitar los desencadenantes conocidos de la reacción para prevenir futuros episodios de anafilaxia. El especialista adecuado para ello es alergólogo, a quien debe ser remitido todo paciente que haya presentado una anafilaxia.
Es importante que las personas alérgicas que hayan presentado una anafilaxia y sus familiares estén preparados para actuar en caso de una nueva reacción anafiláctica. Esto implica llevar siempre consigo una inyección de adrenalina y saber cómo administrarla correctamente
Alergia a Prunáceas
En Verano aumenta el consumo de futas de la familia de las prunáceas, que son aquellas que tienen un hueso que contiene en su interior una especie de almendra, como el melocotón, albaricoque, cereza, ciruela, paraguayo o nectarina. Se consideran responsables del 70 % de todas las reacciones alérgicas a las frutas.
Algunos tips importantes a tener en cuenta son:
- En el área mediterránea predomina la alergia a vegetales por sensibilización a LTP (proteínas transportadoras de lípidos), muy presentes en las prunáceas, especialmente en la piel, donde su concentración es mucho mayor.
- La LTP es un alérgeno muy estable que condiciona que su alergia se produzca con la ingesta de la fruta fresca al igual que procesada (zumos, mermeladas, compotas…)
- Conocer el alérgeno vegetal responsable de la alergia permite predecir la gravedad de las manifestaciones clínicas que puede desencadenar y la posible reactividad cruzada con otros alimentos. La alergia a LTP se puede asociar con alergia a otros alimentos como frutos secos y otras frutas rosáceas (manzana, fresa…)
- Especialmente en el caso de alergia a LTP, algunos factores como el ejercicio físico, el alcohol o los antiinflamatorios (AINE) pueden actuar como cofactores, y desencadenar o amplificar una reacción.
- La alergia a prunáceas en nuestro país, aunque con menor frecuencia, también se puede producir relacionada con la alergia al polen y en este caso, en muchos pacientes, es posible consumir la fruta cocinada. Es aconsejable por tanto, seguir las indicaciones de su alergólogo sobre la evitación o los permisos en las formas de consumo.
La reacción alérgica a las prunáceas como el melocotón se suele producir después de su ingesta y, con menor frecuencia, tras su inhalación o tras el contacto cutáneo. Cuando provoca síntomas, suelen aparecer en la primera hora, habitualmente a los pocos minutos. Los síntomas que puede desencadenar incluyen:
- Síndrome de alergia oral (SAO). Síntomas locales leves, que consisten en picor oral, orofaríngeo y/o ótico. Son los más frecuentes
- Síntomas cutáneos. Síntomas locales en la zona de contacto con el alimento, o generalizados en forma de urticaria y angioedema (hinchazón) de labios, párpados, lengua u otras zonas.
- Síntomas digestivos. Náuseas, vómitos, dolor abdominal, distensión abdominal, diarrea
- Anafilaxia. Reacción alérgica grave de instauración rápida y de riesgo para la vida. Puede iniciarse con picor oral, faríngeo, en manos, pies o cuero cabelludo y después progresar con generalización del picor y aparición de urticaria y/o angioedema, así como síntomas generales respiratorios, digestivos y cardiovasculares (conjuntivitis, obstrucción nasal, estornudos, mucosidad, dificultad para tragar o respirar, tos, silbidos, náuseas, vómitos, dolor abdominal, diarrea, y caída de la tensión arterial con mareo, pérdida de conocimiento, y si la situación se prolonga sin tratamiento, parada cardiorrespiratoria). Se requiere, pues, tratamiento médico urgente en el momento del episodio. En cuanto el paciente advierte la generalización de la reacción, debe administrarse la adrenalina autoinyectable y ser llevado a un centro médico.
Es importante un buen diagnóstico para evitar los alimentos con los que el paciente presente síntomas. Así mismo, siempre llevar consigo la medicación de rescate como antihistamínicos, corticoides y por supuesto la adrenalina autoinyectable.
«Participa en mejorar el conocimiento sobre Inmunoterapia con Alimentos!»
La inmunoterapia es el tratamiento estrella de la especialidad de alergología, claramente diferenciado del resto de tratamientos por su enfoque etiológico. La inmunoterapia con alimentos ha experimentado un auge en las últimas dos décadas que se ha disparado a partir del momento en que la industria farmacéutica ha tomado una posición predominante liderando proyectos de investigación con poblaciones mucho más grandes que las que se reunían mediante iniciativas meramente académicas.
Este desarrollo a nivel de investigación se ha visto respaldado con la nueva publicación de la guía de inmunoterapia europea, en la que por primera vez, se abre una puerta oficial al empleo de inmunoterapia con alérgenos para la alergia alimentaria fuera del contexto de la investigación en centros con un nivel de experiencia y recursos elevado. Hasta la fecha de esta importante publicación, la posición oficial de las organizaciones científicas era la de no recomendar este tipo de tratamiento fuera del contexto de la investigación, a pesar de que su uso se estaba produciendo en determinados centros de muchos países europeos.
En los próximos años, es probable que nos encontremos con productos farmacológicos aprobados para el uso en inmunoterapia oral con alimento, que a su vez, aumenten la demanda de los pacientes para recibir este tipo de tratamiento. Sin embargo, puede darse la situación de que la demanda supere la capacidad de los servicios de alergia para atender dichas peticiones por la complejidad del tratamiento y las dificultades en instaurarlo como parte de la cartera de servicios en departamentos donde no sea un tratamiento en el que no se tenga experiencia.
Con la meta de realizar un mapa a nivel europeo de los centros donde se administra este tratamiento y conocer la forma en que se está realizando, surge el proyecto FIND, del acrónimo en inglés Food Immunotherapy Practice: Nation Differences Across Europe (Práctica de inmunoterapia con alimentos: diferencias entre las naciones en Europa). Este proyecto inicia su camino en Noviembre de 2017, cuando consigue financiación por parte de la EAACI para su puesta en marcha. El grupo de trabajo está constituido por 12 miembros de distintos países europeos y un comité asesor con expertos en alergia a nivel mundial. Tras elaborar un cuestionario, el estudio inicia su fase de recopilación de datos el 20 de Junio de 2018 con el envío de una invitación masiva a todos los miembros de la EAACI para comunicar su experiencia con el tratamiento.
En caso de no haber recibido dicha invitación, y querer participar, puedes hacerlo a través de este link: (https://www.surveymonkey.com/r/FINDproject_Level2) o bien, ponerte en comunicación con el coordinador en nuestro país (find.spain2018@gmail.com) para recibir la información que quieras solicitar y decidir tu participación.
Desde el Comité Infantil de Alergia, os invitamos a participar para que conozcamos cual es la realidad sobre este tratamiento tan relevante.
Pablo Rodriguez Del Rio. Comité de Alergia Infantil SEAIC.
USO Y DESUSO DE LA ADRENALINA
En las últimas décadas el término alergia se ha convertido en un concepto popular y casi familiar, facilitado sobre todo por la incidencia progresivamente creciente de las distintas patologías alergológicas y el impacto socio-sanitario que estas representan.
Por supuesto, entre las varias formas de presentación clínica, la anafilaxia es la que más nos preocupa como médicos, no solo como alergólogos, ya que por definición representa una “reacción alérgica grave de instauración rápida y potencialmente mortal”. En los últimos años se ha multiplicado el esfuerzo de la comunidad científica para sensibilizar a la sociedad sobre esta patología y tratarla como se merece, con el intento de minimizar las consecuencias que de ella puedan surgir.
En el algoritmo de actuación de la anafilaxia, la adrenalina intramuscular representa el tratamiento de primera línea independientemente de la edad del paciente y del entorno en que ocurra. El retraso en la administración de este medicamento se ha asociado a desenlaces fatales o reacciones bifásicas. La administración de adrenalina siempre tiene que estar seguida de una valoración médica por el Servicio de Urgencias más cercano. Una vez resuelto el cuadro clínico, al paciente se le prescribirá un auto inyector de adrenalina con un informe médico en el que deben de estar representados un plan escrito de recomendaciones (alérgeno a evitar) así como una explicación detallada del correcto uso de la adrenalina.
Recientemente se ha publicado un trabajo interesante que investiga las razones por las cuales hay un menor uso de adrenalina en la atención del paciente pediátrico (“Factors associated with the underuse of adrenaline in children with anaphylaxis”). Se trata de un estudio multicéntrico que incluyó 149 pacientes (edad menor de 15 años) atendidos por anafilaxia en 18 Servicios de Urgencias del norte de Francia, en un periodo comprendido entre los años 2015 y 2017. La edad media de los niños incluidos en el estudio era de 7,4 años; 35 niños (23%) estaban diagnosticados previamente de alergia alimentaria y 17 niños (11%) habían ya experimentado una anafilaxia. El Servicio de Emergencia Extrahospitalario de la zona fue contactado en 63 ocasiones (43%), en 55 de ellas (37%) los niños recibieron tratamiento in situ, por sus familias o por el mismo Servicio de Emergencias. Antes de la llegada de ayuda médica, 15 de los 31 niños (48%) con un dispositivo de auto inyector de adrenalina recibieron el tratamiento, mientras que el Servicio de Emergencias solo la administró en 4 de los 55 casos. De los 149 niños diagnosticados de anafilaxia solo 52 de ellos (35% del total) recibieron tratamiento con adrenalina en un entorno hospitalario. En definitiva, solo 71 de los 149 (48%) recibieron tratamiento con adrenalina, y el auto inyector de adrenalina fue prescrito o renovado en 103 (69%) casos antes del alta hospitalaria.
Si analizamos los datos obtenidos en este estudio podemos concluir que se ha observado que la adrenalina fue administrada con más frecuencia en niños más pequeños (edad media de 6,5 años), no identificando otro factor que pueda ser asociado con un uso mas frecuente de adrenalina.
Podemos concluir también que las dos principales razones por las que la adrenalina no se administró en ninguno de los escenarios (intra o extra hospitalario) de asistencia médica fueron:
- subestimación y falta de reconocimiento de la potencial gravedad de la reacción presentada.
- espontánea y rápida mejoría de la clínica desde los primeros síntomas/signos presentados.
El miedo a los posibles efectos adversos de una administración de adrenalina no se reconoció como una causa frecuente para su menor utilización.
Los autores concluyen que la distancia entre el porcentaje de un diagnóstico correcto y los casos que fueron tratados con adrenalina como primera línea de tratamiento sea principalmente debido a no considerar la reacción anafiláctica lo suficientemente grave si ésta no asocia una afectación respiratoria y circulatoria.
En definitiva y como conclusión importante que debemos de sacar de todo este texto es que la administración de adrenalina i.m. es el tratamiento de primera línea para una anafilaxia siendo ésta capaz de reducir las consecuencias potencialmente fatales, antes de que eventualmente se presente una afectación cardiorrespiratoria.
Dr. Nicola Giangrande, del hospital Hospital Público da Mariña , Burela (Lugo). Comité de Alergia Infantil SEAIC.
Articulo aconsejado:
¿En qué consisten las pruebas cutáneas a medicamentos?
Las pruebas cutáneas son útiles para el diagnóstico de la alergia a medicamentos. Existen tres tipos de pruebas cutáneas para el diagnóstico alergológico: prick-test (pruebas intraepidérmicas), pruebas intradérmicas y las pruebas epicutáneas (parches). En el prick test se aplica una gota del medicamento a estudiar en la cara anterior del antebrazo y se hace una ligera punción con una lanceta a través de la gota de dicho medicamento y la capa más externa de la piel conocida como epidermis. De esta forma, se permite que el medicamento penetre y contacte directamente con las células responsables de las reacciones alérgicas, los mastocitos.
Si el paciente presenta un resultado positivo, los mastocitos reaccionan, liberando unas sustancias que producen inflamación, lo que se traduce en la aparición de una roncha o habón, rodeada de un eritema (piel roja). Esta respuesta se inicia en pocos minutos y es máxima a los 15 o 20 minutos y va cediendo a lo largo de las horas.
Si el resultado es negativo, es decir, no se produce la aparición de la roncha, se procede a la prueba cutánea intradérmica. Estas pruebas son más sensibles que las anteriores y consisten en la inyección directa del medicamento en la segunda capa de la piel del paciente (dermis), con una aguja muy fina y se procede a la lectura de forma similar al prick. Está técnica tiene la ventaja de poder investigar la alergia de tipo tardío, que consiste en hacer una lectura a las 24, 48 e incluso 96 horas.
Las pruebas epicutáneas, llamadas también pruebas de parche, consisten en la aplicación sobre la piel, sin punzar, del medicamento sospechoso. Se utilizan generalmente para el diagnóstico de dermatitis de contacto y reacciones tardías, aquellas que aparecen más de 6 horas entre la administración del fármaco y la aparición de la reacción. Se mantiene el alérgeno en la piel, tapado con una tira adhesiva, que se retirará a las 48 horas. La lectura inicial de estas pruebas se realiza a las 48 horas y la respuesta se observa aproximadamente 2 días después de la retirada del parche.
Para realizar las pruebas cutáneas, no se debe de dejar de tomar la medicación habitual. Es importante evitar el tratamiento con antihistamínicos (cetirizina, ebastina, loratadina…) 5-7 días antes de las pruebas y los corticoides orales entre 7 a 21 días antes de las pruebas.
Dra. Giovanna Araujo Sánchez, M.D. PhD.
Servicio de Alergología (ICR).
Hospital Clínic Barcelona. IRCE-IDIBAPS.
Atención del niño alérgico en Urgencias: El Papel del Triaje
Cuando diagnosticamos a un paciente de anafilaxia, le indicamos una serie de medidas de actuación en caso de que presente un nuevo episodio que incluyen la autoadministración de adrenalina y la necesidad de acudir a un centro médico para ser evaluado y tratado. Es más, asumimos que ese paciente será atendido correcta y rápidamente en Urgencias.
Somos poco conscientes del papel que han cobrado los sistemas de Triaje en la mayoría de los servicios de urgencias para hacer frente a la creciente presión asistencial. En los últimos 25 años se han implantado progresivamente múltiples sistemas de triaje hospitalario1, en base a los que se decide cuándo (tiempo de espera), quién (según la organización propia del centro) y dónde (Consulta o Sala de Exploración, Sala de Reanimación…) se atiende a los pacientes. La sala de triaje es donde debe identificarse al paciente con anafilaxia.
Nuestro hospital utiliza el Canadian Paediatric E.D. TRIAGE and Acuity Scale (PaedCTAS)2, con 5 posibles niveles de prioridad (I: Reanimación, de atención inmediata; II: Emergencia, con un tiempo de espera de atención inferior a 15 minutos; III: Urgencia, con un tiempo de espera de unos 30 minutos; IV: Semi urgencia, con tiempo de espera de 1 hora y finalmente, la No Urgencia, con una espera de hasta 2 horas). Estos tiempos recomendados para atender a los pacientes se cumplen en mejor o en peor medida según la afluencia. Según este sistema de triaje una anafilaxia es una patología de prioridad I.
Nos planteamos evaluar la calidad del triaje del niño alérgico a raíz del comentario de un paciente en la Consulta. Nuestro paciente, con anafilaxia previa por alergia a alimentos, siguió todos los pasos indicados en consulta y en su informe clínico, incluidos el uso de su autoinyector y traslado a Urgencias de nuestro hospital. Una vez allí, y tras el triaje, se le envió a la Sala de Espera y fue dado de alta en menos de 2 horas.
Al evaluar triaje en urgencias de pediatría de otros niños atendidos por alergia encontramos que más de la mitad de los niños con diagnóstico de anafilaxia habían recibido una prioridad III (categoría: urgente; prioridad intermedia; tiempo de espera estimado: 30 minutos). En la práctica, una prioridad intermedia supone esperar en la Sala de Espera el mismo tiempo que niños con enfermedades tan frecuentes como la fiebre, gastroenteritis y bronquiolitis. En periodos epidémicos esto se traduce en retrasos de horas por el gran aumento de la demanda asistencial. Además, este retraso podría condicionar peor respuesta a la adrenalina (por su administración más tardía), y aumentar el riesgo de mortalidad. En nuestro centro Sólo un caso de cada 3 fue identificado correctamente como prioridad I-II3.
El siguiente paso fue proponer medidas de mejora de 2 tipos:
- Formación del personal de enfermería que realiza labores de Triaje: Se destacaron la importancia del tiempo de evolución y la duración de síntomas, la importancia de la anamnesis obtenida de los padres sobre la apariencia del paciente al llegar a Urgencias….
- Modificaciones en el propio Sistema de Triaje (no fue posible la implementación de modificaciones en el Soporte informático, por lo que se introdujo material de apoyo (chuleta) al personal encargado del triaje): Se destacó la importancia de la afectación multisistémica, la prescripción y/o el uso de dispositivos de adrenalina autoinyectable y la duración de síntomas.
Al reevaluar el funcionamiento de nuestra urgencia 12 meses después de estas medidas, encontramos que el número de niños correctamente triados había pasado del 36.2 % al 72.2 % y lo que es más importante, que el tiempo de espera medio se había reducido de 8 min a 1 min. También se observaron modificaciones en la ubicación de los pacientes, que, en lugar de ser enviados a la sala de espera, quedaron en observación4.
Nuestros resultados no son extrapolables a otros hospitales dado que en nuestro país se utilizan varios sistemas de triaje distintos, incluyendo, entre otros, el Sistema Canadiense de Triaje Pediátrico, Sistema Estructurado de Triaje-Modelo Andorrano de Triaje, Sistema Manchester de Triaje5. Cada uno de estos sistemas consta de procesos propios en su aplicación e idiosincrasia a la hora de gestionar la prioridad de los pacientes y de las patologías. Además, precisan de formación específica para su aplicación.
Como alergólogos:
- Debemos ser conscientes de que el triaje del servicio de urgencias es clave para que el paciente diagnosticado de anafilaxia reciba el tratamiento adecuado en el momento preciso.
- Deberíamos conocer el sistema de triaje que se utiliza en nuestros hospitales y saber si tiene (o no) problemas en la identificación de los pacientes con anafilaxia.
- Debemos colaborar con el personal de urgencias para, desde nuestro conocimiento de las peculiaridades de la anafilaxia, proponer medidas de mejora que faciliten la identificación precoz y por tanto, la atención correcta de los pacientes.
Dra. Esozia Arroabarren Alemán, Servicio de Alergia, Complejo Hospitalario de Navarra, Pamplona. Comité de Alergia Infantil SEAIC
Bibliografía
- Mínguez Navarro MC, Guerrero Márquez G, Ignacio Cerro MC, editores. Manual de Clasificación y Triage del paciente Pediátrico en Urgencias. Primera Edición. Majadahonda (Madrid): Ergon; 2015.
- Warren DW, Jarvis A, LeBlanc L, Gravel J; CTAS National Working Group; Canadian Association of Emergency Physicians; National Emergency Nurses Affiliation; Association des Médecins d’Urgence du Québec; Canadian Paediatric Society; Society of Rural Physicians of Canada. Revisions to the Canadian Triage and Acuity Scale paediatric guidelines (PaedCTAS). CJEM. 2008; 10(3):224-43.
- Arroabarren E, Alvarez-Garcia J, Anda M, de Prada M, Ponce MC, Palacios M. Quality of the Triage of Children With anaphylaxis at the Emergency Department. Pediatr Emerg Care. 2018 May 15. doi: 10.1097/PEC.0000000000001442
- Arroabarren E, Alvarez-García J, Anda M, de Prada M, Ponce C, Alvarez-Puebla MJ. Impact of specific training in anaphylaxis of the Triage nursing staff in a Tertiary Hospital’s Paediatric Emergency Department. J Investig Allergol Clin Immunol. 2018 May 2:0. doi: 10.18176/jiaci.0271.
- https://www.aetsa.org/download/publicaciones/antiguas/AETSA_2011-4_Triage_def.pdf (ultimo acceso: junio 2019)
Premios Best in Class
Apreciados socios:
Se adjunta carta de nuestro Presidente con información importante con respecto a la convocatoria de los premios Best in Class sobre la calidad de los servicios de Alergología del sistema sanitario público.
Un cordial saludo.
Dr. Pedro Ojeda
Secretario General Sociedad Española de Alergología e Inmunología Clínica
—————————————–
Documento para la descarga:
Programas para alergólogos jóvenes
La SEAIC anuncia el lanzamiento conjunto de 3 programas para Jóvenes alergólogos, con el objeto de ofertar una formación integral y focalizados en distintos aspectos:
- Inmunoterapia – Programa ExperAIT. Límite para presentar solicitudes: 11 de mayo.
- Alergia cutánea grave – Programa REacciona. Límite para presentar solicitudes: 12 de mayo.
- Alergia a los alimentos – Programa ALiAdos. Límite para presentar solicitudes: 15 de mayo.
IMPORTANTE: Los programas son mutuamente excluyentes. En caso de participar en uno, no se podrá participar en otro, para dar oportunidades a más personas.
![]() Convocatoria programa ExperAIT (2369 descargas )
Convocatoria programa ExperAIT (2369 descargas )
![]() Agenda programa ExperAIT (2383 descargas )
Agenda programa ExperAIT (2383 descargas )
![]() Convocatoria programa REacciona (2506 descargas )
Convocatoria programa REacciona (2506 descargas )
![]() Convocatoria programa ALiAdos (2955 descargas )
Convocatoria programa ALiAdos (2955 descargas )
Escombroidosis
Lo que puede parecer una alergia a pescado pero no serlo
En los últimos meses hemos visto publicaciones de varios casos de intoxicaciones alimentarias con pescados en algunos comedores escolares, desde el Comité de Alergia a Alimentos de la SEAIC consideramos conveniente aclarar algunos conceptos que han sido empleados como “sinónimos” en algunos medios de comunicación sin serlo realmente.
Los peces pertenecientes a la familia de los escómbridos, entre los que se encuentran el atún blanco, el atún rojo, el bonito o la caballa, tienen un elevado contenido en histidina. Si estos peces o pescados ya cocinados no se mantienen en condiciones adecuadas de conservación y refrigeración, la musculatura de los mismos sufre una descomposición bacteriana que transforma la histidina que contienen en histamina. La histamina es la sustancia o mediador que se libera en la reacciones de alergia mediante un mecanismo inmunológico. De este modo su presencia en el pescado que se va a ingerir puede dar cuadros que parezcan una reacción alérgica sin realmente serlo.
Característicamente pueden producir enrojecimiento o flushing, cefalea, diarrea, palpitaciones e incluso hipotensión. Por todo ello el origen de los síntomas (intoxicación versus alergia) puede ser confuso en ocasiones. Sin embargo hay algunos detalles que pueden ayudar a diferenciarlos:
1-. En el caso de la escombroidosis la histamina se encuentra en el pescado, lo que hace que cualquiera que lo consuma pueda presentar los síntomas que acabamos de mencionar. Por ello, es frecuente que aparezcan varios casos simultáneos o cercanos en el tiempo. En lo que a alergia se refiere, el origen de la liberación de histamina es el propio individuo, de manera que la aparición de clínica “colectiva” es rara.
2.- En personas susceptibles la alergia a pescado puede aparecer frente a cualquier especie, mientras que la escombroidosis sólo sucede con el consumo de las especies que contienen elevadas cantidades de histidina.
3-. En la escombroidosis los síntomas raramente ponen en peligro la vida. En contraposición, la alergia puede producir desde síntomas leves a otros de mayor severidad, que precisen tratamiento urgente.
4-. Ante un caso de alergia a pescado es preciso realizar una eliminación adecuada de la especie o especies origen de la clínica. Sin embargo, tras un episodio de escombroidosis se podría volver a consumir el mismo pescado siempre y cuando éste haya pasado antes por unas adecuadas condiciones de conservación y refrigeración, tal y como exige la Normativa sobre manipulación de alimentos.
Con todo esto sólo queremos recordar que en lo que a la alergia al pescado se refiere, ser y parecer no es lo mismo, y que llamar a cada cosa por su nombre es importante porque el tratamiento y las medidas de evitación difieren.
Anafilaxia en el lactante.
En los últimos meses se han publicado varios artículos acerca de la anafilaxia en el lactante.
Cárdenas Morales y Hernández Trujillo (1) nos dan una visión global a través de una revisión. Carlisle y Lieberman (2) se centran en el manejo del episodio y Frith y colaboradores actualizan las guías de la Australasian Society of Clinical Immunology and Allergy (ASCIA) (3).
La incidencia de la anafilaxia está aumentando particularmente en los lactantes y preescolares, aunque los datos son limitados y las cifras varían según los diferentes autores.
Las peculiaridades del lactante incluyen diferencias en la presentación clínica, las comorbilidades asociadas, dificultades en el diagnóstico y en el tratamiento, siendo por todo ello aún menor la frecuencia de utilización de adrenalina que en otras edades.
Como factores de riesgo en lactantes hay que considerar comorbilidades como el asma, la bronquiolitis y la laringotraqueobronquitis. Entre los posibles cofactores se incluyen la fiebre, infecciones respiratorias y el estrés. No parece haber acuerdo (1,2) en el papel del eccema atópico como comorbilidad de interés en anafilaxia.
Los síntomas más frecuentes en lactantes suelen ser cutáneos, seguidos de los respiratorios y digestivos. Los síntomas cardiovasculares parecen ser menos frecuentes o peor detectados. Además, la sintomatología puede pasar de tener valor diagnóstico a ser inespecífica según el contexto clínico, o pasar desapercibida por ser específica del lactante (Tabla 1) (2). También debemos tener en cuenta que el diagnóstico diferencial es amplio, con entidades propias de esta edad (Tabla 2)(1).
La alergia alimentaria es el principal desencadenante, destacando la leche y el huevo como los principales implicados. Sin embargo, hay que tener en cuenta los hábitos de consumo local. En nuestro medio las frutas y pescados son también causa frecuente de anafilaxia (1).
En cuanto al diagnóstico en el lactante, se han identificado varias dificultades
- La imposibilidad a esta edad de comunicar síntomas verbalmente
- Las diferencias entre las distintas definiciones de anafilaxia. Aunque los criterios de Sampson et al está muy extendidos y se consideran aplicables también en este grupo de edad, algunas sociedades como la ASCIA no incluyen la sintomatología digestiva como criterio de anafilaxia
- La determinación de triptasa suele tener limitaciones en el caso de la anafilaxia inducida por alimentos y no se han determinado puntos de cortes específicos a esta edad.
El tratamiento se basa en el reconocimiento de síntomas, y en la administración precoz de adrenalina. Como medidas adicionales, la guía ASCIA recomienda específicamente evitar que los lactantes estén en brazos sobre el hombro de sus cuidadores y recomienda que se mantengan horizontales sobre los brazos del cuidador (3). Aunque pueden ser necesarias medidas adicionales como la fluidoterapia, apenas se mencionan otros fármacos, como los antihistamínicos y corticoides (2), acerca de los que sí se discutía en revisiones previas (4,5).
La infrautilización de adrenalina se ha atribuido a un peor reconocimiento de los síntomas, pero también a una menor prescripción de dispositivos de adrenalina. Una de las razones se debe a que en lactantes hay discordancia entre el peso y la dosis de los autoinyectores disponibles (0.15 y 0.3 mg). Tanto la guía de anafilaxia pediátrica de EAACI de 2007(6) como la australiana proponen la prescripción de dispositivos de 0.15mg lactantes-niños a partir de los 7.5 kg de peso (3). En 2017 la Food and Drug Administration autorizó la comercialización de dispositivos de 0.1mg en Estados Unidos, por lo que las recomendaciones en este punto varían según la guía consultada (1,2,4).
Finalmente, desconocemos aun el efecto de las recomendaciones actuales de introducción precoz de la alimentación complementaria en la incidencia y prevalencia futuras de anafilaxia en lactantes.
| Órgano Diana | Síntoma Típico propio de otras edades | Síntoma poco frecuente…o propio de lactante |
| Piel | Habones, rash, picor, angioedema | Roce ocular, picor ocular, rascado de las orejas, sacar la lengua, lamido repetido de labios o de las manos |
| Digestivos | Vómitos, diarrea, dolor abdominal | Escupir, arquear la espalda, llevarse las rodillas al pecho, hipo |
| Respiratorios | Tos, sibilancias taquipnea | Llanto, afonía, meterse los dedos en la orejas, tirarse de las orejas |
| Cardiovascular | Hipotensión, desmayo, sincope | Piel moteada |
| Neurológico | Irritabilidad, llanto inconsolable, letargo |
Tabla 1. Síntomas de anafilaxia en lactantes. De A Carlisle y J. Lieberman
| Signo/Síntoma Guía | Diagnóstico alternativo |
| Angioedema | Angioedema Hereditario
Celulitis |
| Diarrea | Gastroenteritis |
| Habones/Rash | Dermatitis de contacto
Eritema multiforme Mastocitosis Síndrome de piel escaldada estafilocócica Síndrome de shock tóxico |
| Hipotensión | Shock séptico |
| Neurológico | Intoxicación por fármacos o alcohol
Encefalitis Hemorragia intracraneal Meningitis Traumatismo no accidental (maltrato) Convulsión |
| Dificultad respiratoria | Asma
Espasmo del Sollozo Bronquiolitis Crup Aspiracion de cuerpo extraño Membrana laríngea Traqueolaringomalacia Anillo vascular |
| Vómitos | Enterocolitis inducida por proteínas alimentarias (FPIES)
Intoxicación alimentaria Gastroenteritis Reflujo gasotroesofágico |
| Otros | BRUE (episodios breves resueltos inexplicado: brief resolved unexplained) **
Síndrome de Munchausen Síndrome de muerte súbita del lactante |
Tabla 2. Diagnóstico diferencial de anafilaxia en lactantes **Denominación actual del Episodio Aparentemente Letal
Esozia Arroabarren Aleman. Servicio de Alergología. Complejo Hospitalario de Navarra. Comité de Alergia Infantil SEAIC
Bibliografía
- Cardenas-Morales M, Hernandez-Trujillo V. Infant Anaphylaxis: A Diagnostic Challenge. Curr Allergy Asthma Rep. 2021 Feb 23;21(2):12. doi: 10.1007/s11882-021-00990-4.
- Carlisle A, Lieberman J. Clinical Management of Infant Anaphylaxis. J Asthma Allergy. 2021 Jul 8;14:821-827. doi: 10.2147/JAA.S286692.
- Frith K, Smith J, Joshi P, Ford LS, Vale S. Updated anaphylaxis guidelines: management in infants and children. Aust Prescr. 2021 Jun;44(3):91-95. doi: 10.18773/austprescr.2021.016.
- Greenhawt M, Gupta RS, Meadows JA, Pistiner M, Spergel JM, Camargo CA, Jr, et al. Guiding principles for the recognition, diagnosis, and management of infants with anaphylaxis: an expert panel consensus. J Allergy Clin Immunol Pract 2019;7:1148-1156.e5. 10.1016/j.jaip.2018.10.052 –
- Simons FE, Sampson HA. Anaphylaxis: Unique aspects of clinical diagnosis and management in infants (birth to age 2 years). J Allergy Clin Immunol. 2015 May;135(5):1125-31. doi: 10.1016/j.jaci.2014.09.014.
- Muraro A, Roberts G, Clark A, Eigenmann PA, Halken S, Lack G, Moneret-Vautrin A, Niggemann B, Rancé F; EAACI Task Force on Anaphylaxis in Children. The management of anaphylaxis in childhood: position paper of the European academy of allergology and clinical immunology. Allergy. 2007 Aug;62(8):857-71. doi: 10.1111/j.1398-9995.2007.01421.x.
Falsos mitos sobre el deporte en niños asmáticos
El deporte no sólo no es contraproducente, sino que resulta saludable para los niños que padecen asma. La actividad física mejora el desarrollo del niño y la condición física, ayudando a disminuir la intensidad de las crisis asmáticas.
Descargar tríptico: ![]() Falsos mitos sobre deporte y asma (5648 descargas )
Falsos mitos sobre deporte y asma (5648 descargas )
Fallecimiento Dr. Baena-Cagnani
Estimados socios,
El ilustre Dr.Carlos E. Baena-Cagnani falleció súbitamente recibiendo el año 2015 con sus hijos y nietos en Ascochinga, Provincia de Córdoba, Argentina.
Comenzó su formación como alergólogo, en la Universidad de Navarra (Pamplona) con su jefe y maestro, Dr. Alberto Oehling. Participó muy activamente en diferentes Sociedades Científicas que presidió, como la Asociación Argentina de Alergia e Inmunología Clínica, la Sociedad latinoamericana de Alergia, Asma e inmunología, la Organización Mundial de Alergia (WAO), y actualmente presidía la Asociación Global de Asma (Interasma). Desde la SEAIC queremos transmitir nuestro más sentido pésame a su familia y amigos. Su muerte es una pérdida irreparable para nuestra especialidad, para la que trabajó incansablemente a lo largo de su vida profesional. Descanse en paz.
Darío Antolín
Secretario de la Junta Directiva de la SEAIC
Reunión CYNA 2025
La SEAIC y GSK reúnen a más de 400 expertos en alergología para abordar novedades en asma, exposoma y reacciones a alimentos y medicamentos
- La XXI edición de la reunión de Controversias y Novedades en Alergia (CYNA) ha analizado los avances en el manejo del asma, las reacciones alérgicas a fármacos y a alimentos, así como la influencia del exposoma.
- El encuentro, organizado por GSK con el aval de la Sociedad Española de Alergología e Inmunología Clínica (SEAIC), ha contado con la participación de 12 ponentes nacionales y 5 internacionales.
Congreso Centroamericano y del Caribe
Estimados socios,
El comité organizador del XIII Congreso Centroamericano y del Caribe de Alergia, Asma e Inmunología, y el VII Congreso Nacional de Alergología e Inmunología Clínica, envía la invitación para todo aquel socio interesado. Las fechas de celebración serán del 19 al 21 de Agosto en el Hotel Hilton de la Ciudad de Panamá. Para más información podéis consultar el archivo pdf adjunto. Esperamos que sea de vuestro interés,
Un cordial saludo
Darío Antolín
Secretario de la Junta Directiva de la SEAIC
Elecciones EAACI
Apreciados socios:
La Dra. Cardona nos informa de la apertura del proceso de presentación de candidaturas para los Board de cada una de las secciones de la EAACI. Os incluimos las instrucciones para que el que quiera forme parte de la sección o del grupo de interés que le apetezca. Os animamos a presentaros para aumentar así la presencia de la Alergología española en el resto de Europa.
Un cordial saludo.
Dr. Pedro Ojeda
Secretario General de la Sociedad Española de Alergología e Inmunología Clínica
Elecciones en EAACI
Todos los miembros de EAACI pueden pertenecer a una sola Sección (Asma, Rinitis, Dermatología, Pediatría o Inmunología) y se pueden apuntar a todos los Grupos de Interés que quieran (Aerobiología y contaminación; Alergia, Asma & Deporte; Diagnóstico en Alergia; Enfermería; Productos Biológicos; Alergia a Medicamentos; Epidemiología; Alergias a los Alimentos; Genómica Funcional y Proteómica; Inmunoterapia; Infecciones y Alergias; Hipersensibilidad a Veneno de Insectos; Alergia ocupacional; y Alergia Ocular).
En la actualidad se ha abierto la candidatura a los «Board», para que entren 2 nuevos miembros en cada uno. Las elecciones serán por vía electrónica en Marzo. Cada miembro podrá votar en su Sección y sus grupos de interés.
Estándares mínimos de Informes
Ya pueden descargarse los estándares mínimos para informes de asma, rinoconjuntivitis y reacciones adversas a medicamentos. Aquí y en el área Profesional>>Descargas>>Documentos.
![]() Estándares mínimos para informes de asma (1005 descargas )
Estándares mínimos para informes de asma (1005 descargas )
![]() Estándares mínimos para informes de rinoconjuntivitis (7323 descargas )
Estándares mínimos para informes de rinoconjuntivitis (7323 descargas )
![]() Estándares mínimos para informes de alergia a medicamentos (721 descargas )
Estándares mínimos para informes de alergia a medicamentos (721 descargas )
Beneficio coste-efectivo de la inmunoterapia
El ratio de incremento de costo-efectividad (ICER por sus siglas en inglés) se utiliza en la economía de la salud para analizar el coste-efectividad de una intervención en salud en comparación con una alternativa. En el caso de la inmunoterapia específica con alérgenos (ITA), se compararía con el uso de medicación para el control de los síntomas causados por la exposición al alérgeno. Este índice permite evaluar si el coste añadido de un tratamiento está justificado por los beneficios adicionales en la salud que provee.
La efectividad usualmente se mide en resultados de la salud como por ejemplo, la calidad ajustada por año de vida (QALYs, por sus siglas en ingles) o por años de vida ajustados por discapacidad (DALYs); estos cuantifican tanto la calidad como la cantidad de calidad de vida que se gana con una intervención.
El ICER se calcula dividiendo la diferencia en coste de ambos tratamientos entre la diferencia en efectividad entre ambos tratamientos. Un ICER bajo significa que el tratamiento evaluado provee mejores beneficios en salud por un coste adicional menor siendo coste-efectivo; mientras que, un ICER alto sugiere que el nuevo tratamiento es más costoso comparado a los beneficios de salud que provee.
Una revisión sistemática buscando el ICER de la ITA comparada con tratamiento sintomático encontró estudios de alta y media calidad que sugieren que la inmunoterapia específica con alérgenos es coste-efectiva tomando en cuenta el estándar del sistema nacional de salud para el Reino Unido que considera que una intervención es coste-efectiva por debajo de las 20mil libras esterlinas por QALY (1).
De los estudios analizados con alta calidad, demostraba que el uso de GRAZAX o la inmunoterapia especifica con alérgenos con tabletas sublinguales (ITA-SL) en pacientes con rinitis y asma, el ICER para la ITA-SL era de £8816 por QALY en los precios de 2005 (£10 726 por QALY en 2014/15 ajustado por inflación)(2). Otro estudio con ITA-SL demostró que en la población específica de 5-16 años de edad con rinoconjuntivitis con o sin asma, también era costo efectivo con un ICER de £12 168 por QALY con precios de 2008 (un ICER de £13 357 por QALY para precios de 2014/2015)(3).
Uno de los estudios con calidad media, realizado en la población adulta con rinoconjuntivitis tratada con ITA subcitánea (ITA-SC); sugiere que el ICER para la ITA-SC en comparación con medicación sintomática era de £8866/QALY para Austria, £2360/QALY para Dinamarca, £12 486 para Finlandia, £9399 para Alemania, £22 374 para Suecia y £20 691 para Países Bajos actualizados a precios de 2014/2015. (4)
Recientemente, una revisión de la literatura científica hace referencia a nueva evidencia que demuestra que la ITA tanto subcutánea como sublingual en la población pediátrica con alergia a ácaros del polvo y con alergia a gramíneas, ambas, sí son costo-efectivas durante los años evaluados (5).
Otro beneficio del uso de la ITA para mejorar la calidad de vida e incentivar el ahorro a futuro en tus pacientes con alergia a aeroalérgenos.
Bibliografía
- Asaria M, Dhami S, van Ree R, et al. Health economic analysis of allergen immunotherapy for the management of allergic rhinitis, asthma, food allergy and venom allergy: A systematic overview. Allergy. 2018;73(2):269-283. doi:10.1111/all.13254
- Nasser S, Vestenbaek U, Beriot-Mathiot A, Poulsen PB. Cost-effectiveness of specific immunotherapy with Grazax in allergic rhinitis co-existing with asthma. Allergy. 2008;63(12):1624-1629. doi:10.1111/j.1398-9995.2008.01743.x
- Ronaldson S, Taylor M, Bech PG, Shenton R, Bufe A. Economic evaluation of SQ-standardized grass allergy immunotherapy tablet (Grazax(®)) in children. Clinicoecon Outcomes Res. 2014;6:187-196. Published 2014 Apr 8. doi:10.2147/CEOR.S44079
- Keiding H, Jorgensen KP. A cost-effectiveness analysis of immunotherapy with SQ allergen extract for patients with seasonal allergic rhinoconjunctivitis in selected European countries. Curr Med Res Opin. 2007; 23: 1113-1120.
- 5.Rodríguez-Otero N, Ramírez-Mateo E, Plana MN, Heffler E, Antolín-Amérigo D. Cost-effectiveness of allergen immunotherapy. Curr Opin Allergy Clin Immunol. Published online September 18, 2024. doi:10.1097/ACI.0000000000001028
Plan Estratégico
Plan estratégico de la SEAIC 2011-18
Justificación del proyecto
Desde su creación la Sociedad se constituyó en una asociación de carácter científico y profesional y se ha regido, como es habitual en el mundo de sociedades científicas, por unos estatutos que señalan sus fines y competencias, y que textualmente son:
- Fomentar y dar a conocer los estudios sobre Alergología e Inmunología Clínica.
- Promover y facilitar el contacto de sus miembros entre sí y con otros profesionales o entidades afines.
- Contribuir a la formación y perfeccionamiento profesional en Alergología e Inmunología Clínica.
- Propiciar cualquier tipo de intercambio e iniciativa (no exclusivamente científico profesional) entre los socios, que contribuya a la buena marcha de la Sociedad.
- Intervenir como tal Sociedad en los problemas que puedan afectar a sus miembros, al ejercicio profesional, a la Especialidad, a la Sanidad y a la Salud Pública.
- Promover programas educativos para el público en general, encaminados a dar a conocer las enfermedades inmunoalérgicas, su prevención, tratamiento y cualquier actividad relacionada con este fin.
Es competencia de la Sociedad:
- Organizar o patrocinar en las condiciones que puedan determinarse, reuniones de Alergología e Inmunología Clínica en cualquiera de sus formas y celebrar congresos y simposios nacionales o internacionales.
- Potenciar la formación científica y profesional de sus miembros estimulando toda clase de actividades científicas. Ayudar a sus miembros en la tarea y en la proyección de sus actividades en toda clase de manifestaciones científicas. El copyright de los trabajos de investigación patrocinados por la SEAIC u organismos dependientes de la misma pertenecerán a ésta.
- Mantener un servicio de información referido a la Especialidad entre sus miembros.
- Colaborar con otras entidades científicas, nacionales y extranjeras especialmente con las de Alergología e Inmunología Clínica.
- Cualesquiera otros medios adecuados para el cumplimiento de los fines señalados.
La interpretación de las formas más idóneas para la consecución de estos fines ha quedado al libre albedrío de las sucesivas juntas directivas, lo cual ha generado problemas importantes entre los que se encuentran:
- Toma de decisiones trascendentes por una (presidente) o pocas personas, con falta de participación de otros actores relevantes.
- Falta de previsión para afrontar los cambios del futuro.
- Inexistencia de un plan de viabilidad económica, con toma de decisiones económicas exclusivamente fundamentadas en el corto plazo.
En estas circunstancias parece claro que es urgente la necesidad de desarrollar un verdadero plan estratégico que defina las carencias de la situación actual y analice el posible escenario futuro de forma que se establezcan en líneas generales las líneas estratégicas y las necesidades de cambio en la estructura de la organización, siendo a la vez respetuoso con los fines primarios de la Sociedad y en la medida posible con los estatutos de la misma.
Documentos para la descarga:
![]() Plan Estratégico SEAIC 2011-2018 (9903 descargas )
Plan Estratégico SEAIC 2011-2018 (9903 descargas )
![]() Plan Estratégico de Desarrollo Corporativo de la SEAIC 2013-2018 (3491 descargas )
Plan Estratégico de Desarrollo Corporativo de la SEAIC 2013-2018 (3491 descargas )
![]() Plan Estratégico de la SEAIC para Asociaciones de Pacientes (3596 descargas )
Plan Estratégico de la SEAIC para Asociaciones de Pacientes (3596 descargas )
![]() Plan Estratégico de Comunicación Integral de la SEAIC 2014-2018 (4029 descargas )
Plan Estratégico de Comunicación Integral de la SEAIC 2014-2018 (4029 descargas )
![]() Plan Estratégico de Calidad y Seguridad de la SEAIC 2015-2018 (3835 descargas )
Plan Estratégico de Calidad y Seguridad de la SEAIC 2015-2018 (3835 descargas )
![]() Plan Estratégico de Fomento de la Investigación de la SEAIC 2016-2020 (3503 descargas )
Plan Estratégico de Fomento de la Investigación de la SEAIC 2016-2020 (3503 descargas )
![]() Plan Estratégico de Investigación en Alergología 2017-2021 (3542 descargas )
Plan Estratégico de Investigación en Alergología 2017-2021 (3542 descargas )
Publicado el día 14/11/2016
Formación Continuada Avalada
El Comité de Formación Continuada ofrece a través de esta página las actividades de formación presenciales que cuentan con el aval de la SEAIC (más información moviendo el cursor sobre la tabla para acceder a los enlaces):
PROXIMAMENTE INCORPORAREMOS NUEVOS CURSOS AVALADOS…
Actualizado el día 14/08/2017