resultados de la búsqueda: cme-jiaci/profesionales/aviso-importante/wp-content/uploads/logos/Hospital Universitario Fundación Jiménez Díaz
Concurso Historias de Asma
La Fundación de la SEAIC lanza un concurso enfocado a los pacientes que sufren asma grave.
El objetivo del concurso es premiar a los participantes que muestren de forma creativa su «día a día con asma”.
Se valorará especialmente la positividad y espíritu de superación frente a su enfermedad.
Los interesados pueden mandarnos su trabajo en formato vídeo, relato o gráfico (foto o dibujo) antes del 17 de junio de 2022.
Ayuda a campamentos 2012
La Fundación de la SEAIC convoca una ayuda de asistencia para los campamentos de niños alérgicos y asmáticos.
Premio al Mejor Expediente MIR 2025
¡Nuevo Lanzamiento! Plazo: 31 de julio de 2025.
Si eres socio de la SEAIC y terminas tu residencia en Alergología en julio de 2025, ¡participa!
La Fundación de la SEAIC convoca el Premio al Mejor Expediente MIR 2025, con el patrocinio de API (Asac Pharmaceutical Immunology), con el objetivo de reconocer la excelencia académica, profesional e investigadora de los médicos residentes en la especialidad de Alergología.
-
Premio: 5.000 €.
- Para participar deberás presentar un Informe de Méritos debidamente justificado y certificado por tu tutor y jefe de servicio.
- Descarga las bases para conocer todos los detalles
![]() Instrucciones Premio Mejor Expediente MIR 2025 (1169 descargas )
Instrucciones Premio Mejor Expediente MIR 2025 (1169 descargas )
![]() Convocatoria Premio Mejor Expediente MIR 2025 (1285 descargas )
Convocatoria Premio Mejor Expediente MIR 2025 (1285 descargas )
Historia clínica
Genesis
Descripción general: Genesis es una herramienta de inteligencia artificial que asiste a los médicos capturando en tiempo real la conversación entre el médico y el paciente, generando automáticamente la historia clínica de manera estructurada y precisa.
Ventajas destacadas:
- Captura y transcribe conversaciones en tiempo real, reduciendo la carga administrativa del médico.
- Compatible con cualquier sistema de historia clínica electrónica, permitiendo una integración sencilla.
- Permite finalizar y personalizar la documentación mediante comandos de voz, agilizando el flujo de trabajo.
- Mejora la precisión y uniformidad en la documentación médica.
Desventajas:
- Requiere una conexión a internet estable para su funcionamiento en tiempo real.
- Puede tener limitaciones con acentos o jerga médica específica que no esté en su base de datos.
- La implementación inicial podría requerir capacitación para su uso óptimo.
Modelo de acceso: Genesis ofrece planes basados en suscripción dirigidos a clínicas y profesionales de la salud interesados en optimizar la redacción de historias clínicas.
URL de acceso: https://genesismedical.ai.
Nabla Copilot
Descripción general: Nabla Copilot es una herramienta de inteligencia artificial basada en modelos generativos, como GPT-4, que asiste a los médicos en la redacción de informes y notas clínicas durante las consultas, optimizando el tiempo de documentación.
Ventajas destacadas:
- Transcribe automáticamente notas dictadas por el médico, estructurándolas de forma coherente y profesional.
- Reduce la carga administrativa, permitiendo a los médicos centrarse en la atención al paciente.
- Genera informes claros y precisos que pueden integrarse fácilmente en sistemas de historia clínica electrónicos.
- Ofrece soporte multilingüe, ampliando su utilidad en entornos internacionales.
Desventajas:
- La precisión puede depender de la claridad del dictado y del vocabulario utilizado por el médico.
- Algunas funcionalidades avanzadas pueden estar limitadas a versiones de pago.
- Requiere una conexión a internet estable para procesar datos en tiempo real.
Modelo de acceso: Ofrece una versión básica gratuita y planes de suscripción con funcionalidades avanzadas, orientados a clínicas y profesionales individuales.
URL de acceso: https://www.nabla.com/copilot.
DriCloudAI
Descripción general: DriCloudAI es un sistema avanzado de inteligencia artificial integrado en el software médico DriCloud, diseñado para asistir a los profesionales de la salud en la gestión de historias clínicas, proporcionando sugerencias en tiempo real sobre diagnósticos, tratamientos y medicaciones.
Ventajas destacadas:
- Analiza datos del paciente para sugerir diagnósticos probables, tratamientos adecuados y medicaciones con nombres comerciales y dosis específicas.
- Alerta sobre posibles interacciones medicamentosas y considera los antecedentes personales del paciente.
- Recomienda tratamientos específicos, ejercicios y procedimientos quirúrgicos detallados.
- Permite agregar información directamente en los campos de la historia clínica, ahorrando tiempo y reduciendo errores de escritura.
Desventajas:
- Aunque es preciso, siempre requiere la supervisión del profesional de la salud; no reemplaza el juicio clínico.
- La eficacia depende de la calidad y precisión de los datos ingresados en el sistema.
- Puede requerir una curva de aprendizaje para su uso óptimo por parte del personal médico.
Modelo de acceso: DriCloudAI está integrado en el software médico DriCloud, que ofrece planes de suscripción adaptados a las necesidades de clínicas y profesionales de la salud.
URL de acceso: https://dricloud.com/inteligencia-artificial-medicina-clinica.
Noa Notes
Descripción general: Noa Notes es una herramienta de inteligencia artificial desarrollada por Doctoralia que genera notas médicas automatizadas durante las consultas, permitiendo a los profesionales de la salud centrarse en la atención al paciente sin preocuparse por la documentación.
Ventajas destacadas:
- Opera en segundo plano, analizando y resumiendo en tiempo real todo lo que ocurre en la consulta a nivel médico: síntomas, observaciones, plan de tratamiento, medicación, etc.
- Ahorra hasta un 30% del tiempo de la consulta, permitiendo una mayor atención y empatía con el paciente.
- Genera documentación detallada y personalizada, adaptándose al estilo del profesional.
- Funciona con cualquier sistema de historia clínica, facilitando la integración y uso.
Desventajas:
- Requiere el consentimiento del paciente para grabar la consulta, lo que puede implicar pasos adicionales en el proceso.
- La precisión de las notas generadas depende de la claridad de la conversación y del entorno de la consulta.
- Puede necesitar ajustes iniciales para adaptarse completamente al estilo y preferencias del profesional.
Modelo de acceso: Noa Notes ofrece planes de suscripción adaptados a las necesidades de los profesionales de la salud, con opciones de prueba gratuita para evaluar sus funcionalidades.
URL de acceso: https://noa.ai/es-es.
MedKnowts
Descripción general: MedKnowts es una herramienta de inteligencia artificial diseñada para mejorar la eficiencia de los registros médicos electrónicos (EHR), integrando la documentación clínica con la recuperación de información relevante del paciente en una interfaz unificada.
Ventajas destacadas:
- Proporciona autocompletado de términos médicos y estructuración automática de datos clínicos, agilizando la redacción de notas.
- Presenta información relevante del historial del paciente, como resultados de pruebas de laboratorio y notas anteriores, en el momento necesario.
- Permite el registro automático de secciones de la nota clínica, reduciendo la redundancia y el tiempo dedicado a la documentación.
- Genera notas más claras que pueden traducirse a un lenguaje más comprensible para el paciente.
Desventajas:
- Al ser una herramienta en desarrollo, puede requerir ajustes para adaptarse a diferentes entornos clínicos y flujos de trabajo.
- La implementación puede implicar integración con sistemas EHR existentes, lo que podría presentar desafíos técnicos.
- La adopción por parte del personal médico puede requerir capacitación y adaptación a nuevas formas de documentación.
Modelo de acceso: Actualmente, MedKnowts está en fase de desarrollo y pruebas, con acceso limitado a instituciones colaboradoras. o se ha especificado un modelo de suscripción o disponibilidad comercial general.
URL de acceso: https://clinicalml.org/projects/medknowts.
Llamalítica
Descripción general: Llamalítica es una plataforma de inteligencia artificial generativa diseñada para asistir a los profesionales de la salud en la documentación clínica, transcribiendo y estructurando automáticamente las consultas médicas para mejorar la eficiencia y precisión en la atención al paciente.
Ventajas destacadas:
- Transcripción en tiempo real: Captura y transcribe las conversaciones entre el médico y el paciente durante la consulta, generando informes clínicos detallados sin necesidad de intervención manual.
- Estructuración automática: Organiza la información en secciones como motivo de consulta, examen clínico, diagnóstico y plan de tratamiento, facilitando la revisión y seguimiento del paciente.
- Integración flexible: Compatible con diversos sistemas de registros clínicos electrónicos, permitiendo una implementación sencilla en diferentes entornos sanitarios.
- Reducción de carga administrativa: Al automatizar la documentación, permite a los médicos dedicar más tiempo a la atención directa del paciente, mejorando la calidad del servicio y la satisfacción del paciente.
Desventajas:
- Dependencia tecnológica: Requiere una infraestructura tecnológica adecuada y una conexión a internet estable para su funcionamiento óptimo.
- Curva de aprendizaje: Los profesionales de la salud pueden necesitar tiempo para adaptarse al uso de la herramienta y confiar plenamente en sus capacidades.
- Consideraciones de privacidad: Es esencial garantizar la confidencialidad y seguridad de los datos del paciente, lo que implica cumplir con regulaciones estrictas y mantener actualizadas las medidas de protección de datos.
Modelo de acceso: Llamalítica ofrece sus servicios a través de modelos de suscripción dirigidos a profesionales de la salud, clínicas y hospitales. Los detalles específicos sobre precios y planes de suscripción no se encuentran disponibles públicamente y pueden variar según las necesidades de la institución.
URL de acceso: https://llamalitica.com.
Dificultades diagnóstica en alergia a picadura de himenópteros
El diagnóstico de alergia a veneno de himenópteros consiste en identificar el veneno (o los venenos) responsable de causar reacción alérgica tras una picadura. Para este fin se cuentan con diversas técnicas diagnósticas como lo son las pruebas cutáneas, la determinación de IgE especifica, además de la información que proporciona el paciente sobre el insecto sospechoso.
Pero en ocasiones llegar a descubrir cual es el veneno responsable no es tan sencillo. Esto puede deberse a que: (1) el paciente no puede identificar el insecto que le ha picado, (2) las técnicas diagnósticas (pruebas cutáneas o la determinación de IgE especifica) son negativas, (3) presencia de resultados positivos a varios venenos y (4) discordancia entre el resultado de las pruebas cutáneas y los valores de IgE específica.
Para abordar estas dificultades es recomendable:
(1) Ampliar la historia clínica. Se debe de preguntar por la presencia de aguijón tras la picadura. Cuestionar si había alimentos cerca. Interrogar sobre el lugar donde sufrió la picadura (cerca de ríos, pantanos, lagos o piscinas). Recabar información sobre la presencia de colmenas próximas. Indagar sobre la visualización de nidos (terrestres o aéreos). Investigar sobre la profesión o “hobbies”. Es también muy importante conocer la región geográfica donde presentó la picadura.
(2) Optimizar las técnicas diagnósticas. Reducir el punto de cohorte de la IgE específica a 0,10 kU/L. Repetir las pruebas cutáneas o la determinación de IgE especifica pasados 1 a 2 meses. Ampliar el estudio a todos los venenos disponibles. Emplear otras técnicas diagnósticas más complejas.
(3) Diferenciar reactividad cruzada de doble sensibilización. Cuantificar alergenos especie específicos y alérgenos de reactividad cruzada. Establecer la ratio de antígeno 5 (en caso de resultados positivos para polistes y vespula). Identificar la presencia de CCD’s (en caso de resultados positivos para apis y vespula).
(4) Repetir estudio alergológico. Volver a realizar las pruebas cutáneas y determinación de IgE especifica. Valorar utilizar otro extracto diagnóstico al repetir las pruebas cutáneas. Aplicar plataformas multiplex.
Si tras haber completado todas las recomendaciones anteriores la identificación del veneno no es posible se puede intentar enviar suero del paciente a centros especializados que cuenten con la infraestructura y la experiencia para realizar técnicas diagnósticas más complejas (Test de activación de basófilos, Immunoblot o CAP-inhibición).
Lamentablemente enviar suero o derivar pacientes a otros centros no siempre es posible. A pesar de no poder establecer con una precisión del 100% el veneno (o los venenos) responsable de la reacción, el paciente subsidiario de beneficiarse de inmunoterapia específica para venenos debe recibirla. Si la reacción que presenta pone en riesgo su vida (anafilaxia) o implica un deterioro importante en su calidad de vida se le debe de administrar inmunoterapia específica contra todos los venenos identificados como probables responsables de la reacción.
Actualmente existen protocolos y guías clínicas que explican la forma en la que se debe de iniciar una doble inmunoterapia para veneno de himenópteros en aquellos pacientes que lo requieran. La administración de doble inmunoterapia es segura y confiere una buena protección en caso nuevas picaduras.
Federico de la Roca Pinzón
Médico Especialista en Alergología.
Miembro del comité de alergia a himenópteros.
¿Cómo saber si soy alérgico a las picaduras de abejas y avispas?
La alergia al veneno de himenópteros (abejas, avispas, etc.) no es una enfermedad genética o de nacimiento, sino que se puede desarrollar a lo largo de la vida tras haber sufrido picaduras de estos insectos y haberse sensibilizado a ellos. El estudio alergológico está indicado en pacientes que, o bien han sufrido una reacción generalizada con alguna de estas picadura, o que presentan reacciones locales extensas y tienen una alta exposición o mala calidad de vida, con el objetivo de demostrar la presencia de sensibilización específica mediada por IgE frente al veneno del insecto responsable y valorar si son candidatos a recibir una inmunoterapia con alérgenos (vacuna). Por lo tanto, no está indicado el estudio predictivo ni preventivo en pacientes con miedo a las reacciones o con antecedentes familiares de esta alergia.
Para realizar un diagnóstico correcto, se disponen de una serie de procedimientos que explicamos a continuación:
Historia clínica
Es la herramienta fundamental. Los síntomas presentados con la picadura permiten conocer el tipo de reacción sufrida. Es decir, si se trató de una reacción local normal, local extensa, sistémica o incluso si pueden existir otras enfermedades asociadas como los síndromes de activación mastocitaria. Debe recogerse el número y la zona de las picaduras recibidas, el intervalo de tiempo entre la picadura y el inicio de los síntomas y el tratamiento que se administró en ese momento. Otro aspecto muy importante es la identificación del insecto picador. En algunas ocasiones puede parecer más evidente, aunque en otras es posible que sea ambiguo o realmente difícil. El entorno en el que se produce la picadura puede ayudar a ello, sobre todo con respecto al lugar donde sucedió, época del año, comportamiento del insecto, alimentos cercanos, persistencia del aguijón tras la picadura o presencia cercana de nidos o de colmenas. Es posible que esta información pueda sugerir el género del himenóptero, si se trataba de una avispa (Vespula, Dolichovespula, Vespa, Polistes), una abeja (Apis) o un abejorro (Bombus), entre los más habituales. Incluso, en el caso de que se pudiera haber recogido el insecto que picó, se podría aportar el ejemplar en la consulta.
El cuestionario de calidad de vida (HiCaVi), validado por nuestro comité de la SEAIC, permite evaluar este aspecto en este grupo de pacientes y apoyar la indicación de tratamiento con inmunoterapia en algunos casos.
Pruebas cutáneas
Se realizan de dos tipos: Intraepidérmicas o skin prick test, que son similares a las que se hacen en el estudio de pólenes y de otros alérgenos respiratorios ; e intradérmicas, a concentraciones crecientes seriadas. Su positividad es suficiente para demostrar sensibilización.
Pruebas de laboratorio
Mediante una analítica de sangre se pueden medir las IgE específicas frente a venenos completos, que son los anticuerpos que una persona puede generar después de recibir picaduras. Se consideran positivas a partir de 0,1 kUA/L.
El conocido como diagnóstico molecular permite detectar anticuerpos frente a alérgenos concretos para conocer la clase de proteínas que han podido causar la alergia. Es útil en el caso de que varios venenos sean positivos, con el fin de poder diferenciar entre si estamos sensibilizados de forma primaria a uno solo, a varios a la vez (cosensibilización) o si es por el fenómeno de reactividad cruzada (que es la positividad de varios pero por la composición parecida entre ellos).
El uso de otras técnicas de laboratorio más complejas como el CAP-Inhibición o el test de activación de basófilos (TAB) permiten aumentar la precisión y poder llegar a un diagnóstico definitivo.
Además, en todo paciente que haya sufrido una anafilaxia debe solicitarse una triptasa basal, que es una proteasa que puede estar elevada en algunas patologías del sistema inmunitario.
La prueba de exposición mediante repicadura controlada con el propio insecto no está indicada como método diagnóstico por motivos éticos, pero sí es un procedimiento utilizado en pacientes que ya están recibiendo una vacuna y que tiene como objetivo comprobar la eficacia de este tratamiento.
En el caso de pacientes con una historia de una reacción sistémica y un estudio temprano negativo, hay que repetir las pruebas aproximadamente 1-2 meses después, ya que existe un periodo de tiempo en el que pueden darse falsos negativos. Sin embargo, en un 15% de los pacientes con una historia sugerente de alergia no se llega a detectar IgE específica frente a venenos. Igualmente, es importante señalar que los resultados de estas pruebas no se correlacionan con la gravedad de la picadura ni con el riesgo de tener una nueva reacción generalizada posterior.
Finalmente y teniendo en cuenta lo anterior, queda de manifiesto la relevancia de ser valorado por un médico alergólogo, quien brindará a sus pacientes el diagnóstico más preciso y los mejores cuidados.
Jesús Macías Iglesias
Médico Especialista en Alergología
Miembro del Comité de Alergia a Himenópteros y Mastocitosis de la SEAIC
Bibliografía: Comité de Alergia a Himenópteros de la SEAIC. Algoritmo básico: Alergia al veneno de los himenópteros. En: Alergia a Himenópteros: Recomendaciones y algoritmos de práctica clínica de la Sociedad Española de Alergología e Inmunología Clínica. Actualización. Majadahonda (Madrid): ERGON; 2021. 11-21. ISBN: 978-84-18576-24-9
¿Debo suspender algún tratamiento para poder realizarme el estudio de alergia a medicamentos?
Ésta es una pregunta muy frecuente en las consultas de Alergología previa a la realización del estudio de alergia a medicamentos. Es importante conocer qué medicación podemos mantener el día de la prueba y cuál tendríamos que evitar. Esto es lo que se denomina período de lavado y es fundamental para eliminar el tratamiento en cuestión y que no produzca efectos que pudieran alterar o invalidar el resultado del estudio de medicamentos.
Lo primero es informar al alergólogo sobre el tratamiento que tomamos de forma habitual, la posología, motivo de prescripción y frecuencia de administración.
De forma general, podemos diferenciar entre dos tipos de tratamientos:
1. Medicamentos utilizados para patologías crónicas no alérgicas: entre ellos se incluirían medicamentos para controlar la tensión arterial, el colesterol o los triglicéridos, diabetes, coagulación, antiinflamatorios, protectores gástricos, entre otros. Todos estos medicamentos se deben mantener el día de la prueba con su pauta habitual, excepto los betabloqueantes (atenolol, bisoprolol, carvedilol, etc), que deben suspenderse el mismo día previo a la prueba, ya que pueden interferir en la respuesta de tratamientos específicos, como la adrenalina, necesarios en caso de reacción durante el estudio de alergia a medicamentos.
2. Medicamentos utilizados para patologías alérgicas: entre ellos se incluirían medicamentos como los inhaladores, antihistamínicos, corticoides orales, colirios antihistamínicos, sprays nasales, etc. En líneas generales, tanto los antihistamínicos como los corticoides sí necesitarán un período de lavado (no tomarlos) para no interferir en los resultados. Generalmente, se recomienda suspender los antihistamínicos orales o los corticoides orales o intramusculares de 5 a 7 días antes del estudio de alergia para evitar que falseen los resultados, aunque para algunos antihistamínicos de primera generación el plazo puede ser de hasta 10 días. Sin embargo, en la mayoría de los casos se recomienda un mínimo de 5 días, y siempre se debe seguir la pauta específica indicada por el alergólogo, ya que el tiempo puede variar según el tipo de antihistamínico o corticoide. En relación con sprays nasales o inhaladores, generalmente, no es necesario suspenderlos antes de realizar una prueba de alergia a medicamentos.
En resumen, es muy importante informar al alergólogo de toda la medicación que tomamos habitualmente, incluyendo pautas y dosis, de cara a obtener un resultado correcto en las pruebas de alergia a medicamentos, reduciendo, además, los riesgos para el paciente.
Ignacio García Núñez
Especialista en Alergología
Hospitales Quironsalud Córdoba y Quironsalud Campo de Gibraltar
La alergia a veneno de himenópteros, ¿se cura?
Se estima que entre el 56-94 % de la población general padecerá una picadura de himenóptero (abejas y avispas). Según algunos estudios epidemiológicos, en Europa entre el 0,3 y el 7,5 % de la población adulta, y el 3,4 % de los niños, puede padecer una reacción alérgica generalizada tras la picadura de un avispa o abeja, y entre el 2,4-26,4% podrían presentar reacciones alérgicas locales. La población rural presenta un riesgo superior por el hecho de estar más expuesta a las picaduras de estos insectos.
El tratamiento principal para las personas alérgicas es la inmunoterapia (IT) con veneno de himenóptero, también conocida como “vacuna para la alergia”. La IT consiste en administrar de forma subcutánea pequeñas cantidades del alérgeno de forma gradual (fase de inicio y de mantenimiento) para que el sistema inmunológico se “acostumbre” y reduzca su reacción.
La eficacia de la inmunoterapia específica, o vacunación con extractos de veneno de himenópteros, está ampliamente demostrada. La IT a veneno de himenópteros es muy efectiva para reducir los síntomas alérgicos y mejorar la calidad de vida de las personas sensibilizadas alérgicas a estos insectos. Actualmente es el único tratamiento capaz de prevenir futuras reacciones sistémicas, y está indicada en niños y adultos que hayan padecido alguna reacción generalizada moderada o grave, con síntomas cutáneos y respiratorios o cardiovasculares, y siempre que se demuestre un mecanismo dependiente de la Inmunoglobulina E (IgE). La IT también se puede considerar en adultos con solo síntomas cutáneos, pero con alto riesgo de exposición y/o empeoramiento de su calidad de vida. La duración convencional del tratamiento es de 3 a 5 años. La eficacia de la inmunoterapia varía de persona a persona, pero en general se ha demostrado que es altamente efectiva hasta en un 97% de los casos, consiguiendo la reducción de los síntomas y prevención de reacciones graves. El efecto terapéutico es duradero, de modo que incluso 10 años después de la finalización de la IT alrededor del 90 % de los pacientes sigue estando protegido.
Es importante tener en cuenta que la IT es un tratamiento a largo plazo que requiere un compromiso y seguimiento adecuados. Debe ser administrada bajo la supervisión de alergólogos en una unidad de inmunoterapia y se realiza en etapas, comenzando con dosis bajas e incrementándolas gradualmente hasta llegar al mantenimiento (dosis fija mensual o cada dos meses). Además, es fundamental seguir tomando precauciones para evitar picaduras, como usar ropa protectora y evitar áreas donde suelen encontrarse estos insectos. Sin embargo lo más importante es portar un kit de emergencia con adrenalina auto inyectable hasta que se alcance el mantenimiento con la vacuna.
Javier Pereira
Médico Especialista en Alergología
Miembro del Comité de Alergia a Himenópteros y Mastocitosis de la SEAIC
Administración de inmunoterapia subcutánea: mucho mas que una inyección subcutánea: La Enfermera de Alergología te lo explica.
Cuantas veces nos han preguntado “¿Eres la enfermera/o de alergia? ¿La que pone las vacunas no?”.
 Pues bien, es el momento de afirmar, que la administración de inmunoterapia (IT) subcutánea no solo consiste en el procedimiento de administración del alérgeno en dosis crecientes al paciente por vía subcutánea, sino que es un proceso donde se realiza previamente una valoración integral del paciente.
Pues bien, es el momento de afirmar, que la administración de inmunoterapia (IT) subcutánea no solo consiste en el procedimiento de administración del alérgeno en dosis crecientes al paciente por vía subcutánea, sino que es un proceso donde se realiza previamente una valoración integral del paciente.
El paciente acude a nuestra consulta con la incertidumbre ante lo desconocido, a pesar de haber recibido información el día de la prescripción del tratamiento por el alergólogo/a, sobre el procedimiento y sus riesgos.
Es importante que nos presentemos, que conozca nuestro nombre, y le indiquemos que somos las enfermeras/os responsables de la administración del tratamiento. Es muy importante que el paciente se encuentre tranquilo.
Así mismo, procederemos a resolver aquellas dudas que pueda tener acerca de la inmunoterapia (IT) específica de alergia, además de informarle que este tratamiento consta de dos fases:
- Fase de Inicio: Donde se irá incrementando de forma periódica la dosis/concentración de la vacuna, comprobando la tolerancia a la misma. En esta fase deberemos preguntar siempre si han tolerado bien la dosis anterior y si han sufrido algún tipo de reacción en su domicilio (reacción tardía).
- Fase de Mantenimiento: Donde se habrá alcanzado la dosis terapéutica que se continuará administrando de forma periódica.
Respecto a la administración del tratamiento, como responsables de su administración, deberemos comprobar siempre: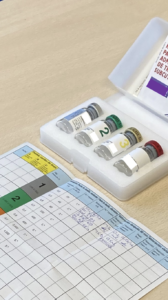
- Que la vacuna que nos entrega el paciente es la que ha prescrito su alergólogo.
- Que corresponde con el nombre del paciente, ya que están identificadas nominalmente.
- La fecha de caducidad.
- Que se ha conservado en nevera (entre 2 y 8 ºC teniendo especial cuidado que no se congele, pues se inactiva y pierde sus propiedades terapéuticas), y trasportada en bolsa térmica .
Procederemos a realizar la valoración de enfermería, recogiendo información sobre su estado de salud:
- Si se encuentra sin síntomas de infección activa (fiebre).
- Si no está presente un episodio agudo (crisis) de su enfermedad alérgica: asma mal controlada o rinoconjuntivitis alérgica.
- Si se encuentra en tratamiento con antibióticos. En cuyo caso se postpondrá la administración hasta su recuperación .
- Si ha recibido en los últimos 7-10 dias vacunas de virus atenuados (gripe, covid…). Como norma general es el intervalo de tiempo mínimo que se recomienda para la administración de la IT específica de alergia.
A continuación procederemos a la toma de constantes vitales (tensión arterial, frecuencia cardiaca, saturación de oxígeno y temperatura) y a la administración del tratamiento de IT específica de alergia siguiendo el protocolo establecido.
Los pacientes deben saber:
- Que tras la administración de su vacuna deben estar un tiempo mínimo de 30 minutos en nuestro servicio de alergia (o Centro de Salud), con el fin de comprobar que ha tolerado bien su IT, y que no han aparecido reacciones adversas inmediatas (por su seguridad).
- Que las reacciones adversas más frecuentes que pueden aparecer son: Enrojecimiento y picor (prurito) en la zona de administración.
- La presencia de síntomas como tos, falta de aire (disnea), aparición de eritemas (zonas enrojecidas en la piel), picor en palma de manos o síntomas exacerbados de su alergia deben ser comunicados inmediatamente para actuar de manera precoz.
- Que la IT especifica de alergia NO sustituye al tratamiento pautado por su alergólogo/a en referencia a antihistamínicos, colirios, inhaladores o nebulizadores nasales. Es un tratamiento conjunto.
- Que no deben practicar ejercicio físico intenso, coger peso, ir a saunas/piscinas cubiertas (ambientes húmedos y cargados) al menos en las 4 primeras horas de la administración de ITSC.
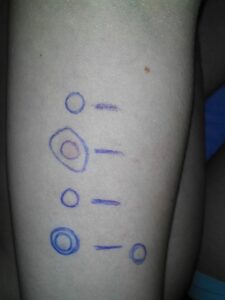
- Que deben informar de la aparición de reacciones tardías (en su domicilio): Aumento de eritema en zona de administración (recomendaremos que se realicen fotos), o cualquier otro síntoma que hayan podido experimentar.
- Que los beneficios de la IT específica de alergia se consiguen a medio/largo plazo y por ello, es necesario que los pacientes acudan a las revisiones programadas por sus alergólogos/as, para valorar la evolución con del tratamiento y si es oportuno continuar con el tratamiento o suspenderlo.
Acta Reunión Comité Alergia Cutánea SEAIC 18/Octubre/2012, Pamplona
![]() Contenido disponible sólo para socios.
Contenido disponible sólo para socios.
¿Debe suspenderse el tratamiento antiasmático durante el embarazo y la lactancia?
En general, se recomienda evitar el empleo de fármacos durante el embarazo, dado el riesgo de malformaciones. Sin embargo, en una mujer asmática embarazada es muy importante obtener un adecuado control de la enfermedad, ya que una crisis puede ser causa de un importante sufrimiento del feto por falta de oxígeno. Si para alcanzar este control es necesario el uso de medicación, no debe suspenderse ni demorarse su administración.
“BLOG” DEL COMITÉ DE INMUNOLOGIA CLINICA COMO FORO DE INFORMACION Y DISCUSION DE TEMAS DE ACTUALIDAD. MARZO 2012
ACTUALIZACIONES BASICAS EN PATOLOGIA ALERGICA
En este blog sobre “Actualizaciones básicas en la patología alérgica” queremos comentar un articulo publicado hace aproximadamente un año en el J Allergy Clin Immunol que nos parece relevante no solo por su contenido básico sino también por su diseño y elaboracion. La hipótesis de trabajo consiste en la posibilidad de que los niños alérgicos pueden tener alterada su capacidad de respuesta inmunológica “natural” frente a determinados componentes bacterianos, lo que daría lugar a una desviación en la maduración del sistema inmunológico, que impide el viraje de la respuestas neonatales con predominio Th2 hacia el predominio de las respuestas Th1 de la edad adulta.
El trabajo en cuestión ha sido realizado en Perth por la Prof. Meri Tulic ![]() , University of Western Australia, en la School of Paediatrics and Child Health (SPACH) y dirigido por la Prof. Susan L. Prescott
, University of Western Australia, en la School of Paediatrics and Child Health (SPACH) y dirigido por la Prof. Susan L. Prescott ![]() , destacada alergóloga con excelentes publicaciones en el campo de la alergia básica y clínica, formada en la escuela del Prof. Patrik Holt, en la misma Universidad de Perth.
, destacada alergóloga con excelentes publicaciones en el campo de la alergia básica y clínica, formada en la escuela del Prof. Patrik Holt, en la misma Universidad de Perth.
La investigación se realizó en colaboración con diferentes Centros y Universidades de Suecia y Reino Unido: Tulic MK, Hodder M, Forsberg A, McCarthy S, Richman T, D’Vaz N, van den Biggelaar AH, Thornton CA, Prescott SL. Differences in innate immune function between allergic and nonallergic children: new insights into immune ontogeny. J Allergy Clin Immunol. 2011 Feb;127(2):470-478.
El reconocimiento bacteriano por el sistema inmune “natural” o innato depende del buen funcionamiento de los receptores Toll que existen en determinadas células del sistema linfo monocitario (Fagocitos mononucleares, linfocitos B, células dendríticas, mastocitos y otras). Estos receptores, alertan al sistema inmune sobre la presencia de los microbios, que detectan reconociendo los antígenos microbianos. El reconocimiento por los receptores Toll y la correspondiente activación celular pone en marcha la defensa primaria o “natural” y en definitiva, representa la primera barrera de los organismos frente a la invasión bacteriana.
El trabajo de Meri Tulic es un estudio caso-control en el que se analiza la respuesta de la inmunidad “natural” o “innata” frente a diferentes productos microbianos que son ligandos de los receptores Toll, como el lipopolisacarido bacteriano o LPS de E. coli o componentes de las membranas bacterianas como el acido lipoteicoico o las partículas de zimosan o bien oligonucleótidos CpG´s no metilados y otros mas, de forma, que cada uno de esos ligandos es especifico para un tipo concreto del repertorio de los receptores Toll, y una vez reconocido el ligando por su correspondiente receptor, se transmite la señal para la activación de la célula correspondiente y la liberación de las citocinas proinflamatorias.
El análisis de activación celular se realizo en 35 niños alérgicos seguidos desde el nacimiento hasta la edad de 5 años, frente a otros 35 controles sanos, en similares circunstancias. Se han estudiado las dos vertientes de la respuesta inmune la “natural” o innata y la “adquirida” o “adaptativa” Para la primera, se estimularon las células mononucleadas de los pacientes con los ligandos citados anteriormente, específicos de los receptores Toll (TLR 2, 3, 4, 2-6, 7/8, y 9) y para la segunda se utilizó la estimulación celular in vitro con antígenos o alérgenos específicos como ácaros y albumina de huevo (OA). Lógicamente, la respuesta que se mide en cada caso es diferente.
En el primero o inmunidad “natural” se mide la síntesis in vitro de citocinas dependientes de TLR´s como la IL-1 beta, IL-6 y el TNF alfa. Por el contrario, para analizar el funcionamiento de la inmunidad “adquirida” o adaptativa, se mide la síntesis de IFN gamma y de IL-13, por las células mononucleares después de la estimulación antígeno específica y mitógenos. En la valoración de las respuestas no solo se analizaron las citocinas solubles sino además se realizó citometria de flujo para cotejar la correspondiente activación celular como consecuencia de la estimulación de los receptores TOLL en las células mononucleares.
Los resultados indican que los niños sanos tienen al nacer una débil respuesta “innata” o “natural”, con escasa producción de IL-1 beta y otras citocinas de la inmunidad “natural”. Con el paso del tiempo, esa respuesta “natural” madura, asemejándose a la de los adultos sanos, además, paralelamente y como consecuencia de esa buena maduración de la respuesta “natural”, la otra respuesta llamada “adquirida” o adaptativa vira hacia un predomino Th1 que es la que prevalece en los sujetos normales adultos. La respuesta normal “adquirida” inducida por alérgenos a los cinco años, será pues de tipo Th1 con predominio de la producción in vitro de interferón gamma. Por el contrario, los niños alérgicos tienen una respuesta “innata” o natural exagerada, ya desde el nacimiento, que es similar o mayor que la de los adultos, pero a lo largo de los primeros años, hay un empobrecimiento de esa respuesta a los ligandos de los TLR ´s, siendo considerablemente menor que la obtenida en los controles sanos a los cinco años. Hay por tanto, en los alérgicos, una respuesta “natural” inicial exageradamente alterada, para deprimirse y deteriorarse a lo largo del desarrollo hacia los cinco años. Se produce una parada en la maduración de la respuesta “adquirida” anti alérgenos , y por tanto, no hay viraje del entorno Th2 de la época prenatal a Th1 como ocurre en los sanos.
Hay unas bases celulares para explicar el que una maduración alterada de la inmunidad “natural” antimicrobiana puede producir una mala respuesta “adquirida” frente a los alérgenos, especialmente, en niños genéticamente predispuestos a las enfermedades alérgicas. Además no solo las células T reguladoras están afectadas sino que en los niños alérgicos hay una mayor expresión de receptores Toll en las células dendríticas plasmocitoides con un incremento en la síntesis de IL-6 y con el consiguiente deterioro en la maduración de las T reguladoras: Dominitzki S, Fantini MC, Neufert C, Nikolaev A, Galle PR, Scheller J, Monteleone G, Rose-John S, Neurath MF, Becker C Cutting edge: trans-signaling via the soluble IL-6R abrogates the induction of FoxP3 in naive CD4+CD25 T cells. J Immunol. 2007 Aug 15;179(4):2041-5.
La modulación de la respuesta alérgica relacionada con la interacción con los agentes microbianos no se limita a la maduración del sistema inmune que condiciona la tendencia a la génesis de la enfermedad alérgica, sino también, es importante por su papel en la rama efectora de la respuesta inflamatoria, previniendo la inflamación eosinofilica que ocurre en el asma bronquial y disminuyendo la hiperreactividad bronquial. Hay un trabajo reciente que utilizando un modelo murino de asma bronquial, demuestra como la infección por H pylori previene la inflamación asmática por inducción de linfocitos T reguladores: Arnold IC, Dehzad N, Reuter S, Martin H, Becher B, Taube C, Müller A. Helicobacter pylori infection prevents allergic asthma in mouse models through the induction of regulatory T cells. J Clin Invest. 2011 Aug;121(8):3088-93. Los efectos beneficiosos (tolerancia inmunológica) sobre la prevención del asma bronquial se manifiestan con mayor intensidad cuando los ratones son infectados con H pylori en el periodo neonatal. El trabajo es un análisis exhaustivo y muy demostrativo desde el punto de vista de la inflamación asmática y su prevención por la infección no solo a nivel histológico sino también molecular.
Obviamente por estos dos trabajos que comentamos en este blog da la impresión que estamos revisitando la “teoría de la higiene” que como es sabido, sostiene que la exposición temprana a los antígenos microbianos es esencial para la prevención de las enfermedades alérgicas. Esto es así, pero querríamos dejar conciencia de que al ser una enfermedad multifactorial no es este aspecto el único ni el mas importante, que modula la aparición de la enfermedad. (Platts-Mills TA, Erwin E, Heymann P, Woodfolk J. Is the hygiene hypothesis still a viable explanation for the increased prevalence of asthma? Allergy. 2005;60 Suppl 79:25-31.)
En algún momento, tendremos que centrar nuestros esfuerzos en una investigación a fondo sobre el papel de las vacunas bacterianas, que en los años 40-50 tuvieron su preponderancia en la alergia, pero que por influencia de la escuela anglosajona, se dejaron de utilizar, incluso fueron denostadas, posiblemente con razón, por falta de los conocimientos científicos adecuados en aquellos tiempos. Es ahora, con todos estos efectos que se han demostrado de la modulación con los productos bacterianos (LPS?) de la respuesta inmunológica, cuando merecería la pena realizar un esfuerzo para aconsejar o no la utilización de estos productos, revisitando los conocimientos, siempre con bases científicas actualizadas por el conocimiento moderno del sistema inmunológico y su modulación por los microbios y sus productos.
LAS INMUNODEFICIENCIAS ASOCIADAS A AGENTES BIOLÓGICOS INMUNOMODULADORES COMO FENOCOPIAS DE LAS INMUNODEFICIENCIAS PRIMARIAS
http://www.thehistoryblog.com/archives/14881
En nuestro sistema sanitario, las consultas de Inmunología atienden principalmente pacientes con una respuesta inmunitaria deficiente. Las inmunodeficiencias primarias (IDP) asociadas a errores innatos de la inmunidad son una causa importante de estas consultas, pero no la única. En la práctica clínica, en la mayoría de los casos, habrá que buscar una causa secundaria de la misma.
Las inmunodeficiencias primarias se incluyen bajo el concepto más global de errores innatos de la inmunidad (EII), que representa un grupo de más de 485 enfermedades definidas genéticamente (1). La inmunodeficiencia secundaria (IDS) podría definirse como una alteración transitoria o persistente de la función de las células o tejidos del sistema inmunitario, causada por factores extrínsecos al mismo (2). Estos grupos de factores incluyen agentes ambientales, malnutrición, trastornos metabólicos, uso de medicamentos inmunosupresores e inmunomoduladores, infecciones crónicas, neoplasias malignas, traumatismos graves o simplemente el envejecimiento. El enfoque inicial recomendado para la valoración de una IDS sigue las mismas directrices que en el caso de las IDP. Los hallazgos de la historia clínica, en particular los patrones de infecciones, y los hallazgos en la exploración física son esenciales para guiar la evaluación del sistema inmunitario.
Dentro de las causas de IDS, la generalización del uso de agentes biológicos inmunomoduladores para tratar enfermedades autoinmunes, inflamatorias o neoplasias hematológicas en las últimas dos décadas, se ha acompañado de un mayor riesgo de infecciones e inmunodeficiencias secundarias (3); el abordaje de este importante tema en una entrada a un blog es complicado como revisión sistemática, así que optaré por una exposición narrativa.
Examinar qué enfermedades infecciosas acompañan a una determinada inmunodeficiencia primaria ha permitido obtener información valiosa sobre los componentes del sistema inmunológico que son claves en la respuesta frente a microrganismos particulares. Gracias a ello sabemos que los defectos en moléculas críticas en la ontogenia, activación y proliferación de los linfocitos T, como las mutaciones en el gen IL2RG del cromosoma X humano, que codifica la cadena gamma común (γc) del receptor de interleucina-2 (IL-2R), o una inactivación mutación en la quinasa Jak3, que se asocia físicamente con γc, causan una depleción profunda en la función del sistema inmune, que de forma sindrómica se denomina Inmunodeficiencia combinada severa. Los defectos en el desarrollo de las células B, como la mutación en el gen que codifica una proteína tirosina quinasa llamada BTK (tirosina quinasa de Bruton), que transduce la señal a través del receptor de células pre-B, provocan deficiencias en la producción de anticuerpos que causan una incapacidad para eliminar bacterias extracelulares y algunos virus cuya eliminación eficaz requiere anticuerpos específicos.
Es instructivo considerar los defectos inmunológicos en el contexto de los principales tipos de inmunidad afectada, ya que estos pueden conducir a distintos patrones de infección y enfermedad clínica.
Las terapias biológicas no causan La inmunosupresión global característica de la terapias inmunosupresoras clásicas como los glucocorticoides, azatioprina, metotrexato o ciclosporina (4). Del mismo modo a cómo actúan las mutaciones específicas en cada IDP, las terapias biológicos se dirigen selectivamente a células y vías del sistema inmunitario para lograr efectos terapéuticos específicos, pudiéndose comportar en ciertos casos como fenocopias de la IDP original.
Por ejemplo, el OKT3 (muromonab-CD3) es un anticuerpo monoclonal IgG2 murino que se une a la cadena CD3-epsilon del complejo receptor de células T-CD3 y produce una linfopenia rápida y profunda de las células T (4). Como cabría esperar, la inmunosupresión asociada provoca una mayor susceptibilidad a las infecciones, en particular por virus herpes y bacterias. Igualmente, Alemtuzumab (anti-CD52) es un anticuerpo monoclonal humanizado utilizado para la terapia de inducción del trasplante de órganos sólidos, depletor de células T.
Basiliximab es un monoclonal contra la cadena alfa del receptor de la interleucina (IL)-2 (CD25). La activación de las células T conduce normalmente a una regulación al alza del receptor de IL-2 de alta afinidad que implica la expresión de la cadena alfa del receptor de IL-2 (CD25) que se asocia con las cadenas beta y gamma del receptor de IL-2. Basiliximab inhibe la generación de células T citotóxicas antígeno-específicas.
Las células T necesitan dos señales para activarse. La primera implica la unión directa del receptor de antígeno de la célula T (TcR) con el complejo formado por el péptido antigénico y determinadas moléculas de superficie (moléculas HLA), presentado por las células presentadoras de antígeno (APC). La segunda señal implica vías coestimuladoras específicas. El CD28 de las células T se une a sus ligandos, el CD80 (B7-1) y el CD86 (B7-2), en las APC. La presencia de ambas señales proporciona una señal de activación a las células T. Por el contrario, la molécula CTLA-4 en las células T compite por la unión a las mismas moléculas CD80/CD86, y esta interacción provoca la supresión de la activación. Abatacept y Belatacept son proteínas de fusión del dominio extracelular de CTLA-4 humano unido a una porción Fc modificada de IgG1 humana (CTLA-4-Ig), que interfieren la activación de las células T interrumpiendo la coestimulación CD28. Abatacept no obstante tiene un perfil de seguridad bien establecido en diferentes ensayos y metanálisis. Belatacept por su parte, con mayor capacidad de unión a CD80/CD86, no debe administrarse a pacientes con serología de VEB negativa candidatos a trasplante de un donante con serología VEB positiva, por el mayor riesgo de desarrollar trastornos linfoproliferativos asociados a VEB (4).
Las Janus quinasas (JAK) son una familia de tirosina quinasas no receptoras, cruciales en el desencadenamiento de las señales generadas por el receptor de diversas citoquinas y transducidas aguas abajo a través de las proteínas STAT (transductoras de señales y activadoras de la transcripción). Las STAT fosforiladas se disocian de sus subunidades receptoras y se translocan al núcleo celular para regular la transcripción génica. La familia JAK se compone de cuatro miembros: JAK1, JAK2, JAK3 y tirosina quinasa 2 (Tyk2). Tofacitinib, inhibidor JAK aprobado para la artritis reumatoide que actúa principalmente sobre JAK1 y JAK3, se ha asociado con un mayor riesgo de infección por herpes zoster (4).
Con respecto a las células B, Ibrutinib es una pequeña molécula inhibidora de la tirosina quinasa de Bruton (BTK). El ibrutinib se une a la actividad de la BTK y la inhibe de forma irreversible, impidiendo así tanto la activación de las células B como la señalización mediada por éstas. La BTK es necesaria para la señalización del receptor de células B, desempeña un papel clave en la maduración de las células B. Se han descrito casos de neutropenia e hipogammaglobulinemia. Igualmente, Idelalisib interrumpe la señalización del receptor de células B, de forma similar a ibrutinib, aunque a través de la inhibición de la isoforma delta de la fosfatidilinositol 3-cinasa. Idelalisib se asocia a un aumento de las infecciones oportunistas (4). Belimumab por su parte, es un anticuerpo monoclonal humano que se une al BlyS humano soluble e inhibe su actividad biológica. Está aprobado para el tratamiento de pacientes con LES. La celulitis y la neumonía son las infecciones graves más frecuentes (4).
Pero sin duda, la familia de biológicos con más impacto en la casuística de las consultas de inmunodeficiencias son los anti CD20 y en particular, rituximab. Este anticuerpo monoclonal quimérico (Ig)G1 CD20 específico actúa sobre las células B desde la fase pre-célula B hasta la fase pre-célula plasmática. Rituximab agota las células B de la sangre periférica, y su normalización posterior suele requerir de seis a nueve meses o más, con una variabilidad significativa entre pacientes. Con las células B deplecionadas, la capacidad del paciente para responder a las vacunas, en particular de polisacáridos, se ve afectada. Además, es frecuente cierto grado de hipogammaglobulinemia transitoria, que en algunos pacientes es persistente y significativa clínicamente, dando lugar a infecciones que requieren profilaxis antibiótica y/o terapia sustitutiva (4).
Así, hasta un largo etcétera de terapias biológicas que actúan selectivamente sobre la vía de diferentes citoquinas (interleuquina 6, interleuquina 1, factor de necrosis tumoral alfa, interleuquinas 4 y 13, interleuquina 17), integrinas (alfa-4 integrinas, CD11 alfa), o proteínas del complemento, entre otros, bloqueando con una precisión quirúrgica el normal funcionamiento del sistema inmune.
Disponemos de evidencias y de herramientas para tratar de disminuir el riesgo de IDS asociado al uso de medicamentos biológicos. Este riesgo se debe prevenir con profilaxis antibiótica adecuada, y se debe prever mediante una planificación del programa de vacunación adaptada al tipo de defecto en la respuesta inmune descrito para el fármaco.
Igualmente, las recomendaciones en cuanto a vacunación de pacientes en grupos de riesgo, tanto centrales como de las comunidades autónomas, deberían estar actualizadas acorde a la evidencia disponible e integrar la opinión de expertos con conocimiento en el funcionamiento del sistema inmune y en el mecanismo de acción de estos fármacos.
REFERENCIAS
- Tangye SG, Al-Herz W, Bousfiha A, Cunningham-Rundles C, Franco JL, Holland SM, Klein C, Morio T, Oksenhendler E, Picard C, Puel A, Puck J, Seppänen MRJ, Somech R, Su HC, Sullivan KE, Torgerson TR, Meyts I. Human Inborn Errors of Immunity: 2022 Update on the Classification from the International Union of Immunological Societies Expert Committee. J Clin Immunol. 2022 Oct;42(7):1473-1507. doi: 10.1007/s10875-022-01289-3. Epub 2022 Jun 24. PMID: 35748970; PMCID: PMC9244088.
- Tuano KS, Seth N, Chinen J. Secondary immunodeficiencies: An overview. Ann Allergy Asthma Immunol. 2021 Dec;127(6):617-626. doi: 10.1016/j.anai.2021.08.413. Epub 2021 Sep 3. PMID: 34481993.
- Cannon L, Pan A, Kovalick L, Sarkissian A, Wu EY. Secondary immunodeficiencies and infectious considerations of biologic immunomodulatory therapies. Ann Allergy Asthma Immunol. 2023 Jun;130(6):718-726. doi: 10.1016/j.anai.2023.02.010. Epub 2023 Feb 18. PMID: 36801438; PMCID: PMC10247415.
- https://www.uptodate.com/contents/secondary-immunodeficiency-induced-by-biologic-therapies (acceso abril/2024).
¿Cómo reconocer una anafilaxia?
Es muy importante reconocer rápidamente que una persona puede estar presentando una anafilaxia para administrar adrenalina precozmente.
Los síntomas de la anafilaxia suelen aparecer de manera brusca y súbita y afectan simultáneamente o de forma rápidamente sucesiva (en minutos) a diferentes órganos del cuerpo. Algunos de los signos más comunes incluyen:
• Un síntoma precoz y frecuente de la anafilaxia es un picor intenso en palmas, plantas y axilas.
• Suele acompañarse de enrojecimiento de la piel, junto con habones (ronchas) que pueden extenderse rápidamente a todo el cuerpo.
• Otro signo típico es la hinchazón, que puede afectar a los párpados y/o los labios, pero también a la lengua y la garganta, provocando en este último caso dificultad respiratoria y alteraciones en el tono de voz o imposibilidad de hablar.
• Pueden darse síntomas en el aparato digestivo, tales como dolor abdominal, náuseas, vómitos o diarrea.
• Si la anafilaxia afecta a los bronquios habrá también dificultad para respirar, pitidos en el pecho, opresión torácica.
• En los casos más graves, si hay bajada de la presión arterial, el paciente puede sufrir mareos intensos e incluso pérdida de conciencia.
A menudo estos síntomas se dan a los minutos del contacto (ingesta, picadura, administración intravenosa) con un alérgeno conocido o potencial, lo cual facilita el diagnóstico. En otras ocasiones, asumir que una persona está sufriendo una anafilaxia no es tan evidente.
La combinación de síntomas que puede presentar cada persona es variable; por tanto es importante saber que la anafilaxia puede manifestarse de diferentes formas.
Las abejas y las avispas
1. LOS HIMENÓPTEROS ABEJAS Y AVISPAS
Los himenópteros son un grupo de insectos artrópodos, caracterizados por poseer alas membranosas (del griego hymen y ptera, membrana y ala, respectivamente) y una organización social compleja. Dentro de los himenópteros existentes son de interés desde el punto de vista alergológico las familias Apidae (abejas) y Vespidae (avispas), ya que son los que ocasionan la mayoría de reacciones alérgicas en nuestro medio.
En el continente americano las hormigas también son causa frecuente de reacciones alérgicas, especialmente la hormiga roja.
La alergia a veneno de himenópteros es conocida desde antiguo: en las paredes de la tumba del rey egipcio Menes (año 2621 a.C.) puede verse representada su muerte por la picadura de una avispa (Figura 1).
Características morfológicas de los himenópteros
El reconocimiento de las características morfológicas, comportamiento y del hábitat del insecto que ha producido la picadura es importante, ya que puede ayudar en su identificación y por tanto mejorar el diagnóstico. La mayoría de los himenópteros son especies solitarias. Una minoría de especies forman sociedades en las cuales se agrupa un número mayor o menor de individuos los cuales trabajan en común para acumular reservas alimenticias y cuidar de sus larvas. Las construcciones donde lo hacen se llaman nidos.
Son estas especies las que interesan desde el punto de vista alergológico, ya que la formación de estas sociedades hace que el riesgo de picadura aumente al aumentar el número de individuos, y lo que es más importante, al aumentar su agresividad como mecanismo de defensa del nido, ya que los himenópteros pican para defender su comida o sus crías.
¿Es usted alérgico a la proteína de leche de vaca o intolerante a la lactosa?: La pregunta que salva vidas
Y es que la diferencia es ciertamente importante. Tan importante como que una de ellas puede ser potencialmente mortal. ¿Sabrías decir a cuál de las dos nos referimos?
Comencemos por los términos importantes:
- Leche: según la definición de la RAE:
- Líquido blanco que segregan las mamas de las hembras de los mamíferos para alimento de sus crías.
- Leche de algunos animales que se emplea como alimento de las personas.
- Jugo blanco obtenido de algunas plantas, frutos o semillas.
- Es decir, CUIDADO, la leche puede ser de origen ANIMAL (vaca, oveja, cabra, búfala…) o VEGETAL (soja, arroz, avena, almendra, coco…).
- Lactosa: según la definición de la RAE:
- Azúcar (disacárido) que contiene la leche, formado por glucosa y galactosa.
- Presente en leches de mamíferos.
- La lactosa se “destruye” (es decir, se separa en glucosa y galactosa) mediante la acción de una enzima digestiva llamada lactasa.
- Azúcar (disacárido) que contiene la leche, formado por glucosa y galactosa.
- Leche de vaca (composición): agua, proteínas (beta-lactoglobulina, alfa-lactoalbúmina, caseína…), grasas, vitaminas, hidratos de carbono (entre ellos, la lactosa) y minerales.
- Yogures y quesos de origen animal: producto lácteo obtenido al fermentar la leche de animales mediante bacterias que transforman la lactosa en ácido láctico, por tanto, el contenido de lactosa en estos productos es menor. Pero siguen conteniendo lactosa (salvo aquellos específicos sin lactosa) y proteínas de leche de animales.
- Leche/yogures/quesos sin lactosa: leche de animales a los que se ha añadido lactasa de forma artificial (pero siguen conteniendo proteínas de leche).
- Leches/yogures vegetales (composición): NO contienen Contienen proteínas diferentes a las de la leche de animales.
DIFERENCIAS FUNDAMENTALES ENTRE AMBAS (ver cuadro)
 Cargando...
Cargando...
La alergia a las proteínas de la leche de vaca:
- Los pacientes pueden tener reacción con leches de otros mamíferos (vaca, cabra, oveja…).
- Reaccionan con pequeñas cantidades (el 50% con menos de 4.1 ml de leche).
- Pueden detectar trazas (menos de 0.1 ml de leche). Los pacientes altamente sensibilizados pueden reaccionar con mínimas cantidades e incluso con contaminaciones indirectas.
- Toleran leches vegetales (excepto si tienen además de su APLV, alergia a alguna de éstas).
- Las reacciones aparecen generalmente en las 2 primeras horas tras la ingesta.
- Los síntomas pueden ser cutáneos (habones, hinchazón de labios…), respiratorios (congestión nasal, dificultad para respirar…), digestivos (dolor abdominal, vómitos, diarrea…) y/o cardiovasculares (mareo, pérdida de conocimiento…).
- Las reacciones pueden ser potencialmente mortales en el caso de afectar a 2 o más órganos o sistemas (ANAFILAXIA).
- Requieren tratamiento urgente específico (por ejemplo, si la afectación es exclusivamente cutánea puede ser tratada con antihistamínicos y corticoides en caso de edema asociado, si los síntomas son respiratorios habrá que utilizar broncodilatadores de rescate y si estamos ante una anafilaxia, el tratamiento de elección será la adrenalina intramuscular).
La intolerancia a lactosa:
- Los pacientes toleran leche sin lactosa.
- Pueden consumir yogures sin lactosa y quesos con bajo contenido en lactosa (queso curado, parmesano, gruyere, mozzarella…). Pero es recomendable preguntar si pueden consumirlo.
- Pueden toleran leche y derivados lácteos con lactosa si toman previamente comprimidos de lactasa.
- Toleran leches vegetales.
- Suelen tener reacciones de tipo digestivo (dolor abdominal, diarrea, flatulencias…).
La cantidad SÍ importa:
3.2 mg de proteína de leche (unos 0.1 ml de leche de vaca) pueden desencadenar una reacción alérgica en al menos el 5% de los pacientes alérgicos a proteínas de leche de vaca. Al menos el 50% reaccionan con 133 mg de proteína de leche (unos 4.1 ml de leche).
EN RESUMEN: el conocimiento es poder. Y en este caso, el uso correcto del lenguaje es de vital importancia.
Grabémonos la pregunta clave:
¿Es usted alérgico a la proteína de la leche de vaca o intolerante a la lactosa?
- Si la respuesta es SOY ALÉRGICO: CUIDADO, pueden tener reacciones alérgicas potencialmente mortales, incluso con trazas, que requieran tratamiento urgente. Tendremos que evitar cualquier contacto con leche de mamíferos y aquellos productos que puedan contenerla.
- Si la respuesta es SOY INTOLERANTE: podemos dar leche y productos lácteos SIN lactosa. Podemos también preguntar por el grado de tolerancia, es decir, si tolera yogures o quesos.
- Si tenemos DUDAS: es mejor SER PRECAVIDOS y EVITAR cualquier contacto con leche de mamíferos o aquellos productos que puedan contenerlos.
Porque hay preguntas que salvan vidas. Usémoslas.
Dra. Laura Argiz Álvarez. Clínica Universidad de Navarra (Madrid).
Bibliografía:
- Turner PJ, d’Art YM, Duca B, et al. Single-dose oral challenges to validate eliciting doses in children with cow’s milk allergy. Pediatr Allergy Immunol. 2021;32(5):1056-1065. doi:10.1111/pai.13482
- Blom WM, Westerhout J, Baumert JL, et al. Updated full range of Eliciting Dose values for Cow’s milk for use in food allergen risk assessment. Food Chem Toxicol. 2022;168:113381. doi:10.1016/j.fct.2022.113381
¿Debe suspenderse el tratamiento antiasmático durante el embarazo y la lactancia?
En general, se recomienda evitar el empleo de fármacos durante el embarazo, dado el riesgo de malformaciones. Sin embargo, en una mujer asmática embarazada es muy importante obtener un adecuado control de la enfermedad, ya que una crisis puede ser causa de un importante sufrimiento del feto por falta de oxígeno. Si para alcanzar este control es necesario el uso de medicación, no debe suspenderse ni demorarse su administración.
XV Curso de Patología Ocupacional Respiratoria
Estimados socios:
Adjuntamos el programa del próximo XV Curso de patología Ocupacional Respiratoria, que se va a celebrar en el Hospital Universitario Vall d’Hebron de Barcelona los días 7 y 8 de noviembre del presente año.
El curso ha sido considerado de interés sanitario por el Instituto de Estudios de la Salud (IES) y está dirigido a profesionales relacionados con la salud laboral.
![]() XV Curso de Patología Ocupacional Respiratoria (2623 descargas )
XV Curso de Patología Ocupacional Respiratoria (2623 descargas )
XIV Curso de Patología Ocupacional Respiratoria
El Hospital Universitario Vall d’Hebron de Barcelona organiza los días 8 y 9 de noviembre de 2010 el XIV curso de patología ocupacional respiratoria, considerado de interés sanitario por el Instituto de Estudios de la Salud y dirigido a profesionales relacionados con la salud laboral.
Descargar programa: Curso de Patología Ocupacional Respiratoria 2010 (3086 descargas )
Obesidad, dieta y asma infantil.
La obesidad infantil es uno de los problemas de salud pública más graves del siglo XXI. Es un problema a nivel mundial cuya prevalencia está aumentando a un ritmo alarmante. Este incremento de la prevalencia de obesidad en niños y en modo paralelo una incidencia cada vez mayor en los mismos de asma han motivado el planteamiento de que ambos procesos pudieran estar relacionados. Diversos estudios han demostrado un efecto de temporalidad entre estados obesogénicos y el posterior desarrollo de asma y de igual modo un efecto de dosis-respuesta, estableciéndose una relación directa entre el grado de obesidad y la severidad con la que cursa el asma.
El asma relacionado con la obesidad pediátrica causa una gran carga de enfermedad y se asocia con anomalías metabólicas. La mala calidad de la dieta, a su vez, parece estar relacionada con el asma, sin embargo, la asociación entre el estado nutricional y la carga de la enfermedad entre los niños con asma relacionada con la obesidad no se conoce bien.
En el estudio de Tobias et al1 se plantea valorar el estado nutricional, definido como concentraciones de carotenoides séricos y ácidos grasos omega-3, y su asociación con la función pulmonar y los marcadores metabólicos entre los niños asmáticos obesos.
Se cuantificaron los carotenoides y ácidos grasos séricos en una cohorte de estudio de 158 adolescentes de minorías urbanas, incluyendo 39 asmáticos obesos, 39 asmáticos con peso saludable, 38 controles obesos y 42 controles con peso saludable y comparados entre los grupos. Se correlacionaron los niveles de carotenoides y ácidos grasos con los índices de función pulmonar y con la resistencia a la insulina y la dislipidemia.
Como resultados se obtuvieron que la media de carotenoides totales fue más baja en niños asmáticos obesos (0,41 μg/ml) frente a asmáticos con un peso inferior al saludable (0,52 μg/ml, p <0,05) y a los controles de peso saludable (0,60 μg/ml, p <0,001). La proporción de ácidos grasos poliinsaturados omega-6/omega-3 también fue distinta entre los grupos (p <0.05) correlacionándose de forma inversa con el pronosticado en los niños asmáticos obesos.
Los carotenoides totales se correlacionaron positivamente con el porcentaje de FEV1 predicho y se correlacionaron inversamente con la resistencia a la insulina sólo entre los asmáticos obesos.
En definitiva, estos hallazgos sugieren que los carotenoides, que son más bajos en niños asmáticos obesos, pueden tener efectos protectores sobre la salud metabólica y la función pulmonar y de manera similar, los ácidos grasos omega-3 también parecen ser protectores de la función pulmonar.
Sería deseable y necesario poner en marcha estudios que profundizasen y aclarasen los entresijos aún por conocer de la relación existente entre la obesidad y las alteraciones respiratorias como el asma. Desde una temprana edad seria necesario inculcar a los niños una dieta saludable con el fin de prevenir enfermedades crónicas futuras, entre ellas, el asma bronquial. Además, resultará igualmente necesario establecer colaboraciones entre los profesionales de las distintas especialidades (Endocrinología, Cardiología, etc.), todo ello orientado a poner en marcha programas de acción y prevención coordinados.
1.-Tobias TAM, Wood LG, Rastogi D. Carotenoids, fatty acids, and disease burden in obese minority adolescents with asthma. Clin Exp Allergy. 2019 Mar 25.
Margarita Tomás Pérez. Médico Adjunto Alergología Hospital General Universitario La Paz. Madrid. Comité de Alergia Infantil SEAIC.