resultados de la búsqueda: profesionales/aviso-importante/cme-jiaci/inicio/prensa
Nuevos horizontes en la inflamación alérgica para explicar los fenotipos graves de alergia
En las últimas décadas, la prevalencia y la complejidad de las patologías alérgicas han aumentado significativamente. Este incremento se observa no solo en el número de pacientes, sino también en la aparición de casos con perfiles complejos, como los pacientes polisensibilizados, aquellos con remodelado epitelial y quienes muestran una respuesta insuficiente a los tratamientos convencionales. El manejo de estos pacientes representa un desafío para los especialistas en alergología (1).
Entre ellos, un grupo considerable presenta formas graves de alergia. La gravedad no se limita únicamente a aquellos que desarrollan reacciones anafilácticas, que representan un riesgo de vida evidente, sino también a aquellos que experimentan reacciones exacerbadas, como en el caso del asma alérgico grave, caracterizado por su difícil control y alta morbilidad (1). Nuestro grupo de investigación lleva más de una década estudiando los mecanismos subyacentes a estos fenotipos graves de alergia con un doble objetivo: 1) Identificar potenciales dianas terapéuticas para el manejo y control de estos pacientes y 2) la identificación y clasificación de estos pacientes.
Son pacientes que por sus características no responden a la mayoría de los tratamientos disponibles, que no suelen tolerar el tratamiento con AIT, tiene una baja calidad de vida y que, además, al tratarse de pacientes crónicos con muchos años de evolución suponen una importante carga económica para el Sistema Nacional de Salud.
Las características geográficas y climatológicas de nuestro país han permitido el estudio detallado de perfiles graves a lo largo de la geografía española. En Extremadura existe un porcentaje significativo de pacientes con alergia al polen de gramíneas que desarrollan reacciones graves a profilina (2); en Córdoba pacientes con alergia al polen de olivo sensibilizados a alergenos menores como Ole e 7 (3) o en las Islas Canarias, pacientes alérgicos a ácaros que además desarrollan reacciones graves (4) al entrar en contacto con harinas contaminadas con ácaros. Todos estos fenotipos alérgicos comparten características comunes: una respuesta inflamatoria persistente y exacerbada.
La inflamación persistente y no resuelta es un factor subyacente común observado en varias enfermedades humanas aparentemente no relacionadas, incluidas las enfermedades cardiovasculares y neurodegenerativas (5).
Algunos de los mecanismos asociados con la respuesta inflamatoria y que hemos demostrado en pacientes con alergia respiratoria grave son: Metabolismo de Warburg, aumento del metabolismo de los esfingolípidos y lisofosfolipidos, potenciación de las células T efectoras, desregulación de las células T reguladoras y cambios en las características biológicas de las plaquetas (4, 6, 7,8).
Estos hallazgos no solo abren nuevas vías de investigación en el campo de la alergia, facilitando una mejor comprensión de los procesos en estos pacientes, sino que también son relevantes para entender mecanismos subyacentes en otras patologías inflamatorias, como la artritis reumatoide o incluso la esclerosis múltiple, que comparten algunas de estas características inflamatorias. Es por este motivo que en España contamos con la Red de Enfermedades Inflamatorias (REI), financiada por el ISCII, que se dedica a la identificación y traslación de biomarcadores dirigidos a implantar estrategias de medicina personalizada en patologías inflamatorias, incluyendo las alérgicas. Su objetivo es proporcionar nuevas herramientas a los profesional para el tratamiento de estos pacientes y optimizar el uso de recursos de forma efectiva.
- Clin Exp Allergy. 2024 Aug;54(8):550-584. doi: 10.1111/cea.14517.
- J Allergy Clin Immunol. 2019 Feb;143(2):681-690.e1. doi: 10.1016/j.jaci.2018.03.013.
- 2019 Nov;74(11):2261-2265. doi: 10.1111/all.13860
- 2022 Jun;77(6):1772-1785. doi: 10.1111/all.15192
- Nat Rev Immunol . 2021 Nov;21(11):739-751. doi: 10.1038/s41577-021-00538-7
- 2018 Nov;73(11):2137-2149. doi: 10.1111/all.13563.
- 2023 May;78(5):1319-1332. doi: 10.1111/all.15621.
- Int J Mol Sci. 2024 Aug 30;25(17):9425. doi: 10.3390/ijms25179425
Acta – Reunión Webex Comité Alergia Cutánea SEAIC
![]() Contenido disponible sólo para socios.
Contenido disponible sólo para socios.
Votaciones EAACI
Apreciados socios:
Hoy viernes 1 de abril a las 17:00 h acaba el plazo para votar a los candidatos que se presentan a los grupos de interés de la EAACI. Tenemos varios miembros españoles que se presentan a estos grupos y sería importante contar con tu apoyo a las candidaturas españolas. Si eres socio de la EAACI, entra con tus datos de acceso en su página web y vota, si estás de acuerdo, a los alergólogos españoles que os indicamos a continuación: Javier Fernández, Miguel Blanca, Marta Ferrer, Montserrat Fernández-Rivas, Carmen Rondón, Ángel Mazón.
Muchas gracias por tu apoyo.
Un cordial saludo,
Dr. P. Ojeda
Secretario de la Junta Directiva de la Sociedad Española de Alergología e Inmunología Clínica
Me han diagnosticado de alergia a la LTP ¿qué es y qué debo hacer?
LTP simplemente quiere decir “Lipid Transfer Protein”, es decir, proteína de transferencia de lípidos. A continuación, 3 datos claves para entenderla:
1) ¿Qué es? Es una proteína vegetal que cumple múltiples funciones en frutas, verduras, hortalizas y frutos secos, fundamentalmente. Esta proteína se encuentra en mayor concentración en la piel de la fruta que en su pulpa. En el caso de la fruta, si has tolerado su pulpa, seguramente te recomendaran que siempre la tomes pelada.
2) Es muy importante entender que no hay unas recomendaciones generales para todos los pacientes sensibilizados o alérgicos a la proteína LTP. Es decir, cada paciente recibe unas pautas completamente personalizadas. Tu especialista te ha diagnosticado y ha ajustado el tratamiento y las normas de evitación de manera individualizada.
3) La alergia a la LTP puede ser un fenómeno mediado o no por cofactores.
Los cofactores son una serie de agentes (o factores) que unidos a la ingestión de un alimento que contiene LTP hacen que desencadene una reacción alérgica, que no hubiese ocurrido, o hubiese sido menos grave, si no hubiesen estado presentes.
Los cofactores ayudan a que se liberen mediadores de la inflamación a través de la “rotura” o degranulación de las células que intervienen en una reacción alérgica (como los mastocitos o basófilos).
Los más habituales son: el ejercicio físico, la fiebre, las infecciones o la toma de antiinflamatorios no esteroideos (AINE) como, por ejemplo: Ibuprofeno, metamizol, ácido acetilsalicílico, etc. Además, hay otros cofactores que pueden llegar a ser importantes tras la ingestión de alimentos con LTP como son: el estrés intenso, la falta de sueño extrema, la menstruación, la toma de alcohol o el uso de drogas como la marihuana.
Una vez que conozcamos estos datos, debemos intentar, cuando sea posible, separar los cofactores y la ingestión del alimento que pueda contener LTP al menos 2 horas.
¿Existe tratamiento para la alergia a LTP?
El principal tratamiento de la alergia a LTP es su evitación. Como hemos comentado previamente, la dieta de evitación será individualizada y específica para cada paciente. El alergólogo debe informar claramente de aquellos alimentos y situaciones que se deben evitar.
En segundo lugar, todo paciente con alergia a alimentos debe llevar consigo un plan y medicación de rescate acompañado de un correcto adiestramiento, para saber cómo actuar en el caso de que acontezca una reacción alérgica por ingesta inadvertida.
En último lugar, es posible que hayas leído que existe una opción de inmunoterapia frente a esta proteína. Es cierto: existe la opción de tratamiento con inmunoterapia frente a rPrup p3 (la proteína específica de LTP de melocotón). Este tratamiento está indicado para pacientes con “síndrome LTP”, es decir, aquellos pacientes que deben evitar la ingesta de múltiples alimentos de diferentes grupos no relacionados entre sí (frutos secos, hortalizas o frutas). Es tu alergólogo el que debe decidir si este tratamiento es adecuado para ti, de forma completamente personalizada.
Dra. Isabel Fernández de Alba Porcel, Hospital HLA Inmaculada de Granada. Comité de Alergia Infantil SEAIC
Fuentes:
- Fernández-Rivas M. Fruit and vegetable allergy. Chem Immunol Allergy. 2015;101:162-70. doi: 10.1159/000375469.
- Asero R, Piantanida M, Pinter E, Pravettoni V. The clinical relevance of lipid transfer protein. Clin Exp Allergy. 2018 Jan;48(1):6-12. doi: 10.1111/cea.13053.
Telealergia: ¿vino para quedarse?
Artículo: Teleallergy: Where Have We Been and Where Are We Going? Ramsey A, Chen Wu A, Bender B, Portnoy J. J Allergy Clin Immunol Pract 2023;11:126-31.
La telemedicina se puede definir, como el uso de las tecnologías de la información, por medio de los sistemas telemáticos, para proporcionar asistencia médica, independientemente de la distancia que separa al paciente del profesional médico.
Los primeros datos de telemedicina aplicados al campo de la Alergología son muy escasos a partir de los años 90. Sin embargo, el uso de la telemedicina se incrementa de forma exponencial a partir del año 2020. Este año, queda marcado en la historia por la extensión de la enfermedad provocada por el virus SARS-CoV-2019 (COVID-19), lo que condicionó un cierre de la actividad socioeconómica mundial casi global. Tras declararse la pandemia por la Organización Mundial de la Salud en marzo de 2020, el gobierno español decretó el estado de alarma con el consiguiente confinamiento domiciliario, que se prolongó hasta junio de 2020. Posteriormente se han sucedido diversas olas pandémicas que han ido afectando de forma diversa la asistencia médica.
El modelo de acceso y prestación de la asistencia sanitaria cambió bruscamente, primero en la Atención Primaria, y posteriormente en las diferentes especialidades médicas. El patrón clásico de asistencia presencial, ha sido sustituido por un patrón mixto, en el que las herramientas de telemedicina han desempeñado un papel determinante. Centrándonos en el campo de la Alergología, investigadores norteamericanos dirigidos por Ramsey y cols., han llevado a cabo una revisión sobre el impacto de la telemedicina en la satisfacción de los pacientes alérgicos, en el coste de la asistencia, así como en el entorno normativo que debe regular en el futuro la telemedicina.
1.- Satisfacción del paciente
- Satisfacción del paciente antes de la epidemia COVID:
Hay diversos estudios en los primeros años del siglo XXI. Así, en 2015, Portnoy y cols., compararon las visitas presenciales frente a la teleasistencia, en 169 pacientes pediátricos con asma bronquial. El 90% de los pacientes consideraban satisfactoria la asistencia sanitaria, y un 88% la recomendaría para las revisiones médicas.
- Satisfacción durante la epidemia COVID:
Diversos estudios muestran una opinión favorable. En el estudio de Mustafa y cols., con 251 pacientes alérgicos, la satisfacción fue general para todos los tipos de enfermedades alérgicas, salvo en la alergia a alimentos, donde los pacientes consideraron óptima la visita presencial. En otro estudio dirigido por Emory con 269 pacientes, la satisfacción fue plena con la consulta telemática para el 79% de los pacientes, siendo el dato mas relevante la facilidad para poder asistir a la cita. No obstante, incluso con datos satisfactorios, los investigadores refieren que determinados procedimientos en el campo de la Alergología, como la realización de las pruebas cutáneas o los estudios de pruebas de tolerancia con alimentos o medicamentos requieren de la visita presencial. Otros estudios, sin embargo, muestran una mayor satisfacción con las visitas presenciales, especialmente en pacientes con dermatitis atópica, múltiples alergias a alimentos o pacientes pediátricos con asma bronquial.
2.- Satisfacción del médico
Tradicionalmente los alergólogos no han utilizado la telemedicina, por lo que se les deben facilitar herramientas que permitan su uso. Sin embargo, salvo en algunos países, no se han desarrollado programas de formación para los especialistas ni tampoco la asistencia mediante aplicaciones informáticas.
La principal ventaja de utilizar la telemedicina en la práctica clínica habitual es el ahorro de tiempo que supone para el médico disminuir las horas de consulta dedicadas a labores burocráticas. Este tiempo podría reinvertirse en reducir las listas de espera dedicadas a dar resultados analíticos, resolver dudas a pacientes a cerca de tratamientos de una forma más rápida, así como conseguir una comunicación más fluida con pacientes y médicos de Atención Primaria. De esta manera, se agilizarían procedimientos ordinarios y mejoraría la calidad asistencial del paciente.
3.- Coste socioeconómico de la telemedicina
Por un lado, la telemedicina puede reducir los costes de las enfermedades alérgicas ya que disminuye los gastos en el transporte hasta la consulta médica, así como el absentismo escolar y laboral. Sin embargo, tiene otras desventajas que pueden incrementar el coste como es la falta de acceso directo al profesional sanitario y su supervisión, lo que puede implicar una peor evolución clínica de la enfermedad. Existen pocos estudios durante la pandemia Covid de telemedicina y coste sanitario. En un estudio sobre pacientes pediátricos diagnosticados de asma bronquial, se observó que tras realizar un programa de telemedicina en el primer año de la pandemia Covid, hubo una reducción en las reagudizaciones asmáticas. Este hecho puede ser atribuible no a la telemedicina en si misma, sino a la escolarización en casa durante los primeros meses Covid, así como el uso de la mascarilla, ya que ambas situaciones redujeron la exposición a diferentes virus durante ese periodo de tiempo, lo que puede explicar la reducción en las exacerbaciones asmáticas. Por otro lado, es conocido que la telealergia tiene su mayor potencial de mejora del gasto sanitario en las zonas rurales o áreas que no disponen de alergólogo cercano, por lo que requieren un desplazamiento importante para la asistencia médica. Así, en un estudio alemán hecho con 112 pacientes con rinitis alérgica, la telemedicina generó un ahorro de 60.000 euros por año y redujo en 2.3 los días perdidos de trabajo o escuela, por paciente y año.
4.- Cambios en el marco regulatorio
La introducción y el uso progresivo de la telemedicina aplicado al campo de la Alergología, debe acompañarse de una actualización en el marco legislativo, así como de la cobertura y coste de los seguros de asistencia médica, tanto en la Sanidad Privada como Pública, que deben ir acometiéndose durante los próximos años.
CONCLUSIONES
Tras la pandemia Covid, la telemedicina aplicada al campo de la Alergología es una realidad. Esta herramienta ofrece ventajas, las principales, la reducción de absentismo laboral/escolar y transporte, la mejor adherencia en el seguimiento y la mayor agilidad en las revisiones médicas. Ofrece también una posible mejoría en la educación continuada del paciente alérgico con las diferentes herramientas informáticas, así como en el seguimiento del cumplimiento terapéutico. Sin embargo, pese a estas ventajas, la asistencia presencial seguirá siendo vital en nuestra especialidad, para la realización de muchos de nuestros procedimientos diagnósticos y terapéuticos, así como para aquellos pacientes que requieran un diagnóstico inicial, una valoración directa por parte del alergólogo o cuando la gravedad o el control de la enfermedad así lo requiera.
Marta Reche. Servicio de Alergología. Hospital Universitario Infanta Sofía. San Sebastián de los Reyes. Madrid. Comité de Alergia Infantil
Un caso insólito
Llevo más de un mes en el hospital. Perdí el conocimiento en plena calle y cuando desperté ya estaba aquí. Al principio me hacían pruebas, que si un “tac”, unos análisis, una resonancia, pero creo que ya me han dado por imposible, porque todo está bien y no saben que me pasa. Por las mañanas rodean mi cama varias batas blancas que discuten sobre enfermedades raras: ¡no!, en ese síndrome no hay visión borrosa, ¡no!, ese cuadro nunca se acompaña de vómitos, ¡no!, en esa patología jamás se ha visto pérdida de conciencia. Y así. Es mi momento de gloria, porque aunque nunca me hablan ni me miran, me hacen sentir importante. Me gustaría que me descubrieran algo, aunque sólo fuese para darles esa satisfacción.
Yo me encuentro bien; no se come mal y total, tampoco tenía trabajo…, aquí nadie me obliga a levantarme, ni me manda al supermercado o a sacar la basura. Al revés, todos son muy agradables y si necesito algo sólo tengo que tocar el timbre.
Cuando tiene turno de noche la enfermera rubia de las tetas estupendas, mando a mi mujer a dormir a casa; que descanse la pobre, lleva mucho tiempo a mi lado en un sillón y amanece como una alcayata. Piropeo a la sanitaria y ella hace que se enfada, pero yo sé que le encanta. Cosas de mujeres.
Si me aburro mucho, me pongo rígido, me cimbreo un poco, vuelvo los ojos y dejo que se me caiga la baba. Entonces me ponen algo que me deja flotando varias horas. Gratis, y mejor que la buena hierba, o sea que no puedo quejarme.
En fin, ellos siguen enredando. Vuelven a preguntarme si me ha pasado otras veces, y yo que sí, que cuántas, y yo que dos o tres, que desde cuándo, y yo que desde la Comunión de mi chico…, después que cuantos años hace de la Primera Comunión de mi niño, ¡qué importará eso! Tendrán muchos estudios, pero conmigo no aciertan.
Me parece, (es mi modesta opinión), que esto que me pasa es porque tengo alergia a las avispas y cuando me pican me quedo muerto, pero ellos sabrán, que son los médicos. Mientras tanto yo aquí, como un señor: a mesa y mantel.
Virginia Reguera Parra
Ganador del I Certamen de Alergia y Humanidades en la categoría de «Relatos»
Día internacional de concienciación de la Enterocolitis Inducida por Proteínas de la Dieta (FPIES).
El pasado 4 de mayo se celebró el día de Star Wars (May the 4th) que coincidió con el día internacional de concienciación de la Enterocolitis Inducida por Proteínas de la Dieta (FPIES).
La FPIES es una alergia a alimentos no mediada por IgE, que típicamente comienza en la infancia, y que se caracteriza por vómitos repetidos, prolongados en el tiempo, que comienzan entre 1 y 4 horas tras la ingesta del alimento y que a menudo se acompañan de decaimiento, letargia o palidez y deposiciones diarreicas.
Los datos epidemiológicos referentes a esta enfermedad son escasos y variables, esto es debido a que, hasta finales de los años 70 no se había reconocido ni definido formalmente este síndrome y también a que no ha recibido una codificación adecuada hasta octubre de 2015 cuando se implementó el código K52.2 en la décima revisión de la Clasificación Internacional de las Enfermedades (CIE-10).
El diagnóstico de FPIES se basa fundamentalmente en la presencia de síntomas característicos que mejoran tras la retirada del alimento causal de la dieta. Estos criterios se han ido modificando según ha ido avanzando el conocimiento y reconocimiento de esta enfermedad. Actualmente están en vigor los propuestos por el Consenso Internacional para el Diagnóstico y Manejo de la Enterocolitis Inducida por Proteínas de la Dieta, elaborado por el grupo de trabajo de reacciones adversas a alimento de la Academia Americana de Alergia, Asma e Inmunología (AAAAI).
Actualmente se reconocen dos presentaciones clínicas:
- FPIES aguda.- Que se manifiesta por los síntomas típicos previamente mencionados.
- FPIES crónica.- Peor caracterizada que la FPIES aguda, descrita fundamentalmente en lactantes menores de 4 meses alimentados con fórmula adaptada de proteínas de leche de vaca o de soja. Las manifestaciones clínicas incluyen vómitos intermitentes, diarrea acuosa y fallo de medro. Los síntomas se producen a lo largo de varios días o semanas y no tienen una clara relación causal con el alimento.
Cualquier alimento es susceptible de producir FPIES, los alimentos más frecuentemente implicados son las proteínas de leche de vaca, y en nuestro medio el pescado. El alimento implicado varia en función de la localización geográfica y no resultan extrapolables las series anglosajonas o japonesas publicadas. En el área mediterránea no es tan frecuente la asociación de FPIES por leche de vaca y la FPIES por soja, por lo que la evitación de este último alimento es discutible y debe ser evaluarse de manera individual. En cuanto a los alimentos sólidos, el pescado es si duda el principal agente causal de FPIES en el área mediterránea. En estos casos se pueden evitar dietas restrictivas innecesarias testando pescados alternativos, minimizando los riesgos de déficits nutricionales en nuestros pacientes para mas información sobre este punto: Infante et al. Food protein-induced enterocolitis syndrome by fish: Not necessarily a restricted diet. Allergy. 2017;00:1-5.
Dado que las manifestaciones clínicas son exclusivamente gastrointestinales y la edad más frecuente de presentación es la infancia, el retraso diagnóstico o un diagnóstico erróneo suele ser habitual. La mayoría de los niños sufren mas de una reacción, en ocasiones grave y con necesidad de acudir a Urgencias, antes de que sean correctamente diagnosticados. Por ello es importante tener presente esta patología ante cuadros exclusivamente digestivos y con resolución en las siguientes 24 horas.
Para un mejor conocimiento de esta patología recomendamos la lectura de:
- International consensus guidelines for the diagnosis and management of food protein-induced enterocolitis syndrome: Executive summary-Workgroup Report of the Adverse Reactions to Foods Committee, American Academy of Allergy, Asthma and Immunology. Nowak-Wegryzn et al. J Allergy Clin Immunol. 2017 Apr;139(4):1111-1126.e4. doi: 10.1016/j.jaci.2016.12.966
- Food Protein-Induced Enterocolitis Syndrome. Nowak-Wegryzn A et al. J Investig Allergol Clin Immunol 2017;27(1):1-18. Doi: 10.18176/jiaci.0135.
Ambos artículos, de acceso libre, resumen de manera práctica y didáctica el conocimiento actual de FPIES. “Aquello que no se conoce no se diagnostica”
Sonsoles Infante Herrero. Médico Adjunto. Unidad de Alergia Pediátrica. Hospital General Universitario Gregorio Marañón. Madrid.
ESOFAGITIS EOSINOFÍLICA EN PACIENTES PEDIÁTRICOS
La esofagitis eosinofílica (EoE) se considera una enfermedad crónica emergente; en la actualidad, ha pasado a ser una de las condiciones más comunes en la valoración y diagnóstico de problemas alimentarios en niños así como en la evaluación de disfagia y/o impactación en la edad adulta.
Se ha estudiado más extensamente en países occidentales, pero, aunque existen datos de prevalencia, se precisan estudios más amplios para consensuar datos epidemiológicos reales. Una revisión sistemática reciente mostró que la prevalencia poblacional de esofagitis eosinofílica en niños es 19,1 casos por 100.000 niños/año (1), con gran variabilidad de los datos según la localización geográfica y, probablemente, de otros factores como el diseño del estudio, los criterios diagnósticos utilizados, etc.
Fisiopatogénicamente se caracteriza por una inflamación Th2 en la que intervienen mecanismos mixtos mediados y/o no mediados por IgE dando lugar a una inflamación eosinofílica en el epitelio esofágico que origina una disfunción del mismo, dando lugar a los síntomas clínicos característicos.
En la población pediátrica los síntomas más prevalentes son los vómitos, dolor abdominal, disfagia, odinofagia e impactación del bolo alimenticio. Estas características clínicas difieren también según la edad del niño, siendo en niños más pequeños (2-8 años) más frecuente: el fallo de medro, rechazo del alimento, dolor abdominal, vómitos, trastornos del sueño, etc. En niños mayores y adolescentes los síntomas se asemejan más a los adultos, presentando disfagia, impactación, odinofagia, regurgitación, etc.
La prueba de oro para el diagnóstico es la toma de biopsias tanto de esófago proximal como distal (aumentando así el rendimiento del estudio) mediante una endoscopia digestiva. Esta técnica precisa de la sedación del paciente, lo que supone un “inconveniente” sobre todo en población pediátrica. Por ello se están estudiando otras técnicas menos invasivas como:
– Prueba del hilo esofágico (EST: esophageal string test), técnica basada en cápsulas que capturan las proteínas asociadas a los eosinófilos de la luz esofágica.
–Citoesponja: tecnología basada también en cápsulas, diseñada originalmente para la evaluación de la mucosa esofágica en el esófago de Barrett.
– Endoscopia transnasal sin sedación.
Estas técnicas y algunas otras en estudio también, podrían tener un papel importante en el control regular de la esofagitis, pero es muy poco probable que reemplacen la confirmación de un diagnóstico dudoso y/o actos terapéuticos realizables durante una endoscopia convencional como una dilatación.
Las opciones terapéuticas, ambas consideradas de primera línea son: tratamiento dietético y farmacológico:
– Terapias dietéticas: la fórmula de aminoácidos se describe como una terapia eficaz en niños con EoE, lo que indica la implicación de antígenos dietéticos en su patogenia. Se han descrito diversos enfoques dietéticos: dieta elemental, dieta dirigida según sensibilización alergénica, dietas empíricas, etc. La dieta de eliminación es una opción no farmacológica de primera línea para el manejo de la EoE; sin embargo, el orden y el número de antígenos específicos a evitar, así como su posterior reintroducción sigue siendo un área activa de investigación.
– Corticoides tópicos: este tipo de fármaco actúa a diversos niveles en esta patología: vías/genes inducidos por IL-13, reducción de la eosinofilia esofágica e infiltración mastocitaria, regulación a la baja de los genes de los mastocitos, reducción de células T y citocinas proinflamatorias como el factor de necrosis tumoral (TNF), etc. Los metanálisis realizados utilizando fluticasona o budesonida demuestran la superioridad de los corticoides frente a placebo para la eosinofilia esofágica, los hallazgos endoscópicos y los síntomas tanto en pacientes adultos como pediátricos. No están exentos de efectos adversos como puede ser la candidiasis, insuficiencia suprarrenal, etc. Los estudios abogan por una terapia que debe ser mantenida a largo plazo por la alta tasa de recaídas tras su retirada. Sigue en estudio la dosis y duración óptima de cada terapia.
– Tratamiento con inhibidores de la bomba de protones (IBP): la tasa de respuesta varía ampliamente desde un 30 a un 70%.Están en estudio las posibles diferencias fisiopatológicas entre la EoE sensible y/o resistente a los IBP. Algunos ejemplos incluyen:
– Técnicas de biología molecular demuestran que la expresión del transcrito para el canal de potasio Kir2.1 (gen KCNJ2) es menor en los pacientes que responden a los IBP. Si se valida, esto podría proporcionar una detección potencial para terapias personalizadas.
– Los pacientes con rinitis alérgica y metabolizadores rápidos CYP2C19 tienen un mayor riesgo de pérdida del control de la EoE a pesar de la terapia continua con IBP.
– Dilatación esofágica: destinada a aliviar complicaciones como la estenosis; técnica destinada a modificar cambios estructurales sin alivio histológico.
– Terapias emergentes:
* Nuevas formulaciones de esteroides: budesonida viscosa, budesonida en comprimidos bucodispersables, etc.
* Tratamientos biológicos: ANTICUERPOS MONOCLONALES
Anti-L5: benralizumab, mepolizumab, reslizumab. Se están realizando estudios para valorar la mejoría tanto clínica como histológica de estos tratamientos, por la involucración de la IL-5 en la infiltración y supervivencia del eosinófilo, sin resultados científicamente concluyentes aún.
Anti-IL13: la IL-13 es un mediador claramente implicado en la patogénesis de la EoE, mediante la activación y quimiotaxis de los eosinófilos a través del aumento de los niveles de eotaxina-3 y periostina. El anticuerpo QAX576 parece reducir los síntomas pero no se ha demostrado efecto significativo en la actividad clínica de la enfermedad; mientras que RPC4046 consigue una reducción significativa de la eosinofilia esofágica y la actividad de la enfermedad endoscópica así como en la reducción de síntomas.
Anti-IL4 y Anti-IL-13: Dupilumab (aprobado por la FDA en > 12 años). Se están llevando a cabo ensayos que parecen demostrar mejoría sintomática, endoscópica e histológica significativa.
Anti-IgE (omalizumab) y Anti-TNF (infliximab). No existe ningún ensayo clínico con evidencia científica que apoye su uso en la EoE.
*Otras dianas moleculares en estudio: Integrina α4β7, Siglec 8, TSLP, TGFβ, canales de calcio, IL- 9, 15 y 33, receptor de eotaxina anti CCR3.
Dra. Guacimara Hernández Santana, Hospital Universitario Nuestra Señora de la Candelaria en Santa Cruz de Tenerife. Comité de Alergia Infantil SEAIC
BIBLIOGRAFÍA:
- Arias A, Perez-Martinez I, Tenias JM, Lucendo AJ. Systematic review with meta-analysis: the incidence and prevalence of eosinophilicesophagitis in children and adults in population-based studies. Aliment Pharmacol Ther 2016; 43(1): 3-15.
- Alfredo J Lucendo (2019): Pharmacological treatments for eosinophilic esophagitis: current options and emerging therapies, Expert Review of Clinical Immunology, DOI:10.1080/1744666X.2019.1705784
- Nirmala P. Gonsalves, Seema S. Aceves. Diagnosis and Treatment of Eosinophilic Esophagitis. J Allergy Clin Immunol. 2020 January ; 145(1): 1–7.
- Thomas Greuter, Ikuo Hirano, Evan S. Dellon. Emerging therapies for eosinophilic esophagitis. J Allergy Clin Immunol. 2020 January ; 145(1): 38–45.
- Arianna De Matteis et al. Eosinophilic Esophagitis in Children: Clinical Findings and Diagnostic Approach.Current Pediatric Reviews, 2020, 16, 206-214.
¿Qué es la anafilaxia?
En esta primera entrada del blog del Comité de Anafilaxia parece lógico que hablemos acerca de lo que es la anafilaxia.
La anafilaxia es una respuesta inmunológica extrema del sistema inmunitario ante una sustancia alergénica a la que el paciente ha desarrollado alergia.
En esta reacción se libera una gran cantidad de histamina y otras sustancias químicas en el cuerpo, lo que causa una serie de síntomas graves, de instauración rápida y potencialmente mortales, especialmente si no se reconocen los síntomas a tiempo y no se actúa rápidamente.
En este caso la reacción alérgica afecta a todo el organismo, y puede manifestarse con síntomas variados y simultáneos en diversos sistemas; por tanto, sus síntomas pueden variar ampliamente, pero comúnmente incluyen síntomas sugestivos de alergia que afectan a la vez la piel, el aparato respiratorio, el tracto digestivo o sistema cardiovascular.
La afectación de la piel, con urticaria, enrojecimiento, picor o hinchazón, es la manifestación más frecuente en la anafilaxia; está presente en el 80 % de los casos.
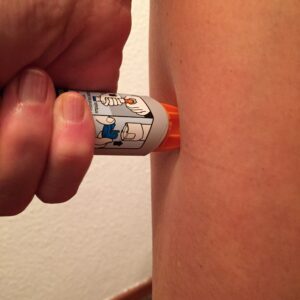
La anafilaxia es una emergencia médica que requiere atención inmediata. El tratamiento principal es la inyección precoz de adrenalina intramuscular en el muslo.
Es crucial, una vez tratado el cuadro, identificar y evitar los desencadenantes conocidos de la reacción para prevenir futuros episodios de anafilaxia. El especialista adecuado para ello es alergólogo, a quien debe ser remitido todo paciente que haya presentado una anafilaxia.
Es importante que las personas alérgicas que hayan presentado una anafilaxia y sus familiares estén preparados para actuar en caso de una nueva reacción anafiláctica. Esto implica llevar siempre consigo una inyección de adrenalina y saber cómo administrarla correctamente
Alergia a Prunáceas
En Verano aumenta el consumo de futas de la familia de las prunáceas, que son aquellas que tienen un hueso que contiene en su interior una especie de almendra, como el melocotón, albaricoque, cereza, ciruela, paraguayo o nectarina. Se consideran responsables del 70 % de todas las reacciones alérgicas a las frutas.
Algunos tips importantes a tener en cuenta son:
- En el área mediterránea predomina la alergia a vegetales por sensibilización a LTP (proteínas transportadoras de lípidos), muy presentes en las prunáceas, especialmente en la piel, donde su concentración es mucho mayor.
- La LTP es un alérgeno muy estable que condiciona que su alergia se produzca con la ingesta de la fruta fresca al igual que procesada (zumos, mermeladas, compotas…)
- Conocer el alérgeno vegetal responsable de la alergia permite predecir la gravedad de las manifestaciones clínicas que puede desencadenar y la posible reactividad cruzada con otros alimentos. La alergia a LTP se puede asociar con alergia a otros alimentos como frutos secos y otras frutas rosáceas (manzana, fresa…)
- Especialmente en el caso de alergia a LTP, algunos factores como el ejercicio físico, el alcohol o los antiinflamatorios (AINE) pueden actuar como cofactores, y desencadenar o amplificar una reacción.
- La alergia a prunáceas en nuestro país, aunque con menor frecuencia, también se puede producir relacionada con la alergia al polen y en este caso, en muchos pacientes, es posible consumir la fruta cocinada. Es aconsejable por tanto, seguir las indicaciones de su alergólogo sobre la evitación o los permisos en las formas de consumo.
La reacción alérgica a las prunáceas como el melocotón se suele producir después de su ingesta y, con menor frecuencia, tras su inhalación o tras el contacto cutáneo. Cuando provoca síntomas, suelen aparecer en la primera hora, habitualmente a los pocos minutos. Los síntomas que puede desencadenar incluyen:
- Síndrome de alergia oral (SAO). Síntomas locales leves, que consisten en picor oral, orofaríngeo y/o ótico. Son los más frecuentes
- Síntomas cutáneos. Síntomas locales en la zona de contacto con el alimento, o generalizados en forma de urticaria y angioedema (hinchazón) de labios, párpados, lengua u otras zonas.
- Síntomas digestivos. Náuseas, vómitos, dolor abdominal, distensión abdominal, diarrea
- Anafilaxia. Reacción alérgica grave de instauración rápida y de riesgo para la vida. Puede iniciarse con picor oral, faríngeo, en manos, pies o cuero cabelludo y después progresar con generalización del picor y aparición de urticaria y/o angioedema, así como síntomas generales respiratorios, digestivos y cardiovasculares (conjuntivitis, obstrucción nasal, estornudos, mucosidad, dificultad para tragar o respirar, tos, silbidos, náuseas, vómitos, dolor abdominal, diarrea, y caída de la tensión arterial con mareo, pérdida de conocimiento, y si la situación se prolonga sin tratamiento, parada cardiorrespiratoria). Se requiere, pues, tratamiento médico urgente en el momento del episodio. En cuanto el paciente advierte la generalización de la reacción, debe administrarse la adrenalina autoinyectable y ser llevado a un centro médico.
Es importante un buen diagnóstico para evitar los alimentos con los que el paciente presente síntomas. Así mismo, siempre llevar consigo la medicación de rescate como antihistamínicos, corticoides y por supuesto la adrenalina autoinyectable.
«Participa en mejorar el conocimiento sobre Inmunoterapia con Alimentos!»
La inmunoterapia es el tratamiento estrella de la especialidad de alergología, claramente diferenciado del resto de tratamientos por su enfoque etiológico. La inmunoterapia con alimentos ha experimentado un auge en las últimas dos décadas que se ha disparado a partir del momento en que la industria farmacéutica ha tomado una posición predominante liderando proyectos de investigación con poblaciones mucho más grandes que las que se reunían mediante iniciativas meramente académicas.
Este desarrollo a nivel de investigación se ha visto respaldado con la nueva publicación de la guía de inmunoterapia europea, en la que por primera vez, se abre una puerta oficial al empleo de inmunoterapia con alérgenos para la alergia alimentaria fuera del contexto de la investigación en centros con un nivel de experiencia y recursos elevado. Hasta la fecha de esta importante publicación, la posición oficial de las organizaciones científicas era la de no recomendar este tipo de tratamiento fuera del contexto de la investigación, a pesar de que su uso se estaba produciendo en determinados centros de muchos países europeos.
En los próximos años, es probable que nos encontremos con productos farmacológicos aprobados para el uso en inmunoterapia oral con alimento, que a su vez, aumenten la demanda de los pacientes para recibir este tipo de tratamiento. Sin embargo, puede darse la situación de que la demanda supere la capacidad de los servicios de alergia para atender dichas peticiones por la complejidad del tratamiento y las dificultades en instaurarlo como parte de la cartera de servicios en departamentos donde no sea un tratamiento en el que no se tenga experiencia.
Con la meta de realizar un mapa a nivel europeo de los centros donde se administra este tratamiento y conocer la forma en que se está realizando, surge el proyecto FIND, del acrónimo en inglés Food Immunotherapy Practice: Nation Differences Across Europe (Práctica de inmunoterapia con alimentos: diferencias entre las naciones en Europa). Este proyecto inicia su camino en Noviembre de 2017, cuando consigue financiación por parte de la EAACI para su puesta en marcha. El grupo de trabajo está constituido por 12 miembros de distintos países europeos y un comité asesor con expertos en alergia a nivel mundial. Tras elaborar un cuestionario, el estudio inicia su fase de recopilación de datos el 20 de Junio de 2018 con el envío de una invitación masiva a todos los miembros de la EAACI para comunicar su experiencia con el tratamiento.
En caso de no haber recibido dicha invitación, y querer participar, puedes hacerlo a través de este link: (https://www.surveymonkey.com/r/FINDproject_Level2) o bien, ponerte en comunicación con el coordinador en nuestro país (find.spain2018@gmail.com) para recibir la información que quieras solicitar y decidir tu participación.
Desde el Comité Infantil de Alergia, os invitamos a participar para que conozcamos cual es la realidad sobre este tratamiento tan relevante.
Pablo Rodriguez Del Rio. Comité de Alergia Infantil SEAIC.
USO Y DESUSO DE LA ADRENALINA
En las últimas décadas el término alergia se ha convertido en un concepto popular y casi familiar, facilitado sobre todo por la incidencia progresivamente creciente de las distintas patologías alergológicas y el impacto socio-sanitario que estas representan.
Por supuesto, entre las varias formas de presentación clínica, la anafilaxia es la que más nos preocupa como médicos, no solo como alergólogos, ya que por definición representa una “reacción alérgica grave de instauración rápida y potencialmente mortal”. En los últimos años se ha multiplicado el esfuerzo de la comunidad científica para sensibilizar a la sociedad sobre esta patología y tratarla como se merece, con el intento de minimizar las consecuencias que de ella puedan surgir.
En el algoritmo de actuación de la anafilaxia, la adrenalina intramuscular representa el tratamiento de primera línea independientemente de la edad del paciente y del entorno en que ocurra. El retraso en la administración de este medicamento se ha asociado a desenlaces fatales o reacciones bifásicas. La administración de adrenalina siempre tiene que estar seguida de una valoración médica por el Servicio de Urgencias más cercano. Una vez resuelto el cuadro clínico, al paciente se le prescribirá un auto inyector de adrenalina con un informe médico en el que deben de estar representados un plan escrito de recomendaciones (alérgeno a evitar) así como una explicación detallada del correcto uso de la adrenalina.
Recientemente se ha publicado un trabajo interesante que investiga las razones por las cuales hay un menor uso de adrenalina en la atención del paciente pediátrico (“Factors associated with the underuse of adrenaline in children with anaphylaxis”). Se trata de un estudio multicéntrico que incluyó 149 pacientes (edad menor de 15 años) atendidos por anafilaxia en 18 Servicios de Urgencias del norte de Francia, en un periodo comprendido entre los años 2015 y 2017. La edad media de los niños incluidos en el estudio era de 7,4 años; 35 niños (23%) estaban diagnosticados previamente de alergia alimentaria y 17 niños (11%) habían ya experimentado una anafilaxia. El Servicio de Emergencia Extrahospitalario de la zona fue contactado en 63 ocasiones (43%), en 55 de ellas (37%) los niños recibieron tratamiento in situ, por sus familias o por el mismo Servicio de Emergencias. Antes de la llegada de ayuda médica, 15 de los 31 niños (48%) con un dispositivo de auto inyector de adrenalina recibieron el tratamiento, mientras que el Servicio de Emergencias solo la administró en 4 de los 55 casos. De los 149 niños diagnosticados de anafilaxia solo 52 de ellos (35% del total) recibieron tratamiento con adrenalina en un entorno hospitalario. En definitiva, solo 71 de los 149 (48%) recibieron tratamiento con adrenalina, y el auto inyector de adrenalina fue prescrito o renovado en 103 (69%) casos antes del alta hospitalaria.
Si analizamos los datos obtenidos en este estudio podemos concluir que se ha observado que la adrenalina fue administrada con más frecuencia en niños más pequeños (edad media de 6,5 años), no identificando otro factor que pueda ser asociado con un uso mas frecuente de adrenalina.
Podemos concluir también que las dos principales razones por las que la adrenalina no se administró en ninguno de los escenarios (intra o extra hospitalario) de asistencia médica fueron:
- subestimación y falta de reconocimiento de la potencial gravedad de la reacción presentada.
- espontánea y rápida mejoría de la clínica desde los primeros síntomas/signos presentados.
El miedo a los posibles efectos adversos de una administración de adrenalina no se reconoció como una causa frecuente para su menor utilización.
Los autores concluyen que la distancia entre el porcentaje de un diagnóstico correcto y los casos que fueron tratados con adrenalina como primera línea de tratamiento sea principalmente debido a no considerar la reacción anafiláctica lo suficientemente grave si ésta no asocia una afectación respiratoria y circulatoria.
En definitiva y como conclusión importante que debemos de sacar de todo este texto es que la administración de adrenalina i.m. es el tratamiento de primera línea para una anafilaxia siendo ésta capaz de reducir las consecuencias potencialmente fatales, antes de que eventualmente se presente una afectación cardiorrespiratoria.
Dr. Nicola Giangrande, del hospital Hospital Público da Mariña , Burela (Lugo). Comité de Alergia Infantil SEAIC.
Articulo aconsejado:
¿En qué consisten las pruebas cutáneas a medicamentos?
Las pruebas cutáneas son útiles para el diagnóstico de la alergia a medicamentos. Existen tres tipos de pruebas cutáneas para el diagnóstico alergológico: prick-test (pruebas intraepidérmicas), pruebas intradérmicas y las pruebas epicutáneas (parches). En el prick test se aplica una gota del medicamento a estudiar en la cara anterior del antebrazo y se hace una ligera punción con una lanceta a través de la gota de dicho medicamento y la capa más externa de la piel conocida como epidermis. De esta forma, se permite que el medicamento penetre y contacte directamente con las células responsables de las reacciones alérgicas, los mastocitos.
Si el paciente presenta un resultado positivo, los mastocitos reaccionan, liberando unas sustancias que producen inflamación, lo que se traduce en la aparición de una roncha o habón, rodeada de un eritema (piel roja). Esta respuesta se inicia en pocos minutos y es máxima a los 15 o 20 minutos y va cediendo a lo largo de las horas.
Si el resultado es negativo, es decir, no se produce la aparición de la roncha, se procede a la prueba cutánea intradérmica. Estas pruebas son más sensibles que las anteriores y consisten en la inyección directa del medicamento en la segunda capa de la piel del paciente (dermis), con una aguja muy fina y se procede a la lectura de forma similar al prick. Está técnica tiene la ventaja de poder investigar la alergia de tipo tardío, que consiste en hacer una lectura a las 24, 48 e incluso 96 horas.
Las pruebas epicutáneas, llamadas también pruebas de parche, consisten en la aplicación sobre la piel, sin punzar, del medicamento sospechoso. Se utilizan generalmente para el diagnóstico de dermatitis de contacto y reacciones tardías, aquellas que aparecen más de 6 horas entre la administración del fármaco y la aparición de la reacción. Se mantiene el alérgeno en la piel, tapado con una tira adhesiva, que se retirará a las 48 horas. La lectura inicial de estas pruebas se realiza a las 48 horas y la respuesta se observa aproximadamente 2 días después de la retirada del parche.
Para realizar las pruebas cutáneas, no se debe de dejar de tomar la medicación habitual. Es importante evitar el tratamiento con antihistamínicos (cetirizina, ebastina, loratadina…) 5-7 días antes de las pruebas y los corticoides orales entre 7 a 21 días antes de las pruebas.
Dra. Giovanna Araujo Sánchez, M.D. PhD.
Servicio de Alergología (ICR).
Hospital Clínic Barcelona. IRCE-IDIBAPS.
Alergología en España y la Unión Europea
La Alergología es una especialidad médica oficialmente reconocida en España por los Ministerios de Sanidad, Política Social e Igualdad y de Educación.
Se entiende por Alergología la especialidad médica que comprende el conocimiento, diagnóstico y tratamiento de la patología producida por mecanismos inmunológicos, con las técnicas que le son propias. El Programa Oficial de la especialidad vigente se publicó en el BOE número 241, de lunes 9 de octubre de 2006.
Para acceder a la formación especializada en Alergología son requisitos previos imprescindibles ser licenciado en Medicina y obtener plaza en la convocatoria del examen MIR.
El alergólogo es un médico especializado en Alergología y por tanto preparado para prevenir, diagnosticar y tratar las enfermedades alérgicas y educar a pacientes y familiares sobre las mismas. Es importante resaltar que el alergólogo recibe formación y acumula experiencia en enfermedades alérgicas tanto en pacientes pediátricos como en adultos.
El alergólogo está capacitado para evaluar los diferentes aspectos de las enfermedades alérgicas que pueden afectar a distintos sistemas del organismo (piel, aparato digestivo, aparato respiratorio, sistema cardiovascular, etc). Es frecuente que un mismo paciente presente rinitis, conjuntivitis, asma, dermatitis y alergia alimentaria. El alergólogo es competente para realizar un diagnóstico y tratamiento integral.
En el momento actual la especialidad médica de Alergología existe como especialidad completa en 14 países de la Unión Europea (Chequia, Chipre, Eslovaquia, España, Grecia, Holanda, Italia, Lituania, Luxemburgo, Portugal, Reino Unido, Rumania, Suecia y Suiza). Además se reconoce como subespecialidad en otros 7 países (Alemania, Estonia, Finlandia, Francia, Hungría, Polonia y Turquía).
En relación con el proyecto de troncalidad, la Alergología se incluirá en el denominado tronco médico y se mantendrán las competencias de la especialidad.
Fuente: Comisión Nacional de la Especialidad de Alergología
» Título de Alergólogo Europeo
![]() Orden 3081/2006: Programa Oficial de la Especialidad de Alergología (6711 descargas )
Orden 3081/2006: Programa Oficial de la Especialidad de Alergología (6711 descargas )
Atención del niño alérgico en Urgencias: El Papel del Triaje
Cuando diagnosticamos a un paciente de anafilaxia, le indicamos una serie de medidas de actuación en caso de que presente un nuevo episodio que incluyen la autoadministración de adrenalina y la necesidad de acudir a un centro médico para ser evaluado y tratado. Es más, asumimos que ese paciente será atendido correcta y rápidamente en Urgencias.
Somos poco conscientes del papel que han cobrado los sistemas de Triaje en la mayoría de los servicios de urgencias para hacer frente a la creciente presión asistencial. En los últimos 25 años se han implantado progresivamente múltiples sistemas de triaje hospitalario1, en base a los que se decide cuándo (tiempo de espera), quién (según la organización propia del centro) y dónde (Consulta o Sala de Exploración, Sala de Reanimación…) se atiende a los pacientes. La sala de triaje es donde debe identificarse al paciente con anafilaxia.
Nuestro hospital utiliza el Canadian Paediatric E.D. TRIAGE and Acuity Scale (PaedCTAS)2, con 5 posibles niveles de prioridad (I: Reanimación, de atención inmediata; II: Emergencia, con un tiempo de espera de atención inferior a 15 minutos; III: Urgencia, con un tiempo de espera de unos 30 minutos; IV: Semi urgencia, con tiempo de espera de 1 hora y finalmente, la No Urgencia, con una espera de hasta 2 horas). Estos tiempos recomendados para atender a los pacientes se cumplen en mejor o en peor medida según la afluencia. Según este sistema de triaje una anafilaxia es una patología de prioridad I.
Nos planteamos evaluar la calidad del triaje del niño alérgico a raíz del comentario de un paciente en la Consulta. Nuestro paciente, con anafilaxia previa por alergia a alimentos, siguió todos los pasos indicados en consulta y en su informe clínico, incluidos el uso de su autoinyector y traslado a Urgencias de nuestro hospital. Una vez allí, y tras el triaje, se le envió a la Sala de Espera y fue dado de alta en menos de 2 horas.
Al evaluar triaje en urgencias de pediatría de otros niños atendidos por alergia encontramos que más de la mitad de los niños con diagnóstico de anafilaxia habían recibido una prioridad III (categoría: urgente; prioridad intermedia; tiempo de espera estimado: 30 minutos). En la práctica, una prioridad intermedia supone esperar en la Sala de Espera el mismo tiempo que niños con enfermedades tan frecuentes como la fiebre, gastroenteritis y bronquiolitis. En periodos epidémicos esto se traduce en retrasos de horas por el gran aumento de la demanda asistencial. Además, este retraso podría condicionar peor respuesta a la adrenalina (por su administración más tardía), y aumentar el riesgo de mortalidad. En nuestro centro Sólo un caso de cada 3 fue identificado correctamente como prioridad I-II3.
El siguiente paso fue proponer medidas de mejora de 2 tipos:
- Formación del personal de enfermería que realiza labores de Triaje: Se destacaron la importancia del tiempo de evolución y la duración de síntomas, la importancia de la anamnesis obtenida de los padres sobre la apariencia del paciente al llegar a Urgencias….
- Modificaciones en el propio Sistema de Triaje (no fue posible la implementación de modificaciones en el Soporte informático, por lo que se introdujo material de apoyo (chuleta) al personal encargado del triaje): Se destacó la importancia de la afectación multisistémica, la prescripción y/o el uso de dispositivos de adrenalina autoinyectable y la duración de síntomas.
Al reevaluar el funcionamiento de nuestra urgencia 12 meses después de estas medidas, encontramos que el número de niños correctamente triados había pasado del 36.2 % al 72.2 % y lo que es más importante, que el tiempo de espera medio se había reducido de 8 min a 1 min. También se observaron modificaciones en la ubicación de los pacientes, que, en lugar de ser enviados a la sala de espera, quedaron en observación4.
Nuestros resultados no son extrapolables a otros hospitales dado que en nuestro país se utilizan varios sistemas de triaje distintos, incluyendo, entre otros, el Sistema Canadiense de Triaje Pediátrico, Sistema Estructurado de Triaje-Modelo Andorrano de Triaje, Sistema Manchester de Triaje5. Cada uno de estos sistemas consta de procesos propios en su aplicación e idiosincrasia a la hora de gestionar la prioridad de los pacientes y de las patologías. Además, precisan de formación específica para su aplicación.
Como alergólogos:
- Debemos ser conscientes de que el triaje del servicio de urgencias es clave para que el paciente diagnosticado de anafilaxia reciba el tratamiento adecuado en el momento preciso.
- Deberíamos conocer el sistema de triaje que se utiliza en nuestros hospitales y saber si tiene (o no) problemas en la identificación de los pacientes con anafilaxia.
- Debemos colaborar con el personal de urgencias para, desde nuestro conocimiento de las peculiaridades de la anafilaxia, proponer medidas de mejora que faciliten la identificación precoz y por tanto, la atención correcta de los pacientes.
Dra. Esozia Arroabarren Alemán, Servicio de Alergia, Complejo Hospitalario de Navarra, Pamplona. Comité de Alergia Infantil SEAIC
Bibliografía
- Mínguez Navarro MC, Guerrero Márquez G, Ignacio Cerro MC, editores. Manual de Clasificación y Triage del paciente Pediátrico en Urgencias. Primera Edición. Majadahonda (Madrid): Ergon; 2015.
- Warren DW, Jarvis A, LeBlanc L, Gravel J; CTAS National Working Group; Canadian Association of Emergency Physicians; National Emergency Nurses Affiliation; Association des Médecins d’Urgence du Québec; Canadian Paediatric Society; Society of Rural Physicians of Canada. Revisions to the Canadian Triage and Acuity Scale paediatric guidelines (PaedCTAS). CJEM. 2008; 10(3):224-43.
- Arroabarren E, Alvarez-Garcia J, Anda M, de Prada M, Ponce MC, Palacios M. Quality of the Triage of Children With anaphylaxis at the Emergency Department. Pediatr Emerg Care. 2018 May 15. doi: 10.1097/PEC.0000000000001442
- Arroabarren E, Alvarez-García J, Anda M, de Prada M, Ponce C, Alvarez-Puebla MJ. Impact of specific training in anaphylaxis of the Triage nursing staff in a Tertiary Hospital’s Paediatric Emergency Department. J Investig Allergol Clin Immunol. 2018 May 2:0. doi: 10.18176/jiaci.0271.
- https://www.aetsa.org/download/publicaciones/antiguas/AETSA_2011-4_Triage_def.pdf (ultimo acceso: junio 2019)
Premios Best in Class
Apreciados socios:
Se adjunta carta de nuestro Presidente con información importante con respecto a la convocatoria de los premios Best in Class sobre la calidad de los servicios de Alergología del sistema sanitario público.
Un cordial saludo.
Dr. Pedro Ojeda
Secretario General Sociedad Española de Alergología e Inmunología Clínica
—————————————–
Documento para la descarga:
¿Sabías que la alergia al polen y la alergia a los alimentos están relacionadas?

1. ¿Qué es la alergia alimentaria derivada de la alergia al polen?
El síndrome de alergia polen-alimentos (pollen-food allergy syndrome-PFAS) es una alergia alimentaria tipo I en pacientes con alergia al polen. Se produce por reactividad cruzada de proteínas (alérgenos) homólogas (similares) presentes en polen y alimentos vegetales. Aunque los síntomas suelen ser leves y limitados a la orofaringe, en casos raros pueden ocurrir reacciones sistémicas graves.
2. ¿Cuáles son los alérgenos y pólenes implicados?
La sensibilización a los alérgenos de pólenes depende de la región geográfica. En España y en el área mediterránea es frecuente la sensibilización a profilinas de pólenes de gramíneas y malezas (ej. artemisia). Otros alergenos implicados son LTP (proteínas de transferencia de lípidos) de pólenes de árboles como el plátano de sombra y giberelinas de pólenes de cipreses. En el norte y centro de Europa, los alérgenos más relevantes son las PR-10 (proteínas homólogas de Bet v 1, alérgeno mayor del polen de abedul).
3. ¿Qué alimentos dan problemas?
Los más frecuentes son frutas, verduras y frutos secos crudos, ya que las proteínas mayormente implicadas son las profilinas y PR-10, que son sensibles al calor y a los jugos gástricos. Por eso muchos pacientes toleran la versión cocida, enlatada de la fruta/verdura. En el caso de implicación de proteínas como LTP o las giberelinas, que son resistentes al calor y digestión pueden causar reacciones más graves.
| Polen sensibilizante/alérgeno | Alimentos vegetales crudos frecuentemente implicados |
| Abedul/PR-10 | Manzana, melocotón, zanahoria, apio, cereza, ciruela, pera, kiwi, cacahuete, soja, avellana. |
| Gramíneas/profilina | Melón, sandía, melocotón, tomate, kiwi, berenjena, pimiento, cacahuete, trigo, centeno. |
| Artemisa/profilina, LTP | Sandía, melón, banana, calabacín, pepino, apio, zanahoria, pimiento, brócoli, semilla de girasol. |
| Plátano sombra, olivo, melocotonero/ LTP | Melocotón, nuez, avellana, cacahuete. |
| Cipreses/giberelinas | Naranja, melocotón, cereza, granada. |
4. ¿Cuáles son los síntomas y su gravedad?
- Leves (la mayoría): picor o hinchazón en labios, lengua, paladar y garganta a los pocos minutos de comer el alimento crudo. Normalmente remiten sin tratamiento específico en menos de una hora.
- Moderados: además de los síntomas en boca, pueden aparecer estornudos, lagrimeo, urticaria, dolor abdominal o náuseas.
- Graves (muy poco frecuentes): Dificultad para respirar, vómitos, caída de la tensión y anafilaxia. Estos síntomas pueden presentarse si el alimento está concentrado (como en batidos o zumos), si existen cofactores como el ayuno, ejercicio, ciertos fármacos (antiinflamatorios no esteroideos (AINEs), inhibidores de la bomba de protones (IBP)), asma mal controlada o tras una cirugía bariátrica.
5. ¿Cómo se diagnostica?
- Historia clínica detallada: relación clara entre la ingestión de alimentos vegetales crudos y síntomas inmediatos, en una persona con alergia al polen.
- Pruebas cutáneas: prick test con pólenes y prick-prick con la fruta/verdura/fruto seco: positivo en crudo y negativo en cocido/tostado sugiere PFAS.
- Diagnóstico molecular: identificación en suero de IgE específica del alérgeno responsable de la reactividad cruzada.
6. Prevención y tratamiento:
- Educación del paciente: Informar sobre el PFAS, su naturaleza generalmente benigna y el bajo riesgo de reacciones graves; educar sobre cofactores y agravantes anteriormente mencionados.
- Evitar el alimento crudo responsable de los síntomas. No es necesario eliminar otros vegetales.
- Estrategias prácticas:
-Profilina/PR-10: Cocer la fruta/verdura. Preferir conservas, enlatados, compotas, frutos secos tostados. No triturar en batido aquello que tolera entero (el licuado concentra alérgenos).
-LTP: Pelar y lavar la fruta/verdura. Revisar etiquetas de zumos, smoothies, preparados veganos, barritas con frutos secos. - Medicación:
-Antihistamínico oral, si aparecen síntomas.
-Autoinyector de adrenalina: indicado en caso de reacciones graves/sistémicas o pacientes de riesgo (asma mal controlada, implicación de cofactores). - Inmunoterapia: La vacunación con extractos de pólenes mejora la rinitis/asma. No se recomienda la inmunoterapia específica para polen (subcutánea o sublingual) como tratamiento para PFAS, ya que no hay suficiente evidencia de su eficacia.
7. Impacto emocional y calidad de vida:
Aunque las manifestaciones suelen ser leves, el miedo a que aparezcan con comidas nuevas puede generar ansiedad, dificultad en las salidas sociales y complicaciones con dietas vegetarianas. El acompañamiento por un alergólogo es vital y ayudará a limitar exclusiones innecesarias y a mantener una alimentación equilibrada.
8. Conclusiones:
Conocer los alimentos implicados, identificar los síntomas y aplicar medidas sencillas como cocinar, evitar batidos, grandes ingestas y en algunos casos pelar frutas; permite, a la mayoría de los pacientes, llevar una vida normal.
Es importante enfatizar el carácter generalmente benigno y autolimitado de las reacciones. Consulte siempre con su alergólogo antes de eliminar grupos de alimentos o iniciar tratamientos.
Esta información es de carácter divulgativo y no sustituye la valoración alergológica individualizada.
Ante cualquier síntoma grave, acuda a su servicio de urgencias.
Autores:
Dra. María de los Angeles Gónzalez Labrador. Residente 4º año
Dra. María Dolores Alonso Díaz de Durana.
UNIDAD DE ALERGIA, HOSPITAL UNIVERSITARIO FUNDACIÓN ALCORCÓN
COMITÉ DE ALERGIA A ALIMENTOS
Bibliografía:
1. Dramburg S, Hilger C, Santos AF, de Las Vecillas L, Aalberse RC, Acevedo N, et al. EAACI Molecular Allergology User's Guide 2.0. Pediatr Allergy Immunol. 2023 Mar; 34 Suppl 28:e13854. doi: 10.1111/pai.13854. PMID: 37186333.
2. Al-Shaikhly T, Cox A, Nowak-Wegrzyn A, Cianferoni A, Katelaris C, Ebo DG, et al. An International Delphi Consensus on the Management of Pollen-Food Allergy Syndrome: A Work Group Report of the AAAAI Adverse Reactions to Foods Committee. J Allergy Clin Immunol Pract. 2024 Dec; 12(12):3242-3249.e1. doi: 10.1016/j.jaip.2024.09.037. Epub 2024 Nov 2. PMID: 39488768; PMCID: PMC11625607.
3. Kato Y, Morikawa T, Fujieda S. Comprehensive review of pollen-food allergy syndrome: Pathogenesis, epidemiology, and treatment approaches. Allergol Int. 2025 Jan; 74(1):42-50. doi: 10.1016/j.alit.2024.08.007. Epub 2024 Sep 14. PMID: 39278756.
4. Werfel T, Asero R, Ballmer-Weber BK, Beyer K, Enrique E, Knulst AC, et al. Position paper of the EAACI: food allergy due to immunological cross-reactions with common inhalant allergens. Allergy. 2015 Sep; 70(9):1079-90. doi: 10.1111/all.12666. Epub 2015 Jul 7. PMID: 26095197.
5. Skypala IJ, Hunter H, Krishna MT, Rey-Garcia H, Till SJ, du Toit G et al. BSACI guideline for the diagnosis and management of pollen food syndrome in the UK. Clin Exp Allergy. 2022 Sep; 52(9):1018-1034. doi: 10.1111/cea.14208. Epub 2022 Aug 17. PMID: 35975576.
¿Son efectivos los programas de manejo de asma en la escuela en niños y adolescentes ?
Según ha demostrado una investigación de la University College London ( Reino Unido), los niños con asma en edad escolar que reciben educación sobre cómo controlar la enfermedad tienen menos ataques, visitas a urgencias y hospitalizaciones que aquellos que no reciben esta formación.
Kneale D, Harris K, McDonald VM, Thomas J, Grigg J. Effectiveness of school-based self-management interventions for asthma among children and adolescents: findings from a Cochrane systematic review and meta-analysis. Thorax. 2019 Jan 27. pii: thoraxjnl-2018-211909. doi: 10.1136/thoraxjnl-2018-211909.
En este artículo, se analizan los datos de 33 estudios que evaluaron la eficacia de los programas de manejo del asma en la escuela, para evitar síntomas graves que pueden afectar al rendimiento escolar y a la salud. Todos estos estudios incluyeron niños con asma de 5 a 18 años que participaron en su propio entorno escolar, y asignaron al azar a un grupo de niños para que recibiera educación sobre el asma, mientras que otro grupo no la recibió.
Los programas escolares de educación fueron efectivos en reducir la frecuencia de visitas a urgencias y moderadamente efectivos en la reducción de las hospitalizaciones .
Un meta-análisis de tres de los estudios incluidos sugiere que las intervenciones de autocontrol podrían reducir el número de días de actividad restringida.
Sin embargo, el estudio no encontró conexión entre los programas de educación de asma en la escuela y el absentismo escolar.
El autor principal, Dylan Kneale asegura que “para los niños que no pueden acceder fácilmente a un médico, las escuelas pueden ser una ruta particularmente efectiva para impartir la educación en autogestionar la enfermedad”.
Los autores del artículo concluyen que “las intervenciones de autocontrol para los niños con asma administradas en las escuelas reducen el número de episodios agudos y las visitas a urgencias. El entorno escolar es un espacio importante para realizar intervenciones que mejoren la salud de los niños”.
Patricia Prieto Montaño. Servicio de Alergología. Complejo Hospitalario Universitario Albacete. Comité de Alergia Infantil SEAIC
Programas para alergólogos jóvenes
La SEAIC anuncia el lanzamiento conjunto de 3 programas para Jóvenes alergólogos, con el objeto de ofertar una formación integral y focalizados en distintos aspectos:
- Inmunoterapia – Programa ExperAIT. Límite para presentar solicitudes: 11 de mayo.
- Alergia cutánea grave – Programa REacciona. Límite para presentar solicitudes: 12 de mayo.
- Alergia a los alimentos – Programa ALiAdos. Límite para presentar solicitudes: 15 de mayo.
IMPORTANTE: Los programas son mutuamente excluyentes. En caso de participar en uno, no se podrá participar en otro, para dar oportunidades a más personas.
![]() Convocatoria programa ExperAIT (2260 descargas )
Convocatoria programa ExperAIT (2260 descargas )
![]() Agenda programa ExperAIT (2275 descargas )
Agenda programa ExperAIT (2275 descargas )
![]() Convocatoria programa REacciona (2404 descargas )
Convocatoria programa REacciona (2404 descargas )
![]() Convocatoria programa ALiAdos (2857 descargas )
Convocatoria programa ALiAdos (2857 descargas )
Escombroidosis
Lo que puede parecer una alergia a pescado pero no serlo
En los últimos meses hemos visto publicaciones de varios casos de intoxicaciones alimentarias con pescados en algunos comedores escolares, desde el Comité de Alergia a Alimentos de la SEAIC consideramos conveniente aclarar algunos conceptos que han sido empleados como “sinónimos” en algunos medios de comunicación sin serlo realmente.
Los peces pertenecientes a la familia de los escómbridos, entre los que se encuentran el atún blanco, el atún rojo, el bonito o la caballa, tienen un elevado contenido en histidina. Si estos peces o pescados ya cocinados no se mantienen en condiciones adecuadas de conservación y refrigeración, la musculatura de los mismos sufre una descomposición bacteriana que transforma la histidina que contienen en histamina. La histamina es la sustancia o mediador que se libera en la reacciones de alergia mediante un mecanismo inmunológico. De este modo su presencia en el pescado que se va a ingerir puede dar cuadros que parezcan una reacción alérgica sin realmente serlo.
Característicamente pueden producir enrojecimiento o flushing, cefalea, diarrea, palpitaciones e incluso hipotensión. Por todo ello el origen de los síntomas (intoxicación versus alergia) puede ser confuso en ocasiones. Sin embargo hay algunos detalles que pueden ayudar a diferenciarlos:
1-. En el caso de la escombroidosis la histamina se encuentra en el pescado, lo que hace que cualquiera que lo consuma pueda presentar los síntomas que acabamos de mencionar. Por ello, es frecuente que aparezcan varios casos simultáneos o cercanos en el tiempo. En lo que a alergia se refiere, el origen de la liberación de histamina es el propio individuo, de manera que la aparición de clínica “colectiva” es rara.
2.- En personas susceptibles la alergia a pescado puede aparecer frente a cualquier especie, mientras que la escombroidosis sólo sucede con el consumo de las especies que contienen elevadas cantidades de histidina.
3-. En la escombroidosis los síntomas raramente ponen en peligro la vida. En contraposición, la alergia puede producir desde síntomas leves a otros de mayor severidad, que precisen tratamiento urgente.
4-. Ante un caso de alergia a pescado es preciso realizar una eliminación adecuada de la especie o especies origen de la clínica. Sin embargo, tras un episodio de escombroidosis se podría volver a consumir el mismo pescado siempre y cuando éste haya pasado antes por unas adecuadas condiciones de conservación y refrigeración, tal y como exige la Normativa sobre manipulación de alimentos.
Con todo esto sólo queremos recordar que en lo que a la alergia al pescado se refiere, ser y parecer no es lo mismo, y que llamar a cada cosa por su nombre es importante porque el tratamiento y las medidas de evitación difieren.