resultados de la búsqueda: asma/profesionales/aviso-importante/wp-content/uploads/logos/Hospital Universitario Fundación Jiménez Díaz
Acta Reunión Comité Alergia Cutanea Valencia 2018
![]() Contenido disponible sólo para socios.
Contenido disponible sólo para socios.
Angiodema hereditario
Seguimiento del angioedema hereditario
Requisitos
- Diagnóstico previo de angioedema hereditario confirmado por un especialista.
- Disposición de teléfono, sistema de videoconsulta y de envío de imágenes. Disposición de Internet. El paciente ha de entender el sistema de funcionamiento de la aplicación empleada.
- No sufrir ninguna discapacidad que impida usar ninguno de estos sistemas.
- El paciente menor de 16 años debe estar acompañado por un progenitor o persona responsable.
- Consentimiento verbal o escrito del paciente o tutor legal, que debe reflejarse en la historia clínica. Actualmente la normativa no exige el consentimiento por escrito.
- Aceptar unas condiciones de legales y de privacidad de datos acorde a la normativa vigente.
Fase de preparación
- Fecha y hora de la visita.
- Si precisa: cuestionarios de evaluación de calidad de vida para angioedema, con instrucciones para su cumplimentación y para disponer, en el momento de la consulta, de ellos ya cumplimentados.
- Valoración de pruebas complementarias, si estas han sido solicitadas en la visita anterior.
Esta fase puede estar dirigida a una visita de revisión ya programada o a una visita solicitada por el propio paciente para resolver dudas o abordar una reagudización de la enfermedad o preparar futuros momentos que supongan un aumento de riesgo, como intervenciones o viajes.
Consulta telemática
Se realiza mediante llamada telefónica o plataforma para videoconsultas. Se aconseja realizar consultas síncronas aunque la disposición de consultas asíncronas puede ayudar a mejorar la accesibilidad del sistema y su usabilidad para el paciente. Durante el desarrollo de la consulta se abordarán los siguientes aspectos:
Introducción
Presentación y recordatorio del motivo de la consulta de seguimiento.
Evaluación del estado actual
- Preguntar por la frecuencia de brotes, áreas afectadas y gravedad de las crisis desde la última consulta.
- Investigar si ha habido algún desencadenante identificable o pródromos en las crisis.
- Preguntar por la duración y respuesta al tratamiento de rescate de los episodios. Preguntar cuántos episodios precisaron tratamiento en algún centro médico y cuántos se resuelven en domicilio.
- Los episodios ¿han tenido repercusión en actividades diarias o laborales?
- Indagar sobre el uso correcto del medicamento de rescate: ¿qué intervalo temporal existió entre el inicio de los síntomas y la administración del medicamento de rescate?
Valoración de pruebas complementarias en caso de haberse solicitado previamente
Comentar los resultados de analíticas y pruebas de imagen, si estas se habían solicitado en anterior consulta.
Revisión de medicación de mantenimiento a largo plazo
- Confirmar la adhesión al tratamiento prescrito. ¿Ha olvidado alguna dosis del tratamiento de control a largo plazo?
- Preguntar por posibles efectos secundarios del mencionado medicamento, o por nuevas afecciones aunque a priori no tengan una relación causal aparente con el medicamento pautado. (Ante la supuesta aparición de efecto adverso por el medicamento empleado, comunicar a farmacovigilancia).
- Discutir cualquier cambio en la dosis o la necesidad de ajustes en la medicación.
Educación y asesoramiento
- Ofrecer consejos sobre medidas de autocuidado, identificación de desencadenantes y estrategias para evitarlos.
- Aclarar cualquier duda o preocupación del paciente sobre su condición y tratamiento.
Plan de manejo consensuado
- Establecer un plan de acción para manejar futuros ataques, incluida la instrucción en el uso del medicamento de rescate.
- Recordar las señales de alarma que requieren atención médica inmediata.
- Confirmar la disponibilidad de medicamentos y recursos en caso de nuevo episodio. Actualizar receta electrónica.
Seguimiento y programación de citas
- Programar la próxima consulta de seguimiento o cualquier prueba complementaria necesaria.
- Confirmar la disponibilidad de apoyo continuo de atención médica entre consultas, según disponibilidad de cada área (teléfono de contacto, consulta WhatsApp, consulta médico de primaria, etc)
Despedida
Fijar fecha de próxima cita y agendar.
Agradecer al paciente por su tiempo y colaboración.
Documentación adecuada de la consulta en la historia clínica electrónica del paciente.
Consultas asíncronas: Aunque se aconseja realizar consultas síncronas, la disposición de consultas asíncronas puede ayudar a mejorar la accesibilidad del sistema y su usabilidad para el paciente. En caso de optar por esta modalidad debe disponerse siempre de un correo electrónico seguro con dirección de correo electrónico corporativa. A través de esta vía pueden enviarse al paciente:
- Cuestionarios de calidad de vida para angioedema.
- Informes clínicos actualizados.
- Planes de tratamiento nuevos, copia de receta electrónica o receta de farmacia hospitalaria.
- Aplicaciones recomendadas.
- Copias de pruebas de imagen o de laboratorio si lo solicita el paciente.
Aplicaciones y páginas web
de apoyo a la consulta telemática en angioedema hereditario.
Recursos adicionales para pacientes
- Guía del paciente angioedema hereditario:
- Asociación española de angioedema familiar
- https://angioedema-aedaf.haei.org
Homenaje al Dr. Conde
Una vida, una ilusión…
HISTORIA DE LOS INHALADORES
La administración o aplicación de los tratamientos inhalados se conoce desde hace 4000 años en China, India y Egipto. En aquella época se administraban plantas ricas en escopolamina y en atropina (como Datura stramonium o Atropa belladona) en forma de vahos, fumigaciones, pipas de agua e incluso “cigarrillos terapéuticos” por su efecto relajante en el músculo bronquial.
La terapia inhalada comienza en los balnearios en el s.XIX cuando empiezan a utilizar las nebulizaciones para tratar la tuberculosis. En 1856, el médico Sales-Girons desarrolló el primer inhalador portátil lo que permitió la administración en domicilio. Aunque estos aparatos tuvieron detractores que los consideraban ineficaces, se siguieron desarrollando nuevos modelos. Si bien, en la farmacología el interés de la vía respiratoria fue en aumento sobre todo cuando se aisló la molécula de adrenalina en 1901 por Thomas Aldrich y Jokichi Takamine y cuando Bullying desarrolló un nebulizador con motor eléctrico. Los siguientes avances se dieron en conseguir broncodilatadores con menos efectos adversos y aparatos más pequeños que generaran partículas inferiores a 5 micras.
De esta forma, gracias a los avances en farmacología se consiguió identificar los receptores α y β adrenérgicos en 1947 y posteriormente, los β1 y β2 lo que dio lugar al descubrimiento en 1969 de un broncodilatador específico con mínimos efectos cardiovasculares y musculares, el salbutamol.
En 1948 se comercializó una primera versión de los futuros dispositivos de inhalación Aerohaler®. Era un vial de vidrio donde se colocaba el principio activo en forma de polvo seco la cantidad que en cada situación se consideraba adecuada y el paciente aspiraba a través de una pieza desmontable, por la boca o por la nariz. Este dispositivo fracasó ya que las dosis administradas eran variables, cada persona utilizaba la dosis que le parecía bien, además los asmáticos que lo utilizaban no eran capaces de generar el flujo suficiente para mover el fármaco y quedaba casi todo en el vial. Cuando se inhalaba por la nariz, la función de filtro de las fosas nasales hacía que no llegara el fármaco hasta el árbol bronquial, por lo que desde entonces se desechó la aplicación nasal.
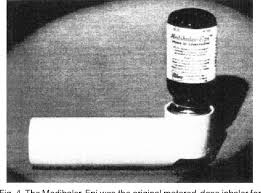
El primer inhalador de cartucho presurizado surgió en el año 1956, a raíz de la insistencia de la hija asmática del doctor George Maison que le solicitaba un inhalador cómodo y portátil. Éste tenía un mecanismo valvular para dispensación de fluidos por medio de un propelente. Con el tiempo sería empleado en medicina pero también en cosmética (desodorantes, espuma de afeitar, etc) le denominaron Medihaler. Su éxito fue inmediato. Era un aparato ligero, portátil y que siempre administraba dosis fijas que venían medidas de fábrica. Su inicio de acción era rápido y cómodo de usar en cualquier lugar. Su principal desventaja era la coordinación de la inspiración con la activación del aparato.
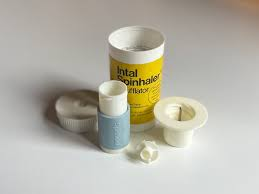
El origen de los inhaladores de polvo seco va unido al descubrimiento, por el médico Roger Altounyan, del cromoglicato disódico como protector del broncoespasmo por su acción relajante sobre el músculo liso. Debido a ello, en 1967 se lanzó al mercado el primer inhalador de polvo seco, Spinhaler® diseñado específicamente para administrar el cromoglicato disódico. Este dispositivo aportó dos grandes avances:a) administración de dosis fijas, por medio de una cápsula que se introducía en el dispositivo y se perforaba para liberar el polvo al inhalar; y b) no se planteaba como una medicación de rescate sino como una “profilaxis”. Spinhaler® ha dado lugar a toda la familia de inhaladores de polvo seco. Y además aportaba la ventaja frente al inhalador de cartucho presurizado de no tener que coordinar la inhalación con la función del aparato. Sus desventajas es que precisan mayor flujo inspiratorio y su uso puede ser complejo en personas mayores o con deformidad en las manos.
En los años 70 llegaron las cámaras espaciadoras/inhalatorias, permitiendo llevar los beneficios del cartucho presurizado a pacientes con dificultad para coordinar la maniobra.
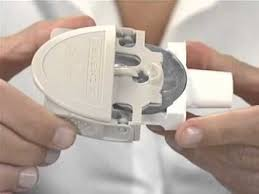
En los años 80 aparecieron los inhaladores de polvo seco multidosis, Diskhaler®. Esto reducía la complejidad y dificultad de la maniobra ya que las cápsulas con el polvo seco vienen integradas en el dispositivo y sólo hace falta cargarlas e inhalar. Aunque siguen precisando de alto flujo inspiratorio por parte del paciente y no se pueden acoplar a una cámara espaciadora al igual que los dispositivos de polvo seco unidosis.
A partir de estas familias de inhaladores, (cartuchos presurizados, inhaladores de polvo seco unidosis y multidosis) han ido surgiendo diferentes sistemas modernos que reutilizan la idea original y añaden mejoras como contadores de dosis, sistemas de feedback para que el paciente realice correctamente la técnica inhalatoria, etc.
Desde 1997 se conocen los inhaladores de vapor suave (Respimat®), en el que el fármaco en disolución es propulsado por un efecto de muelle, sin propelentes. Esto permite una maniobra inhalatoria sencilla, con una capacidad inspiratoria baja o muy baja, que unido a su producción de partículas muy pequeñas alcanza un gran depósito pulmonar. De todas maneras este sistema no llegó a España hasta 2010.
Otras variantes del cartucho presurizado clásico que han aparecido después han sido los sistemas Alvesco® y Modulite® donde el fármaco está disuelto, en vez de en suspensión, produciendo partículas muy finas y permitiendo una penetración pulmonar mayor. A su vez los sistemas accionados por la inspiración, Autohaler®, Easy Breath ® perciben el momento en que el paciente realiza la inspiración y se activan para propulsar el fármaco. Aunque este sistema no se ha comercializado en España.
BIBLIOGRAFÍA
- Las 4 reglas de la terapia inhalada.
- https://www.agefec.org/web/wp-content/uploads/2013/03/INFORMACI%C3%93N-ESCRITA-TALLER.pdf
- GEMA inhaladores. Terapia inhalada: fundamentos, dispositivos y aplicaciones prácticas. 2018
Hospital Clínic I Jornada Alergia Alimentaria y Anafilaxia
Avalada por SEAIC: el 14 de febrero de 2025 tendrá lugar en el Hospital Clínic de Barcelona la I Jornada de Alergia Alimentaria y Anafilaxia.
![]() Programa Hospital Clínic I Jornada Alergia Alimentaria y Anafilaxia (1163 descargas )
Programa Hospital Clínic I Jornada Alergia Alimentaria y Anafilaxia (1163 descargas )
Premios europeos a la Sección de Alergología del Hospital Niño Jesús
La Sección de Alergología del Hospital Infantil Universitario Niño Jesús de Madrid ha ganado dos premios en el 30th Congress of the European Academy of Allergy and Clinical Immunology (Estambul 2011), con motivo de sus trabajos sobre inmunoterapia oral en niños alérgicos a la leche.
“La quimioterapia puede dar alergia. Los alergólogos podemos ayudar a que los pacientes la vuelvan a tolerar si la necesitan”
La alergia a la quimioterapia, al igual que la alergia a otros medicamentos es una reacción en la cual el sistema inmunológico, que es el responsable de protegernos de agresiones externas, produce una respuesta contra un fármaco empleado para tratar el cáncer. Normalmente, las personas no deberían reaccionar a la quimioterapia, pero en determinadas circunstancias pueden presentar este tipo de respuesta.
Las reacciones alérgicas por estos fármacos generalmente son de 2 tipos:
Las reacciones inmediatas, es decir, aquellas que comienzan rápidamente tras la administración de la quimioterapia. Suelen ser graves, incluso pueden afectar varios órganos simultáneamente, en cuyo caso se trataría de una anafilaxia que es una reacción generalizada que puede poner en peligro la vida. En este tipo de reacciones los síntomas pueden incluir ronchas, picor o enrojecimiento de la piel, hinchazón de cualquier parte del cuerpo, opresión de garganta, afonía, dificultad o pitos al respirar, náuseas, vómitos, dolor abdominal, mareos, dolor de espalda, tiritonas, fiebre o desmayos.
Las reacciones tardías las cuales suelen aparecer una hora después de haber acabado el tratamiento, siendo usual que se presenten tras un tiempo superior a 6 horas. Este tipo no suele ser grave y generalmente causa erupción en la piel, episodios de hinchazón o fiebre.
En cualquier caso, el Alergólogo es el especialista que debe estudiar y confirmar la posible alergia. Si se confirma y el especialista en Oncología recomienda continuar con la misma quimioterapia (porque es la mejor línea de tratamiento para ese cáncer), el alergólogo puede realizar una desensibilización, que en muchos casos es la única forma en la que se puede volver a dar el mismo fármaco en condiciones seguras para evitar una reacción similar o más grave.
La desensibilización es un procedimiento que debe ser realizado en un ambiente hospitalario y bajo supervisión de un alergólogo experto en su ejecución. Consiste en engañar a las células responsables de la alergia (llamadas mastocitos), administrando la quimioterapia de manera gradual y en tiempos muy definidos, para que la persona tolere temporalmente el fármaco sin que desarrolle una nueva reacción alérgica.
La forma en la que se realiza una desensibilización dependerá de la vía por la que se administra habitualmente la quimioterapia, con lo cual puede ser por vía oral, subcutánea o intravenosa entre otras, pero siempre debe ser realizada por un especialista en Alergología.
Un aspecto importante de las desensibilizaciones es que solo tienen un efecto temporal, esto quiere decir, que cada vez que se necesite dar la misma quimioterapia, se deberá realizar una nueva desensibilización.
Recuerde que el Alergólogo es el único especialista formado para ayudarle con estas reacciones.
Dr. Teodorikez Wilfox Jiménez Rodríguez.
Adjunto de la Sección de Alergología.
Coordinador de la Unidad de Desensibilización a Fármacos.
Hospital General Universitario Dr. Balmis, ISABIAL, Alicante, España.
Jimenez_teorod@gva.es
Concurso Historias de Asma
La Fundación de la SEAIC lanza un concurso enfocado a los pacientes que sufren asma grave.
El objetivo del concurso es premiar a los participantes que muestren de forma creativa su «día a día con asma”.
Se valorará especialmente la positividad y espíritu de superación frente a su enfermedad.
Los interesados pueden mandarnos su trabajo en formato vídeo, relato o gráfico (foto o dibujo) antes del 17 de junio de 2022.
La dieta mediterránea: un patrimonio inmaterial que nos protege frente al asma y la alergia
La dieta mediterránea está considerada como uno de los patrones nutricionales más saludables para el mantenimiento del estado de salud. Además, el seguimiento de esta dieta es sumamente respetuoso con el medio ambiente y permite reducir el impacto medioambiental y la emisión de gases del efecto invernadero.
Lamentablemente, el estilo de vida mediterráneo se ha distanciado del patrón tradicional de alimentación debido a los fuertes cambios económicos y socioculturales de las últimas décadas. Como consecuencia de ello, se ha observado un incremento en el desarrollo de obesidad y en la incidencia de enfermedades crónicas. Este cambio no es ajeno a la patología alérgica. Recientemente, la revista Pediatric Allergy and Immunology ha publicado un estudio sobre la adherencia a la dieta mediterránea en la cohorte PARIS (Pollution and Asthma Risk: an Infant Study) y su asociación con el asma y la alergia en la edad escolar1.
¿En qué consiste la dieta mediterránea?
La dieta mediterránea es un patrón nutricional saludable basado en la ingestión de productos frescos y de temporada, principalmente de origen vegetal (frutas, verduras y hortalizas, legumbres y frutos secos) y cereales no procesados, en la que la principal fuente de proteínas de origen animal es el pescado (tradicionalmente procedente de la pesca local), moderado consumo de productos lácteos, y bajo consumo de carne y productos cárnicos.
Con esta proporción se cubren totalmente las necesidades energéticas, y estos alimentos contienen un alto porcentaje de elementos bioactivos como, por ejemplo, la fibra, las vitaminas y los polifenoles que tienen carácter antioxidante.
La adherencia a este patrón dietético se ha asociado con una menor incidencia de enfermedades cardiovasculares, ciertos tipos de cáncer, enfermedades neurodegenerativas como el Parkinson o Alzheimer y la diabetes tipo 2 2. Diversos análisis han sugerido que la dieta mediterránea podría ser un factor protector frente al asma en niños 3,4.
¿Qué es el estudio PARIS y cómo estudió el patrón alimentario de sus participantes?
El grupo francés que estudia la cohorte PARIS ha recogido datos de 3.840 niños sanos nacidos en la ciudad de París. Sus padres rellenaron cuestionarios sobre alimentación, en los que se preguntaba cada cuánto consumían los diferentes alimentos, tanto en casa como en el comedor escolar, restaurantes, etc.
Se usó el Mediterranean Diet Score (MDS) modificado para niños, incluyendo 7 alimentos beneficiosos: vegetales, legumbres, frutas y frutos secos, cereales, pescado, leche y otros derivados lácteos, y ácidos grasos insaturados. Se incluyó un alimento perjudicial: carne y procesados cárnicos, y se eliminó el alcohol.
También se utilizó el índice KIDMED, una herramienta validada para conocer la calidad y la adherencia de niños al patrón de dieta mediterránea.
A los 8 años se les realizó un control de salud, incluyendo pruebas de función respiratoria como FEV1 y FeNO.
Se analizaron los datos de 975 niños que completaron el MDS y/o el KIDMED. Dentro de las variables a analizar se incluyeron sexo, altura y peso, nivel socieconómico, edad de la madre, origen geográfico y ocupación de los padres, presencia de hermanos mayores, hábito tabáquico de la madre durante el embarazo, exposición a tabaco en el hogar, antecedentes familiares de alergia, duración de la lactancia materna, realización de actividad física, consumo de alimentos orgánicos y restricciones dietéticas, ya fueran por prescripción médica o no.
En los resultados del estudio se observó que más de la mitad de los niños tenían una adherencia moderada a la dieta mediterránea y un 10% incluso una adherencia óptima.Aproximadamente un tercio de los niños tenían una dieta de mala calidad, con baja adherencia al patrón mediterráneo.
¿Qué factores se asociaron a la adherencia a la dieta mediterránea?
El alto nivel socieconómico, la prolongación de la lactancia materna y el consumo de alimentos orgánicos se asociaron a una mayor adherencia a la dieta mediterránea. Por el contrario, la presencia de hermanos mayores se asoció a una menor adherencia.
En cuanto a la adherencia a la dieta mediterránea y su relación con asma y alergia a la edad de 8 años, los pacientes con mayor adherencia mostraron un FEV1 más alto (+52,3 ml) y un riesgo más bajo de presentar asma. También se asoció a menor incidencia de sensibilización a alérgenos. Sin embargo, no se hallaron diferencias significativas en cuanto al FeNO, la frecuencia de rinitis o la prevalencia de eccema.
¿Qué conclusiones podemos sacar para nuestros pacientes?
Desde el punto de vista biológico, los antioxidantes contenidos en vegetales y frutas (vitaminas C y E, betacarotenos, flavonoides, polifenoles, etc.) pueden tener un efecto beneficioso sobre la respuesta inmunitaria durante la infancia, e incluso jugar un papel en procesos inflamatorios crónicos como el asma.
Aunque este estudio se realizó en una población urbana y suburbana de París, dado que nuestros hábitos en España son similares las conclusiones podrían ser extensibles a nuestra población.Desde las consultas debemos promover una alimentación saludable y fomentar un patrimonio tan nuestro como es la dieta mediterránea.
Olaya Álvarez. Complejo Hospitalario Universitario de Ferrol. Comité de Alergia Infantil
Bibligrafía
- Amazouz H, Roda C, Beydon N, Lezmi G, Bourgoin-Heck M, Just J, et al. Mediterranean diet and lung function, sensitization, and asthma at school age: The PARIS cohort. Pediatr Allergy Immunol. 2021 Oct;32(7):1437-1444. doi: 10.1111/pai.13527. PMID: 33914969.
- Sofi F, Abbate R, Gensini GF, Casini A. Accruing evidence on benefits of adherence to the Mediterranean diet on health: an updated systematic review and meta-analysis. Am J Clin Nutr. 2010 Nov;92(5):1189-96. doi: 10.3945/ajcn.2010.29673. PMID: 20810976.
- Castro-Rodriguez JA, Garcia-Marcos L. What Are the Effects of a Mediterranean Diet on Allergies and Asthma in Children? Front Pediatr. 2017 Apr 21;5:72. doi: 10.3389/fped.2017.00072. PMID: 28484688
- Papamichael MM, Itsiopoulos C, Susanto NH, Erbas B. Does adherence to the Mediterranean dietary pattern reduce asthma symptoms in children? A systematic review of observational studies. Public Health Nutr. 2017 Oct;20(15):2722-2734. doi: 10.1017/S1368980017001823. Epub 2017 Aug 14. PMID: 28803594.
Reunión Foro Biológicos en Asma Grave
Coincidiendo con el XXXI Congreso de la SEAIC, el Comité de Asma celebrará su «Reunión Foro Biológicos en Asma Grave». A continuación se detalla el programa de este evento.
Curso TRIPLE Asma
Os presentamos el curso TRIPLE ASMA, patrocinado por Chiesi y Avalado por la SEAIC, un programa online avanzado diseñado específicamente para especialistas en alergología,
neumología, medicina familiar y comunitaria. Este curso se centra en la actualización de conocimientos y el desarrollo de habilidades en el manejo del asma incluyendo la utilización de la triple terapia
Link al curso: https://www.tripleasma.com/#/public/inicio
“BLOG” DEL COMITÉ DE INMUNOLOGIA CLINICA COMO FORO DE INFORMACION Y DISCUSION DE TEMAS DE ACTUALIDAD. DICIEMBRE 2011
AVANCES EN LA INICIACION Y DESARROLLO DEL ASMA BRONQUIAL
A la hora de valorar las teorías sobre la patogénesis de la alergia, aparte de la desregulación de las células T (Tr y/o predominio Th2), hay que tener en cuenta otras que cada vez están tomando mas preponderancia y que se basan en la activación de las barreras epiteliales y del tejido conectivo subyacente. Además suele estar implicada la inmunidad natural (IN) y un reconocimiento poco específico, aunque muy eficaz, de los agentes agresores por parte de las células que intervienen en la IN. En los trabajos que se citan se demuestra que como iniciador de la respuesta alérgica , pueden co-existir junto con la teoría clásica del desbalance de los linfocitos T, otras como por ejemplo, las que se basan en una desregulación de la barrera epitelial que da lugar a un procesamiento de los alérgenos que activan la cascada inmunológica y las reacciones de hipersensibilidad (1).
![]() Hace aproximadamente una década Stephen T. Holgate describió la llamada Unidad Trófica Epitelio – Mesenquimatosa (UTEM) como responsable de la activación continuada y la inflamación y remodelamiento de las vías aéreas en el asma bronquial. La activación persistente del epitelio bronquial manda señales hacia las células mesenquimatosas subyacentes aumentando sus funciones efectoras y activando los mecanismos que intervienen en la perdida de la reversibilidad del proceso inflamatorio de las vías aéreas (2).
Hace aproximadamente una década Stephen T. Holgate describió la llamada Unidad Trófica Epitelio – Mesenquimatosa (UTEM) como responsable de la activación continuada y la inflamación y remodelamiento de las vías aéreas en el asma bronquial. La activación persistente del epitelio bronquial manda señales hacia las células mesenquimatosas subyacentes aumentando sus funciones efectoras y activando los mecanismos que intervienen en la perdida de la reversibilidad del proceso inflamatorio de las vías aéreas (2).
La atopia afecta de forma creciente a una gran parte de la población en los países desarrollados, sin embargo, en la gran mayoría de los atópicos, no hay una progresión del proceso alérgico hacia el asma. Por otra parte, aunque exista un componente elevado de sensibilización hacia uno u otro alérgeno común que favorece la aparición del asma, hay que reconocer que la propia inmunoterapia específica y otros tratamientos basados en el cambio de la predominancia de una población celular T sobre otra o en el bloqueo de citocinas, no siempre se acaba de resolver el problema de la curación total de la enfermedad asmática. Existen otros factores que modulan la enfermedad y que hacen que los tratamientos mas efectivos y seguros sean los sintomáticos, pues su complejidad patogénica supone una seria dificultad para poder tratar el asma desde sus bases y fundamentos originales.
Durante esta década han aparecido diversos trabajos reforzando la idea de que no solo son los alérgenos específicos los que mantienen la continuidad del proceso sino que los agentes externos ambientales polucionantes, virus respiratorios, tabaco, drogas etc., juegan un papel muy importante en esa persistencia de la enfermedad. Producen señales a través de la UTEM que propagan y amplifican la respuesta inflamatoria y el remodelamiento del proceso inflamatorio en la submucosa.
![]() Recientemente se ha publicado un trabajo del grupo finlandés de Risto Renkonen en el Hospital Central de la Universidad de Helsinki, que culmina una serie de ellos en los que han demostrado como es realmente la interacción del epitelio con esos agentes externos, utilizando avanzada tecnología como la microscopía electrónica de alta resolución con marcaje múltiple, la espectrometría de masas, proteomica y la transcriptómica. Es muy interesante el hecho de que la interacción de la barrera epitelial con los alérgenos u otras partículas es diferente en el caso de los enfermos alérgicos y de los sujetos sanos (3). No solo hay diferencias en las estructuras del epitelio que mantienen las uniones de las células epiteliales (Holgate describió alteraciones del cemento intercelular inducido por el humo del tabaco), sino que además el movimiento de las moléculas a través del epitelio hacia las células dendríticas que las rodean en la submucosa (células presentadoras), se realiza de forma selectiva (Renkonen) y de manera diferente entre sanos y alérgicos. Esto es fundamental para transportar el antígeno procesado hacia los ganglios linfáticos regionales correspondientes y para iniciar la respuesta inflamatoria frente a los agentes externos agresores.
Recientemente se ha publicado un trabajo del grupo finlandés de Risto Renkonen en el Hospital Central de la Universidad de Helsinki, que culmina una serie de ellos en los que han demostrado como es realmente la interacción del epitelio con esos agentes externos, utilizando avanzada tecnología como la microscopía electrónica de alta resolución con marcaje múltiple, la espectrometría de masas, proteomica y la transcriptómica. Es muy interesante el hecho de que la interacción de la barrera epitelial con los alérgenos u otras partículas es diferente en el caso de los enfermos alérgicos y de los sujetos sanos (3). No solo hay diferencias en las estructuras del epitelio que mantienen las uniones de las células epiteliales (Holgate describió alteraciones del cemento intercelular inducido por el humo del tabaco), sino que además el movimiento de las moléculas a través del epitelio hacia las células dendríticas que las rodean en la submucosa (células presentadoras), se realiza de forma selectiva (Renkonen) y de manera diferente entre sanos y alérgicos. Esto es fundamental para transportar el antígeno procesado hacia los ganglios linfáticos regionales correspondientes y para iniciar la respuesta inflamatoria frente a los agentes externos agresores.
El transporte de las moléculas del alérgeno se hace por medio de las caveolas que son las estructuras responsables del transporte transepitelial y de la endocitosis de los agentes externos en el aparato respiratorio y digestivo. Están consideradas como un tipo de “balsas lipídicas” integradas en la membrana de determinadas células endoteliales y epiteliales. Son pequeñas invaginaciones en la membrana ricas en lípidos (colesterol y esfingolipidos) y proteínas del tipo de la caveolina de 21kDa. Estas estructuras tienen sus inhibidores específicos por lo que se vislumbra una nueva era en el tratamiento de la enfermedad respiratoria con esas sustancias que impiden el transporte a través de la barrera y por tanto la activación posterior de la UTEM.
Por otra parte se han realizado diferentes estudios en el epitelio nasal de los transcriptos de RNA tisulares de los enfermos alérgicos y de los controles (RNA mensajero o mRNA), que cuando se transduce a proteína nos da una idea de cómo es la situación funcional en un tejido determinado y en un momento concreto y qué proteínas se han secretado en ese lugar y a que grupo funcional pertenecen. Pues bien, en estudios realizados en pacientes y controles durante la estación del polen y en invierno se ha visto que en el epitelio nasal de los sujetos normales había 605 transcriptos relacionados con lo que serán proteínas de regulación de la respuesta inmune citocinas, factores nucleares, mediadores etc., mientras en los alérgicos existía la mitad o sea 331 transcriptos, lo que quiere decir que existe la posibilidad de que en los alérgicos puede existir una inmunodeficiencia de la respuesta inmune local (barrera epitelial) que posibilita el paso a la submucosa de los agentes agresores que activan la UTEM y dan lugar a la enfermedad asmática.
El epitelio respiratorio no es el único ejemplo de la importancia de la integridad de la barrera epitelial en la respuesta inmune inflamatoria. En el caso de la dermatitis atópica la alteración de la función de la filagrina conlleva el desarrollo de la sensibilización a determinados alérgenos por alteración de la funcionalidad de la barrera cutánea o intestinal como en el caso de la alergia al cacahuete.
1*Holgate ST: Has the time come to rethink the pathogenesis of asthma? Curr Opin Allergy Clin Immunol 2010, 10:48-53.
2*Holgate ST, Davies DE, Lackie PM, et al. Epithelial-mesenchymal interactions in the pathogenesis of asthma. J Allergy Clin Immunol 2000; 105 (2 Pt 1):193 – 204.
3*Pirkko Mattila, Sakari Joenväärä, Jutta Renkonen, Sanna Toppila-Salmi and Risto Renkonen. Allergy as an epithelial barrier disease. Clinical and Translational Allergy 2011, 1:5 doi:10.1186/2045-7022-1-5 The electronic version of this article is the complete one and can be found online at: http://www.ctajournal.com/content/1/1/5
Curso diagnóstico molecular en Hospital Valle de Hebrón
Curso de formación en diagnóstico molecular para residentes de alergología, del Hospital Valle de Hebrón (Barcelona).
II Curso de Procedimientos en Asma CAJMIR
Los días 19 y 20 de noviembre se celebrará on-line la II edición del Curso de Procedimientos en Asma, organizado por la Comisión de Alergólogos Jóvenes y MIR, junto con el Comité de Asma, con el patrocinio de GSK y ALK-Abelló.
![]() II Curso Procedimientos en Asma, día 1 (2046 descargas )
II Curso Procedimientos en Asma, día 1 (2046 descargas )
![]() II Curso Procedimientos en Asma, día 2 (2138 descargas )
II Curso Procedimientos en Asma, día 2 (2138 descargas )
Cuarto Curso Online de Procedimientos en Asma CAJMIR
Los próximos 16 y 18 de Enero de 2023 tendrá lugar el 4º Curso Online de Procedimientos en Asma CAJMIR, dirigido a médicos internos residentes de Alergología, desde MIR de segundo año, a nivel nacional; y coordinado por el Grupo de Procedimientos en Asma del Comité de Asma de SEAIC.
Más info: ![]() Curso Procedimientos en Asma CAJMIR (2305 descargas )
Curso Procedimientos en Asma CAJMIR (2305 descargas )
Proyecto FAST
Buscamos alérgicos al pescado para un ensayo clínico con una vacuna para tratar esta alergia
¿Tiene pacientes alérgicos al pescado de más de 18 años? Si es así, nos gustaría invitarlos a participar en un ensayo clínico para determinar si la inmunoterapia (vacuna para la alergia) es efectiva en la alergia a pescados.
La inmunoterapia es el único tratamiento que existe para curar la alergia. Consiste en la inyección de una dosis muy baja de alérgeno bajo la piel, que será incrementada lentamente. Antes y después del tratamiento se realizará una provocación con pescado para determinar si, tras este tratamiento, su paciente tolera sin problemas una mayor cantidad de pescado.
Este estudio se realiza en el Hospital Clínico San Carlos de Madrid, en el Hospital Universitario Reina Sofía de Córdoba, en el Hospital Regional Universitario de Málaga, y en otros 5 centros de 5 países europeos. Este ensayo clínico cuenta con la aprobación de los comités de ética de estos hospitales y de la Agencia Española del Medicamento y Productos Sanitarios (AEMPS) y se engloba dentro de un proyecto de investigación llamado FAST (Food Allergy Specific immunoTherapy) financiado por la Comunidad Europea.
Si precisa información adicional o si alguno de sus pacientes está interesado puede ponerse en contacto con los investigadores a través de las siguientes direcciones de email y teléfonos:
Hospital Clínico San Carlos, Madrid
Dra. Montserrat Fernández Rivas mariamontserrat.fernandez@salud.madrid.org
Dra. Maria Luisa Sánchez Millán mluisa.sanchezmi@salud.madrid.org
Tel: 91 330 30 10
Hospital Universitario Reina Sofía, Córdoba
Dra. Carmen Moreno Aguilar carmen.moreno.sspa@juntadeandalucia.es Tel: 677 905 267
Hospital Regional Universitario de Málaga
Dr. Miguel Blanca Gómez mblancago@gmail.com Tel: 609572992
Dra Francisca Gómez Pérez paquigomez.p@hotmail.com Tel: 677903259
¿Sabías que la alergia al polen y la alergia a los alimentos están relacionadas?

1. ¿Qué es la alergia alimentaria derivada de la alergia al polen?
El síndrome de alergia polen-alimentos (pollen-food allergy syndrome-PFAS) es una alergia alimentaria tipo I en pacientes con alergia al polen. Se produce por reactividad cruzada de proteínas (alérgenos) homólogas (similares) presentes en polen y alimentos vegetales. Aunque los síntomas suelen ser leves y limitados a la orofaringe, en casos raros pueden ocurrir reacciones sistémicas graves.
2. ¿Cuáles son los alérgenos y pólenes implicados?
La sensibilización a los alérgenos de pólenes depende de la región geográfica. En España y en el área mediterránea es frecuente la sensibilización a profilinas de pólenes de gramíneas y malezas (ej. artemisia). Otros alergenos implicados son LTP (proteínas de transferencia de lípidos) de pólenes de árboles como el plátano de sombra y giberelinas de pólenes de cipreses. En el norte y centro de Europa, los alérgenos más relevantes son las PR-10 (proteínas homólogas de Bet v 1, alérgeno mayor del polen de abedul).
3. ¿Qué alimentos dan problemas?
Los más frecuentes son frutas, verduras y frutos secos crudos, ya que las proteínas mayormente implicadas son las profilinas y PR-10, que son sensibles al calor y a los jugos gástricos. Por eso muchos pacientes toleran la versión cocida, enlatada de la fruta/verdura. En el caso de implicación de proteínas como LTP o las giberelinas, que son resistentes al calor y digestión pueden causar reacciones más graves.
| Polen sensibilizante/alérgeno | Alimentos vegetales crudos frecuentemente implicados |
| Abedul/PR-10 | Manzana, melocotón, zanahoria, apio, cereza, ciruela, pera, kiwi, cacahuete, soja, avellana. |
| Gramíneas/profilina | Melón, sandía, melocotón, tomate, kiwi, berenjena, pimiento, cacahuete, trigo, centeno. |
| Artemisa/profilina, LTP | Sandía, melón, banana, calabacín, pepino, apio, zanahoria, pimiento, brócoli, semilla de girasol. |
| Plátano sombra, olivo, melocotonero/ LTP | Melocotón, nuez, avellana, cacahuete. |
| Cipreses/giberelinas | Naranja, melocotón, cereza, granada. |
4. ¿Cuáles son los síntomas y su gravedad?
- Leves (la mayoría): picor o hinchazón en labios, lengua, paladar y garganta a los pocos minutos de comer el alimento crudo. Normalmente remiten sin tratamiento específico en menos de una hora.
- Moderados: además de los síntomas en boca, pueden aparecer estornudos, lagrimeo, urticaria, dolor abdominal o náuseas.
- Graves (muy poco frecuentes): Dificultad para respirar, vómitos, caída de la tensión y anafilaxia. Estos síntomas pueden presentarse si el alimento está concentrado (como en batidos o zumos), si existen cofactores como el ayuno, ejercicio, ciertos fármacos (antiinflamatorios no esteroideos (AINEs), inhibidores de la bomba de protones (IBP)), asma mal controlada o tras una cirugía bariátrica.
5. ¿Cómo se diagnostica?
- Historia clínica detallada: relación clara entre la ingestión de alimentos vegetales crudos y síntomas inmediatos, en una persona con alergia al polen.
- Pruebas cutáneas: prick test con pólenes y prick-prick con la fruta/verdura/fruto seco: positivo en crudo y negativo en cocido/tostado sugiere PFAS.
- Diagnóstico molecular: identificación en suero de IgE específica del alérgeno responsable de la reactividad cruzada.
6. Prevención y tratamiento:
- Educación del paciente: Informar sobre el PFAS, su naturaleza generalmente benigna y el bajo riesgo de reacciones graves; educar sobre cofactores y agravantes anteriormente mencionados.
- Evitar el alimento crudo responsable de los síntomas. No es necesario eliminar otros vegetales.
- Estrategias prácticas:
-Profilina/PR-10: Cocer la fruta/verdura. Preferir conservas, enlatados, compotas, frutos secos tostados. No triturar en batido aquello que tolera entero (el licuado concentra alérgenos).
-LTP: Pelar y lavar la fruta/verdura. Revisar etiquetas de zumos, smoothies, preparados veganos, barritas con frutos secos. - Medicación:
-Antihistamínico oral, si aparecen síntomas.
-Autoinyector de adrenalina: indicado en caso de reacciones graves/sistémicas o pacientes de riesgo (asma mal controlada, implicación de cofactores). - Inmunoterapia: La vacunación con extractos de pólenes mejora la rinitis/asma. No se recomienda la inmunoterapia específica para polen (subcutánea o sublingual) como tratamiento para PFAS, ya que no hay suficiente evidencia de su eficacia.
7. Impacto emocional y calidad de vida:
Aunque las manifestaciones suelen ser leves, el miedo a que aparezcan con comidas nuevas puede generar ansiedad, dificultad en las salidas sociales y complicaciones con dietas vegetarianas. El acompañamiento por un alergólogo es vital y ayudará a limitar exclusiones innecesarias y a mantener una alimentación equilibrada.
8. Conclusiones:
Conocer los alimentos implicados, identificar los síntomas y aplicar medidas sencillas como cocinar, evitar batidos, grandes ingestas y en algunos casos pelar frutas; permite, a la mayoría de los pacientes, llevar una vida normal.
Es importante enfatizar el carácter generalmente benigno y autolimitado de las reacciones. Consulte siempre con su alergólogo antes de eliminar grupos de alimentos o iniciar tratamientos.
Esta información es de carácter divulgativo y no sustituye la valoración alergológica individualizada.
Ante cualquier síntoma grave, acuda a su servicio de urgencias.
Autores:
Dra. María de los Angeles Gónzalez Labrador. Residente 4º año
Dra. María Dolores Alonso Díaz de Durana.
UNIDAD DE ALERGIA, HOSPITAL UNIVERSITARIO FUNDACIÓN ALCORCÓN
COMITÉ DE ALERGIA A ALIMENTOS
Bibliografía:
1. Dramburg S, Hilger C, Santos AF, de Las Vecillas L, Aalberse RC, Acevedo N, et al. EAACI Molecular Allergology User's Guide 2.0. Pediatr Allergy Immunol. 2023 Mar; 34 Suppl 28:e13854. doi: 10.1111/pai.13854. PMID: 37186333.
2. Al-Shaikhly T, Cox A, Nowak-Wegrzyn A, Cianferoni A, Katelaris C, Ebo DG, et al. An International Delphi Consensus on the Management of Pollen-Food Allergy Syndrome: A Work Group Report of the AAAAI Adverse Reactions to Foods Committee. J Allergy Clin Immunol Pract. 2024 Dec; 12(12):3242-3249.e1. doi: 10.1016/j.jaip.2024.09.037. Epub 2024 Nov 2. PMID: 39488768; PMCID: PMC11625607.
3. Kato Y, Morikawa T, Fujieda S. Comprehensive review of pollen-food allergy syndrome: Pathogenesis, epidemiology, and treatment approaches. Allergol Int. 2025 Jan; 74(1):42-50. doi: 10.1016/j.alit.2024.08.007. Epub 2024 Sep 14. PMID: 39278756.
4. Werfel T, Asero R, Ballmer-Weber BK, Beyer K, Enrique E, Knulst AC, et al. Position paper of the EAACI: food allergy due to immunological cross-reactions with common inhalant allergens. Allergy. 2015 Sep; 70(9):1079-90. doi: 10.1111/all.12666. Epub 2015 Jul 7. PMID: 26095197.
5. Skypala IJ, Hunter H, Krishna MT, Rey-Garcia H, Till SJ, du Toit G et al. BSACI guideline for the diagnosis and management of pollen food syndrome in the UK. Clin Exp Allergy. 2022 Sep; 52(9):1018-1034. doi: 10.1111/cea.14208. Epub 2022 Aug 17. PMID: 35975576.
Premios otorgados y personas premiadas Simposio Internacional Bilbao 2024
Relación de premios otorgados y personas premiadas en el Simposio Internacional de Enfermedades Alérgicas de Riesgo Vital – Bilbao del 6 al 9 de noviembre de 2024
Premio Nacional Fundación de la SEAIC Trayectoria Profesional en Investigación
Dr. Santiago Quirce Gancedo
Programa de Formación en Investigación
Subprograma de Formación de Investigadores Emergentes Parte II: entrega de diplomas 6 becas para realizar el Máster Universitario en Investigación en Medicina Clínica UMH:
• Dra. Leticia De las Vecillas Sánchez - REACCIONA: formación integral en patología cutánea para jóvenes alergólogos
• Dr. David Loli Ausejo - REACCIONA: formación integral en patología cutánea para jóvenes alergólogos
• Dr. Fco. Javier Solá Martínez - ExperAIT: formación integral en inmunoterapia con alérgenos (ita) para futuros expertos
• Dra. Paula Galván Blasco - EntusiASMAdos: formación integral en asma para jóvenes alergólogos
• Dra. Patricia Karina Mir Ihara - CURSO DE EXCELENCIA EN INVESTIGACIÓN
• Dr. Filip Skrabski - ALIADOS: formación Integral en Alergia a los Alimentos para alergólogos jóvenes.
Premio Micrófono Abierto en Investigación 2024
Investigador Principal: Dra. Paola Leonor Quan López.
CARACTERIZACIÓN TRANSCRIPTÓMICA Y PROTEÓMICA DE VESÍCULAS EXTRACELULARES EN PACIENTES CON URTICARIA COLINÉRGICA SINTOMÁTICA
Premio Profesor Alberto Oehling
- Premio: Berta Ruiz León, Ana María Navas Romo, Marisa Espinazo Romeu, Ipek Guler, Corona Alonso Díaz, Aurora Jurado Roger y Carmen Moreno Aguilar.
HELIOS-NEGATIVE REGULATORY T CELLS AS A KEY FACTOR OF IMMUNE TOLERANCE IN NONALLERGIC BEEKEEPERS
- Accesit: Sonia Gelis, Mariona Pascal, E. Fernández Caldas, E. Fernández, G. Araujo Sánchez, Joan Bartra y Antonio Valero.
USEFULNESS OF THE NASAL ALLERGEN PROVOCATION TEST IN THE DIAGNOSIS OF SHELLFISH ALLERGY
Premios a las mejores comunicaciones orales
- Andreina María Mugno Saba, Stephanie Steixner Zeballos, Paula Gutiérrez Álvarez, Sonia del Pozuelo Aparicio, Laura Manzanedo Ortega y Patricia Alloza Gómez.
UN RETO DIAGNÓSTICO: SÍNDROME DE ALFA-GAL - Marcela Rodríguez Pérez, Patricia García Robledo, Marta García Robledo, José Carlos García Ortiz y Alicia Armentia Medina.
ANGIOEDEMA HEREDITARIO Y AUTOINMUNIDAD - Gabriela Pretre, Nicola Giangrande, Francisco Carballada González, María Teresa Lizaso Bacaicoa, Ana Isabel Tabar Purroy y Sébastien Boulo.
DIPEPTIDIL PEPTIDASA IV DE VESPA VELUTINA, EL ALÉRGENO IGNORAD
Premios a las mejores comunicaciones en póster
- José Julio Laguna, Cosmin Boteanu, María Luisa Sánchez Millán, Yaiza Lorenzo del Pie, Mercedes Martínez García y Joaquín Archilla Esteban.
ESTUDIO PROSPECTIVO DE LA INCIDENCIA DE REACCIONES DE HIPERSENSIBILIDAD PERIOPERATORIA - Sofía Carreras Kàtcheff, Marta Planas Vinós, Moisés Labrador Horrillo, Victoria Cardona Dahl y Mar Guilarte Clavero.
OMALIZUMAB COMO ADYUVANTE EN LA INMUNOTERAPIA ORAL PARA ALERGIA ALIMENTARIA EN PACIENTES ADULTOS
Premios Fundación SEAIC y DIATER Laboratorios
Premio Nacional "Dr. Ricardo Palacios" a la Mejor Tesis Doctoral en Alergología
- Dra. Ana Rosado Ingelmo - EL SISTEMA DE ALERTAS DE ALERGIA A MEDICAMENTOS E INTERVENCIÓN PRECOZ PARA LA INTRODUCCIÓN DE BETALACTÁMICOS EN PACIENTES CON ALERTAS DE ALERGIA
Premio Nacional al Mejor Trabajo de Fin de Grado (TFG) en Alergología
- Dra. María Aldaba Anaut - ESTUDIO DE CORRELACIÓN ENTRE LA SUPERFICIE DE LA PÁPULA EN LOS PRICK TEST MEDIDA UTILIZANDO EL DISPOSITIVO NEXKIN DSPT® Y LA DETERMINACIÓN DE IGE ESPECÍFICA CON ALEX2®
Accesit al Mejor Trabajo de Fin de Grado (TFG) en Alergología
- Dra. Cristina Picón Jara - ESTUDIO DE LA ALTERACIÓN DE LA BARRERA EPITELIAL ORAL E INTESTINAL EN PACIENTES ALÉRGICOS A LAS PROTEÍNAS DE TRANSFERENCIA DE LÍPIDOS (LTPS)
Novartis Urtinnova Grants 2024 - Mejor Comunicación sobre Urticaria Crónica
- Carlos Sánchez Dorrego, Carolina Gómez Fariñas, Olinda Pérez Quintero, Raquel López Rodríguez, Manuel Jorge Rial Prado y Beatriz Veleiro Pérez.
ANAFILAXIA EN UNA SERIE DE PACIENTES CON URTICARIA POR FRÍO - Gabriela Aray-Moran, Sofía M. Proaño Mosquera, Sonsoles Infante Herrero, Alberto Álvarez-Perea, Paula Cabrera-Freitag y Ana Entrala Bueso.
URTICARIA A FRIGORE EN PACIENTES PEDIÁTRICOS
Programa de Becas de Investigación en Angioedema Hereditario: AEHwards 2024. Behring
PROTOBECA:
Ana Gabriela Mariño Fernández, Mariam Tawfiq Piedad, Marta Fontanillas Garmilla, Ángel José Albarracín Contreras, Pilar Andrea Ortiz Aljaro e Irene García Gutiérrez.
NUEVAS PROFILAXIS A LARGO PLAZO COMO TRATAMIENTO EN EL ANGIOEDEMA HEREDITARIO
PUBLIBECAS:
- Johana Gil Serrano, Moisés Labrador Horrillo, Anna Sala Cunill, Paula Galván Blaso, Marta Planas Vinos y Mar Guilarte Clavero
ROL DE LA INFLAMACIÓN SISTÉMICA EN PACIENTES CON DIFERENTES TIPOS DE ANGIOEDEMA - África Serrano Sánchez, Mercedes Pellin Nuevo, Rosario Cabañas Moreno, Marta Goyanes Malumbres, Teresa Caballero Molina y María Dolores Moreno Llorente
ANÁLISIS RETROSPECTIVO DEL PROGRAMA DE AUTOADMINISTRACIÓN DE FÁRMACOS PARENTERALES PARA PACIENTES CON ANGIOEDEMA HEREDITARIO EN EL HOSPITAL UNIVERSITARIO LA PAZ - Alexandre Ruiz Carrasco, Johana Gil Serrano, Paula Galvan Blasco, Marta Planas Vinos, Roger Colobran Oriol y Mar Guilarte Clavero
DESCRIPCIÓN DE CARACTERÍSTICAS CLÍNICAS Y DESENCADENANTES EN ATAQUES DE ANGIOEDEMA HEREDITARIO ASOCIADO A MUTACIONES DEL FACTOR XII DE LA COAGULACIÓN
Bec-AT Allergy Therapeutics
María José López Toro, Sira Miquel Marcó, Nerea Albert Yécora, Mireia Gómez Fernández, Albert Roger Reig y Raquel E. Sánchez Peña
RE-INFORMACIÓN PRECOZ PARA MEJORAR EL CUMPLIMIENTO DEL INICIO DE INMUNOTERAPIA CON ALÉRGENOS
Premios del Certamen de Humanidades de la SEAIC
PREMIO DE PINTURA:
Dra. Alicia Armentia Medina - Obra: Achíss
PREMIO DE POESÍA:
Dra. Ana Gabriela Mariño Fernández - Obra: Tormenta y calma
PREMIO DE RELATO CORTO:
Dr. Alfonso Calvo Alonso - Obra: La rinitis del selenita
CARAT: una herramienta validada para evaluar el control del asma y la rinitis alérgica en la práctica clínica
El Control of Allergic Rhinitis and Asthma Test (CARAT) es un cuestionario diseñado para evaluar el control simultáneo del asma y la rinitis alérgica (RA) en los pacientes, mediante una evaluación retrospectiva de cuatro semanas. Recientemente, un estudio ha realizado una revisión sistemática y un meta-análisis siguiendo las directrices de COSMIN, con el objetivo de evaluar sus propiedades psicométricas.
¿Por qué usar CARAT en la práctica clínica?
La evaluación del control del asma y la rinitis alérgica suele realizarse por separado, con herramientas como el Asthma Control Test (ACT) o el Allergic Rhinitis Control Test (ARCT). Sin embargo, dado que la mayoría de los pacientes con asma también padecen rinitis alérgica, surge la necesidad de una herramienta unificada. CARAT cubre esta brecha con 10 preguntas sobre síntomas de vías respiratorias superiores e inferiores, calidad del sueño, impacto en la actividad diaria y uso de medicación.
Propiedades psicométricas de CARAT
En esta revisión sistemática se incluyeron 16 estudios con los que se concluye que CARAT posee:
- Buena validez de contenido y una adecuada estructura factorial.
- Alta consistencia interna (α de Cronbach = 0.83).
- Alta fiabilidad (coeficiente de correlación intraclase = 0.91).
- Buena validez de constructo, con correlaciones significativas con otros PROMs (ej. ACT y ACQ-5).
- Buena capacidad de respuesta (cambio mínimo importante de 3.5 puntos).
Aplicación práctica
CARAT puede ser administrado en consulta mediante papel puesto que está validado al idioma castellano, pero también está disponible en formato digital a través de aplicaciones móviles como MASK-air y plataformas web, permitiendo un monitoreo continuo del paciente.
Conclusión
Esta revisión sistemática y meta-análisis refuerzan el uso de CARAT como una herramienta confiable para el control del asma y la rinitis alérgica en la práctica clínica habitual. Su implementación puede mejorar el seguimiento de los pacientes y facilitar decisiones terapéuticas más precisas
BIBLIOGRAFIA
Vieira RJ, Sousa-Pinto B, Cardoso-Fernandes A, et al. Control of Allergic Rhinitis and Asthma Test: A systematic review of measurement properties and COSMIN analysis. Clin Transl Allergy. 2022;12(9):e12194.
Diana Q, Abraham A, Yaicith A, Peter O, Juan T. Validation of the Spanish language version of the control of allergic rhinitis and asthma test. NPJ Prim Care Respir Med. 2022;32(1):47. Published 2022 Oct 29.
Sousa-Pinto B, Sá-Sousa A, Amaral R, et al. Assessment of the Control of Allergic Rhinitis and Asthma Test (CARAT) using MASK-air. J Allergy Clin Immunol Pract. 2022;10(1):343-345.e2.
XXIII Congreso Mundial de Asma
Estimados colegas:
Desde la Sociedad Española de Alergia e Inmunología Clínica SEAIC queremos recordaros que en menos de un mes, del 12 al 15 de marzo, se celebrará en Madrid el XXIII Congreso Mundial de Asma (WCA) organizado por la Asociación Global de Asma-INTERASMA con la colaboración científica de la SEAIC. Además informaros que a efectos de inscripción y participación se aplicarán a todos los miembros de la SEAIC los mismos beneficios que a los miembros de INTERASMA.
INTERASMA es una sociedad científica con más de 60 años de historia que, desde un concepto multidisciplinar, tiene como objetivo el estudio del asma. Entre una de sus actividades principales destaca la organización del Congreso Mundial de Asma que se realiza cada dos años en distintas ciudades del mundo. La alta calidad de sus programas científicos y educativos sobre el conocimiento del asma, colaborando con prestigiosos expertos y ponentes tanto locales como internacionales de todo el mundo, han hecho del WCA un congreso exitoso y de amplia participación.
Para mayor información, pueden visitar el sitio web del congreso: www.wca-2016.com. En nombre de SEAIC e INTERASMA es un placer invitarles a participar en el próximo Congreso Mundial de Asma que se celebrará en Madrid del 12 al 15 de marzo de 2016.
Saludos cordiales,
Prof. Joaquín Sastre Prof. G. Walter Canonica
Presidente SEAIC Presidente GAA – INTERASMA