resultados de la búsqueda: profesionales/aviso-importante/wp-content/uploads/logos/Sitio web no disponible
Comunicado oficial SEAIC en apoyo a las movilizaciones contra el borrador del Estatuto Marco
La Junta Directiva de la Sociedad Española de Alergología e Inmunología Clínica (SEAIC), que agrupa a más de 1.800 profesionales, principalmente médicos especialistas en Alergología de los ámbitos público, privado y mixto, y que tiene como objetivo velar por los intereses profesionales, formativos, docentes, investigadores y científicos de sus asociados, manifiesta su rechazo al actual borrador de modificación del Estatuto Marco del personal estatutario de los servicios de salud (Ley 55/2003) proporcionado recientemente por el Ministerio de Sanidad.
Este posicionamiento está en la misma línea de las declaraciones presentadas por la Organización Médica Colegial (OMC), la Federación Española de Sociedades Científico Médicas (FACME), los distintos sindicatos de la profesión médica y múltiples Sociedades Científicas Médicas.
La SEAIC comparte que, en su versión actual, el borrador de modificación del Estatuto Marco no refleja ni resguarda adecuadamente las particulares condiciones laborales, formativas y de responsabilidad propias de la profesión médica. Por esta razón, manifestamos nuestro rechazo y solicitamos a las autoridades competentes que revisen, negocien y modifiquen el Estatuto con el fin de garantizar el reconocimiento y la adecuada protección del colectivo médico.
Por todo ello, queremos adherirnos a las diferentes concentraciones convocadas por las organizaciones sindicales que, en contra del actual borrador y reclamando un Estatuto propio para la profesión médica, se convocan estos días en las diferentes Comunidades Autónomas, y a la convocatoria en Madrid el sábado 22 de marzo de 12:00 a 14:00, bajo el lema “Por un estatuto propio de la profesión médica y facultativa”, que saldrá de la Plaza de las Cortes, frente al Congreso de los Diputados y la sede de la Organización Médica Colegial (OMC) y que transcurrirá hasta el Ministerio de Sanidad.
La Junta Directiva de la SEAIC anima a todos los médicos y profesionales sanitarios a participar activamente en las movilizaciones en defensa de sus derechos laborales y condiciones profesionales.
En Madrid, a 10 de marzo de 2025
Junta Directiva de la Sociedad Española de Alergología e Inmunología Clínica (SEAIC)
![]() Comunicado oficial SEAIC borrador del Estatuto Marco (1563 descargas )
Comunicado oficial SEAIC borrador del Estatuto Marco (1563 descargas )
Acta de la reunión del Comité de Alergia Cutánea – Barcelona,
![]() Contenido disponible sólo para socios.
Contenido disponible sólo para socios.
Acta reunión Noviembre 2024
Alergia a medicamentos
Diagnóstico y seguimiento de alergia a fármacos
Requisitos
- Sospecha de alergia a fármacos con derivación intrahospitalaria o extrahospitalaria.
- Disposición de teléfono y/o Internet y posibilidad de servicio de grabación de voz.
- El servicio de Alergología debe disponer de una mensajería/aplicación segura para realizar envío de correo electrónico o mensaje de texto al paciente al menos 1 semana antes con: Fecha y hora de la consulta telemática.
- No sufrir ninguna discapacidad física ni psicológica que impida usar ninguno de estos sistemas.
- Correo electrónico corporativo específico para Estudio de Alergia a Fármacos, proporcionarlo al paciente y a través de este medio, con previo consentimiento verbal, solicitar envío de fotografías de las lesiones cutáneas presentadas.
- El paciente menor de <16 años puede tener un representante legal que responda al interrogatorio del evento sospechoso.
- El paciente adulto que presente alguna discapacidad puede tener un representante legal que responda al interrogatorio del evento sospechoso.
- Formato digital de consentimiento escrito para el paciente o tutor legal, que debe reflejarse en la historia clínica.
- El consentimiento verbal puede ser grabado vía telefónica si se dispone de grabador de voz.
Fase de preparación
- Acceso y revisión de historia clínica del paciente para informarnos de tratamientos actualizados e identificar los fármacos tolerados, antecedentes personales, antecedentes médicos.
- Revisión de fotografías de lesiones cutánea, tanto en la historia clínica del paciente en caso de disponer de este servicio o en el correo electrónico específico destinado a esta consulta.
- Datos a tener presente como factor de riesgo para desarrollar una reacción de hipersensibilidad a fármacos:
-
Relacionados con el fármaco y su administración:
Masa molecular, capacidad de formar uniones no covalentes con el HLA, vía de administración (la tópica produce más reacciones de hipersensibilidad que la parenteral y esta a su vez más que la oral).
Las dosis bajas y dadas de forma intermitente incrementan el riesgo de reacciones mediadas por IgE. -
Relacionados con el paciente:
Factores genéticos: asociación entre ciertos alelos del HLA y reacciones cutáneas graves (p. ej., HLA B*5701 y abacavir), asociación entre ciertas mutaciones genéticas como la de BCRA en el cáncer de ovario y las reacciones de hipersensibilidad por carboplatino, la α-triptasemia hereditaria y la mastocitosis y opiáceos, AINE, contrastes radiológicos, antihipertensivos IECA y relajantes musculares, entre otros.
- Analizaremos si estamos ante:
- Paciente de ALTO riesgo: AP de reacción grave o alta probabilidad de sufrirla: embarazadas, enfermedad cardiovascular grave, renal y/o respiratoria, mastocitosis sistémica uso de betabloqueantes.
- Paciente de BAJO riesgo: AP de reacción leve o baja probabilidad de sufrirla: AP de reacción con morfología y/o cronología inespecífica, los síntomas aislados como náuseas, vómitos, cefalea NO son señales de peligro.
Consultas asíncronas
- En caso de seguimiento se podrían utilizar mejorar la accesibilidad del sistema y su usabilidad para el paciente, siempre a través de un correo electrónico corporativo.
- Será de utilidad para valorar reacciones tardías que el paciente desee reportar.
Consulta telemática
- La primera consulta se realizará mediante llamada telefónica o plataforma para videoconsultas de manera síncrona de preferencia para dirigir la anamnesis, la sospecha de alergia fármacos puede llevar a confusión por parte del paciente y obviar datos importantes en caso de ser una consulta asíncrona.
- El uso de consultas asíncronas puede ayudar a aportar datos nuevos en las consultas de seguimiento, si las tuviera.
- Comenzaremos la consulta telemática presentándonos y realizaremos anamnesis detallada. Confeccionaremos la historia clínica y comprobaremos:
- Edad y sexo del paciente.
- Antecedentes personales o familiares de urticaria crónica y/o angioedema.
- Antecedentes de RH previas a fármacos.Cirugías previas.
- Tratamiento crónico tomando en cuenta uso crónico de antihistamínicos, IECA, betabloqueantes.
- El fármaco sospechoso, la vía de administración y dosis/días utilizado hasta presentar el cuadro sugerente de alergia a tal fármaco.
- Motivo de toma del fármaco.
- Fecha del evento sospechoso de alergia a fármacos.
- Número de episodios asociados al mismo.
- Tiempo de aparición de signos y síntomas tras toma del fármaco.
- Tratamiento utilizado para revertir los síntomas y tiempo de resolución del cuadro.
- Necesidad de asistencia en urgencias hospitalarias y/o hospitalización.
- Con los datos obtenidos realizaremos una estratificación del Riesgo según:
- Morfología de la reacción: identificaremos «señales de peligro».
- Cronología de la reacción:
Reacciones inmediatas <1h (1-6h)
- Alto riesgo: Urticaria y/o angioedema, prurito palmoplantar, genital, ótico, de cuero cabelludo, broncoespamo, edema laríngeo, anafilaxia.
- Bajo riesgo: Prurito aislado reacciones vasovagales, náuseas vómitos, diarreas, eritema y/o urticaria localizada en zona de administración parenteral, reacciones desconocidas en la infancia.
Reacciones no inmediatas: >1h (>24h)
- Alto riesgo: SSJ, PEAG, DRESS, exantema ampolloso generalizado, vasculitis, afectación órgano específicas: citopenias, hepatitis, neumonitis, enfermedades autoinmunitarias inducidas: Pénfigo ampolloso, pénfigo vulgar, lupus.
- Bajo riesgo: Exantema fijo, dermatitis de contacto, urticaria no inmediata.
- Definiremos endotipos, fenotipos y biomarcadores de las reacciones presentadas, nos podemos basar en el siguiente esquema:

- Con todos estos datos procedemos a programar estudios pertinentes y pruebas complementarias, explicaremos al paciente el tipo de estudio a realizar, tiempos probables: días, hora.
- Solicitaremos consentimiento verbal vía telefónica y posteriormente el día de la prueba se firmará el consentimiento informado.
- Se colocará la alerta de evitar el fármaco sospechoso o grupo de fármacos en historia clínica hasta culminar estudios.
- Solicitaremos en caso de ser necesario analítica sanguínea si corresponde, para la determinación de IgE específica. Ejemplo Penicilinas.
- Solicitaremos, si se dispone del test de activación de basófilos (TAB), si así lo requerimos.
- En caso de anafilaxia, solicitar la determinación en sangre de triptasa basal y comparar cifras de triptasa en el momento de la reacción, si se dispone.
- Determinación de IL-6 si está disponible.
- Dejaremos reflejado en la historia clínica las pautas de estudio alergológico programado que corresponda seguir para el día de la cita presencial.
- Estas pruebas se realizarán bajo supervisión de un alergólogo y equipo de enfermería experimentada para que el paciente pueda recibir tratamiento inmediato en caso de producirse una reacción alérgica.
- Al inicio de estudio alergológico en Hospital de Día se comprobará que no ha tomado el medicamento implicado.
- Se realizarán según el caso:
- Pruebas cutáneas intraepidérmicas, intradérmicas con lectura inmediata o tardía según corresponda o utilizar pruebas epicutáneas.
- Si procede se realizará prueba de exposición controlada (oral, endovenoso, intramuscular , subcutánea) en muchas ocasiones son imprescindibles para llegar al diagnóstico y consisten en administrar dosis pequeñas y progresivas del medicamento implicado hasta alcanzar la dosis terapéutica recomendada para el tratamiento de su enfermedad.
- En caso de confirmarse o descartarse la alergia al fármaco se realiza un informe clínico detallado que quedará reflejado en la historia clínica.
- Si el paciente requiere de manera ineludible el fármaco al que es alérgico le plantearemos a él y a su médico la posibilidad de realizar una desensibilización al medicamento.
Observaciones y bibliografía
*Esta guía pretende ser un complemento a los protocolos habituales desde la perspectiva de la telemedicina (TM) y por tanto no incide en aquellos aspectos que pertenezcan a la práctica clínica habitual en el diagnóstico y tratamiento de la alergia a fármacos.
- Patterson R, DeSwarte RD, Greenberger PA, Grammer LC. La alergia a los medicamentos y protocolos para su tratamiento. Boletín de la Oficina Sanitaria Panamericana (OSP); 106 (6), jun 1989. 1989.
- Pérez TC, editor Alergología y pandemia COVID192021: Real Academia Nacional de Medicina.
- Virginia Villarreal-González R, Canel-Paredes A, Arias-Cruz A, Fraga-Olvera A, Delgado-Bañuelos A, Agustín Rico-Solís G, et al. Alergia a medicamentos: aspectos fundamentales en el diagnóstico y tratamiento. Reporte de grupo del Colegio Mexicano de Inmunología Clínica y Alergia. Revista Alergia de Mexico. 2022;69(4).
- Cernadas JR. Alergia a Fármacos–Breves tópicos de uma enorme aventura. Sociedade Portuguesa de Alergologia e Imunologia Clínica Lisboa,, Portugal; 2023. p. 191-2.
- Su C, Belmont A, Liao J, Kuster JK, Trubiano JA, Kwah JH. Evaluating the PEN-FAST clinical decision-making tool to enhance penicillin allergy delabeling. JAMA Internal Medicine. 2023;183(8):883-5.
- De las Vecillas Sánchez L, Alenazy LA, Garcia-Neuer M, Castells MC. Drug hypersensitivity and desensitizations: mechanisms and new approaches. International journal of molecular sciences. 2017;18(6):1316.
REUNIÓN CAH 26 OCTUBRE 2013. ACTA Nº 18
![]() Contenido disponible sólo para socios.
Contenido disponible sólo para socios.
¿Puede ser preventiva la inmunoterapia con alergenos inhalantes en niños?
Las enfermedades alérgicas suponen una carga de salud que afecta a todos los grupos de edad y que pueden manifestarse temprano en la vida como dermatitis atópica, alergia alimentaria, rinitis/conjuntivitis alérgica y asma alérgica.
En una revisión bibliográfica recientemente publicada por Dwived y col.1 revisan las estrategias de prevención que se pueden implementar en cada etapa de la vida:
- Primaria: se dirige a niños, preferiblemente recién nacidos, que están en alto riesgo de desarrollar enfermedades alérgicas pero que aún no están sensibilizados. El objetivo en esta etapa es prevenir el desarrollo de sensibilizaciones y el consiguiente inicio de una enfermedad alérgica.
- Secundaria: involucra a niños sensibilizados antes de la aparición de síntomas. Este enfoque se centra en la prevención de nuevas sensibilizaciones y el inicio de nuevas enfermedades alérgicas.
- Terciaria: se dirige a niños con enfermedades alérgicas existentes. Los objetivos en esta etapa son prevenir la progresión de la enfermedad alérgica existente a otra y prevenir nuevas sensibilizaciones.
Dado que el sistema inmunológico es más plástico en la primera infancia, esta etapa se considera ideal para llevar a cabo medidas para prevenir enfermedades alérgicas. En este sentido, se han investigado los efectos preventivos de la inmunoterapia con alérgenos (AIT). La evidencia para aplicar la inmunoterapia preventiva con alérgenos (pAIT) está creciendo rápidamente, aunque aún enfrenta desafíos debido a factores relacionados con la edad y que los datos son limitados.
Esta revisión presenta un resumen actualizado de la evidencia disponible sobre aspectos preventivos de AIT con alérgenos respiratorios en nuevas sensibilizaciones, inicio y progresión de enfermedades alérgicas, así como otros efectos inmunomoduladores, centrándose particularmente en niños.
Los autores realizaron una búsqueda en PubMed, Embase y el Registro Central de Ensayos Controlados de Cochrane (CCRCT) para estudios pediátricos sobre AIT con alérgenos inhalantes. Se evaluaron 33 publicaciones de 27 cohortes. En estos informes, participaron 2952 niños y 1491 fueron tratados activamente.
Según los datos obtenidos, la prevención primaria con pAIT parece segura, aunque con resultados inciertos. En uno de los ensayos se observó una efecto preventivo para nuevas sensibilizaciones transitorio y no alérgeno-específico al final del tratamiento (pero no durante ni tras el tratamiento). La reducción en la proporción de asma solo se evidenció después de una prolongación en uno de los estudios. Por tanto, este enfoque plantea algunos retos que aclarar, incluyendo la identificación de sujetos y la optimización de la dosis y duración efectivas.
La prevención secundaria sí demostró ser viable y segura según esta revisión. En un ensayo clínico doble ciego controlado con placebo se evaluó la prevención secundaria en niños asintomáticos y sensibilizados a ácaros o polen de gramíneas. Tras dos años de tratamiento con inmunoterapia sublingual, en este estudio no se observó una prevención en nuevas sensibilizaciones y tampoco mostró datos en relación al inicio de la enfermedad alérgica. Sin embargo, se describieron efectos pro-tolerogénicos como el desarrollo de IgG específica en el grupo activo y la inducción de citoquinas reguladores: Il10 y TGF-b. Por tanto, los niños en edad preescolar sensibilizados pero asintomáticos podrían ser objeto de intervención a este nivel de prevención.
La prevención terciaria fue estudiada en 28 publicaciones. Cambios en la tasa de sensibilización fueron reportados en 13 grupos al final del tratamiento. 6 de ellos observaron protección frente a nuevas sensibilizaciones en los grupos activos. En 9 publicaciones se evidenció un efecto tras el tratamiento en desarrollo de nuevas sensibilizaciones. 4 de ellos reportaron efectos favorables, mientras que en uno se observó un incremento en nuevas sensibilizaciones en el grupo activo. En 3 de 5 cohortes hubo un efecto de la pAIT sobre la progresión de la rinoconjuntivitis alérgica. La persistencia a largo plazo de este efecto se observó en 2 cohortes. 5 estudios que analizaban parámetros inmunomoduladores reportaron efectos favorables al final y tras el tratamiento (incremento en los niveles de IgG e IgG4 específicas, citoquinas reguladoras o niveles bajos de eosinófilos). Por tanto, a nivel de prevención terciaria, los resultados sobre la eficacia de la pAIT en nuevas sensibilizaciones o la progresión de la enfermedad alérgica se describen de manera inconsistente. Los autores concluyen que evaluar la eficacia de este enfoque es complejo y requiere más ensayos, particularmente enfocados en aspectos preventivos.
Los posibles mecanismos subyacentes a la inducción de tolerancia en AIT se han observado en niveles de prevención terciaria y secundaria, pero no en el nivel primario. Para la prevención primaria, algunos autores sugirieron que la inducción de tolerancia específica de alérgeno podría requerir un paso obligatorio que implicara la activación transitoria de la inmunidad primaria. En los otros niveles de prevención (secundaria y terciaria), los posibles mecanismos tolerogénicos incluyen la regulación positiva de IgG1 e IgG 4, principalmente, pero también IgA1 e IgA2. Estos anticuerpos pueden poseer capacidad neutralizante y podrían competir con IgE por el alérgeno. También pueden prevenir la activación de mastocitos y basófilos e inducir células B, que secretan estos anticuerpos bloqueadores y son responsables de la inmunotolerancia a largo plazo. Otras respuestas celulares implican la reducción del reclutamiento de eosinófilos, la supresión de células Th2 y la inducción de poblaciones de células reguladoras (de células linfoides innatas, células dendríticas, células T y B) y respuestas de citoquinas reguladoras (IL10 y TGF β), restableciendo el equilibrio Th1-Th2.
Según los autores, los efectos diferenciales de pAIT en cada etapa del desarrollo de niños y adolescentes deben ser evaluados para identificar la ventana de oportunidad para la prevención. Enfatizan en un inicio temprano de pAIT, ya que tener como objetivo el sistema inmunológico infantil puede ofrecer beneficios preventivos más efectivos y duraderos. Tener una sensibilización, especialmente polisensibilizaciones, a la edad escolar ya eleva el riesgo de asma en la edad adulta. Por lo tanto, los niños entre 5 meses y la edad preescolar, con un riesgo alto de desarrollar alergias debido a antecedentes familiares positivos, teniendo un menor grado de sensibilización y sin síntomas alérgicos o con síntomas leves, parecerían óptimos para pAIT.
El pAIT de ácaros es el más comúnmente estudiado. A diferencia de las mezclas heterogéneas de alérgenos, la aplicación de monoterapia de ácaros para la prevención primaria mostró un efecto protector sobre el desarrollo de nuevas sensibilizaciones.
Se ha establecido que la administración de AIT debe durar 2–3 años para lograr una inmunotolerancia duradera. Se están explorando regímenes de tratamiento más cortos, aunque el valor definitivo de los mismos aún no se ha aclarado, particularmente para enfoques de prevención primaria y secundaria.
Los autores de la revisión concluyen explicando que la eficacia global de pAIT sigue sin aclararse en niños debido a la naturaleza multifactorial de los resultados. La prevención secundaria parece factible y puede inducir inmunotolerancia. La prevención terciaria usando pAIT de pólenes de gramíneas y/o árboles parece ser capaz de prevenir la progresión de rinoconjuntivitis a asma, aunque los beneficios de pAIT basada en otras fuentes de alérgenos no son concluyentes. Es necesario definir la dosis óptima de alérgenos, adyuvantes y vías de administración.
La infancia representa una ventana de oportunidad para iniciar medidas profilácticas, pero se necesitan ensayos pediátricos adicionales bien diseñados para comprender los efectos preventivos de la AIT sobre las nuevas sensibilizaciones, el inicio y la progresión de enfermedades alérgicas junto con los beneficios inmunomoduladores.
Mercedes Ramírez Hernández. Complejo Hospitalario Universitario de Cartagena.Comité de Alergia Infantil SEAIC.
Bibliografía:
1,. Varsha Dwived, Sonja Kopanja, Klara Schmidthaler, Justyna Sieber, Christina Bannert, Zsolt Szépfalusi. Preventive allergen immunotherapy with inhalant allergens in Children. Allergy. 2024;79:2065–2087. DOI: 10.1111/all.16115
Casos clínicos de residentes en Alergología
Ya está disponible el visor de casos clínicos de residentes en Alergología, donde se pueden consultar los casos presentados en 2011 así como los premios a los mejores trabajos de cada sección.
Acceda a la página desde aquí o desde el enlace de la columna central.
Disponibilidad de adrenalina en autoinyector
La Agencia Española de Medicamentos y Productos Sanitarios informa que, ante la escasa disponibilidad actual de unidades se ha hecho precisa la importación de Epipen autoinyector, disponible en los centros de dispensación de medicamentos extranjeros.
Acta Comité de Alergia Cutánea Enero 2015
![]() Contenido disponible sólo para socios.
Contenido disponible sólo para socios.
Acta Comité de Inmunoterapia 24/10/2019
Se adjunta el acta de la reunión del Comité de Inmunoterapia, celebrada en Gran Canaria el 24 de octubre de 2019.
![]() Contenido disponible sólo para socios.
Contenido disponible sólo para socios.
Acta Reunión de Comité Alergia a Himenópteros (Noviembre 2011)
![]() Contenido disponible sólo para socios.
Contenido disponible sólo para socios.
Acta Comité Alergia Cutánea Junio 2015
![]() Contenido disponible sólo para socios.
Contenido disponible sólo para socios.
ACTA Nº4
![]() Contenido disponible sólo para socios.
Contenido disponible sólo para socios.
Acta Nº 5, octubre 2014, Salamanca
![]() Contenido disponible sólo para socios.
Contenido disponible sólo para socios.
Acta 1ª Reunión Consenso Conjuntivitis Alergica
![]() Contenido disponible sólo para socios.
Contenido disponible sólo para socios.
Acta 1º Reunión Comité de Humanidades
This content is for Subscribers Users
La SEAIC y el proceso regulatorio de los medicamentos basados en alérgenos en España
Se encuentra disponible en formato «ahead of print» en Journal of Investigational Allergology and Clinical Immunology la carta al editor titulada “Position of SEAIC Concerning the Regulatory Process of Allergen-Based Medicines: A Compromise Between Quality and Availability for Allergic Patients in Spain”. En ella, la SEAIC expone su posición ante el nuevo marco regulatorio de los medicamentos basados en alérgenos en España, subrayando la importancia de compatibilizar la garantía de calidad, seguridad y eficacia con la adecuada disponibilidad de estos productos para los pacientes alérgicos. El texto revisa la legislación y las principales iniciativas europeas y nacionales en materia de armonización regulatoria, así como el papel activo de la SEAIC en colaboración con la AEMPS para garantizar el acceso a productos esenciales de diagnóstico y tratamiento.
Acta reunión 23 de octubre de 2014
![]() Contenido disponible sólo para socios.
Contenido disponible sólo para socios.
INHALADORES DE CARTUCHO PRESURIZADO O PMDI
La terapia inhalada es fundamental en el abordaje de las enfermedades respiratorias. Es una pieza clave por su comodidad, aplicación selectiva del fármaco en el órgano diana y disponibilidad de dispositivos ligeros y portátiles.
En este caso vamos a abordar el tema de los inhaladores de cartucho presurizado o pMDI.
También conocidos como pMDI (Pressurized Metered Dose Inhaler o Inhalador presurizado de dosis Medida) fueron los primeros dispositivos portátiles multidosis utilizados para inhalación de fármacos desde 1956 por Riker Laboratories.
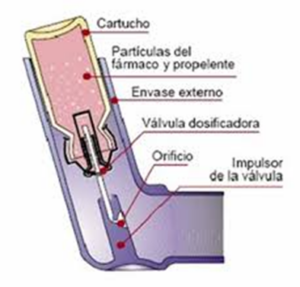
Constan de un cartucho metálico presurizado, una válvula dosificadora, una carcasa externa y una tapa de protección de la boquilla. El cartucho metálico contiene un líquido con un gas propelente donde se encuentra el fármaco disuelto o en suspensión en ese líquido. Lo rodea una carcasa de plástico y se conecta a una válvula dosificadora, de tal forma que, al presionar o activar el dispositivo, el líquido del interior se presuriza en forma de aerosol administrando una dosis fija de fármaco que contiene partículas de diferentes tamaños que salen al exterior a gran velocidad a través de una boquilla.
VENTAJAS E INCONVENIENTES DE LOS INHALADORES DE CARTUCHO PRESURIZADO
TIPOS DE INHALADORES PMDI
1.- Convencionales
- El fármaco está en suspensión o disolución
- Precisan agitar antes de su uso para homogeneizar dosis
- El tamaño de la partícula (DMMA) es entre 1-4 micras
- Tienen mayor impactación orofaríngea y menor depósito pulmonar.
- Se recomienda usar con cámara de inhalación.
- Son los más prescritos.
- Económicos.
- No disponen de contador de dosis.
2.- Partícula extrafina (Modulite® o Alvesco®)
- El fármaco se presenta en solución.
- No necesitan agitar antes de usar.
- El tamaño de partícula (DMMA) es menor de 1,5 micras que garantiza la sedimentación en vías aéreas más distales.
- Tienen menor impactación orofaríngea y mayor depósito pulmonar que los convencionales.
- El efecto freón-frío es menos frecuente.
- Disponen de contador de dosis.
3.- En co-suspensión (Aerosphere®)
- El fármaco se presenta en co-suspensión con partículas porosas de fosfolípidos que los mantienen separados y permite una dosis uniforme.
- Posibilidad de combinación de varios fármacos en el mismo inhalador consiguiendo triple terapia.
- El tamaño de partícula (DMMA) es de 3 micras, de ellas un 25% son partículas extrafinas (<1,5 micra) que garantiza la sedimentación en vías aéreas más distales.
- Tienen un contador de dosis.
4.- Activados por inspiración o BAI (K-haler®, Autohaler®, Easybreath®).
- No están comercializados en España actualmente.
- Se activan con la inhalación.
- Más simple y fácil de administrar.
- No precisan coordinar la inspiración con la pulsación.
- Tienen menor impactación orofaríngea consiguiendo mayor depósito pulmonar que los convencionales.
- No permiten extraer el cartucho ni usar cámaras de inhalación.
5.- Con sistema JET (Ribujet®)
- Cartucho presurizado con espaciador circular incorporado muy pequeño y sin válvula unidireccional.
- Equivale al uso del inhalador con cámara.
- Al inhalar el fármaco circula en espiral dentro del dispositivo.
- Disminuye el impacto orofaríngeo.
- No precisa coordinar la pulsación con la inhalación.
- Se debe agitar antes.
- En España solo se comercializa Ribujet (budesonida).
6.- Niebla fina o SMI (Respimat®)
- Híbrido entre presurizados y nebulizadores.
- El fármaco está en disolución en un cartucho sin propelentes.
- Se libera en forma de nube fina de aerosol al atravesar un filtro cuando se acciona el dispositivo. Esto reduce el impacto orofaríngeo y consiguen mayor depósito pulmonar.
- Precisan un proceso de carga del cartucho complejo.
- La coordinación pulsación-inspiración es más sencilla.
- No hay que agitar el dispositivo.
- La velocidad de salida del fármaco es más lenta que pMDI.
- Disponen de contador de dosis.
- Puede usarse con cámara.
ERRORES MÁS FRECUENTES
- No realizar una inhalación lenta y profunda (92% de pacientes)
- Falta de coordinación entre la pulsación y la inhalación (54%)
- Cese temprano de la inhalación (24 % efecto freón-frío)
- Inhalación por la nariz (12 %)
- No agitar el envase antes de su uso.
- No retirar la tapa.
- Pulsar más de una vez el dispositivo.
- Ausencia de apnea.
- Sostener el dispositivo al revés.
LIMPIEZA Y MANTENIMIENTO DEL DISPOSITIVO
- Limpiar semanalmente.
- Extraer el cartucho metálico (no sumergir en agua)
- Limpiar la carcasa de plástico y la tapa con paño húmedo o agua templada jabonosa y aclarar con agua.
- En los dispositivos que no se pueda extraer el cartucho, limpiar boquilla con paño seco.
- Debe cebarse el inhalador antes de su uso y si lleva más de 7 días sin usar. Para ello, se realizan dos o tres pulsaciones al aire.
- No exponer a temperaturas altas (>50º), ni congelar ni perforar el cartucho metálico.
BIBLIOGRAFIA
- Sorino C, Negri S, Spanevello A, Visca D, Scichilone N. Inhalation therapy devices for the treatment of obstructive lung diseases: the history of inhalers towards the ideal inhaler. Eur J Intern Med. 2020 May;75:15-18. doi: 10.1016/j.ejim.2020.02.023. Epub 2020 Feb 26. PMID: 32113944.
- Las 4 reglas de la terapia inhalada.
- GEMA inhaladores. Terapia inhalada: fundamentos, dispositivos y aplicaciones prácticas. 2018
- Sellers WFS. Asthma pressurised metered doce inhaler performance: propellant effect studies in delivery systems. Allergy Asthma Clin Immunol.2017; 13: 30.
- Giner J, Plaza V, López-Viña A, Rodrigo G, Neffen H, Casan, P. (2013). Consenso SEPAR-ALAT sobre terapia inhalada. Arch Bronconeumol. 49. 2-14. Disponible en: http://www.archbronconeumol.org/ el 09/07/2013.
Acta reunión del Comité de Himenópteros 24/10/2014
![]() Contenido disponible sólo para socios.
Contenido disponible sólo para socios.