resultados de la búsqueda: asma/wp-content/uploads/logos/Sitio web no disponible/wwwww
LAS INMUNODEFICIENCIAS ASOCIADAS A AGENTES BIOLÓGICOS INMUNOMODULADORES COMO FENOCOPIAS DE LAS INMUNODEFICIENCIAS PRIMARIAS
http://www.thehistoryblog.com/archives/14881
En nuestro sistema sanitario, las consultas de Inmunología atienden principalmente pacientes con una respuesta inmunitaria deficiente. Las inmunodeficiencias primarias (IDP) asociadas a errores innatos de la inmunidad son una causa importante de estas consultas, pero no la única. En la práctica clínica, en la mayoría de los casos, habrá que buscar una causa secundaria de la misma.
Las inmunodeficiencias primarias se incluyen bajo el concepto más global de errores innatos de la inmunidad (EII), que representa un grupo de más de 485 enfermedades definidas genéticamente (1). La inmunodeficiencia secundaria (IDS) podría definirse como una alteración transitoria o persistente de la función de las células o tejidos del sistema inmunitario, causada por factores extrínsecos al mismo (2). Estos grupos de factores incluyen agentes ambientales, malnutrición, trastornos metabólicos, uso de medicamentos inmunosupresores e inmunomoduladores, infecciones crónicas, neoplasias malignas, traumatismos graves o simplemente el envejecimiento. El enfoque inicial recomendado para la valoración de una IDS sigue las mismas directrices que en el caso de las IDP. Los hallazgos de la historia clínica, en particular los patrones de infecciones, y los hallazgos en la exploración física son esenciales para guiar la evaluación del sistema inmunitario.
Dentro de las causas de IDS, la generalización del uso de agentes biológicos inmunomoduladores para tratar enfermedades autoinmunes, inflamatorias o neoplasias hematológicas en las últimas dos décadas, se ha acompañado de un mayor riesgo de infecciones e inmunodeficiencias secundarias (3); el abordaje de este importante tema en una entrada a un blog es complicado como revisión sistemática, así que optaré por una exposición narrativa.
Examinar qué enfermedades infecciosas acompañan a una determinada inmunodeficiencia primaria ha permitido obtener información valiosa sobre los componentes del sistema inmunológico que son claves en la respuesta frente a microrganismos particulares. Gracias a ello sabemos que los defectos en moléculas críticas en la ontogenia, activación y proliferación de los linfocitos T, como las mutaciones en el gen IL2RG del cromosoma X humano, que codifica la cadena gamma común (γc) del receptor de interleucina-2 (IL-2R), o una inactivación mutación en la quinasa Jak3, que se asocia físicamente con γc, causan una depleción profunda en la función del sistema inmune, que de forma sindrómica se denomina Inmunodeficiencia combinada severa. Los defectos en el desarrollo de las células B, como la mutación en el gen que codifica una proteína tirosina quinasa llamada BTK (tirosina quinasa de Bruton), que transduce la señal a través del receptor de células pre-B, provocan deficiencias en la producción de anticuerpos que causan una incapacidad para eliminar bacterias extracelulares y algunos virus cuya eliminación eficaz requiere anticuerpos específicos.
Es instructivo considerar los defectos inmunológicos en el contexto de los principales tipos de inmunidad afectada, ya que estos pueden conducir a distintos patrones de infección y enfermedad clínica.
Las terapias biológicas no causan La inmunosupresión global característica de la terapias inmunosupresoras clásicas como los glucocorticoides, azatioprina, metotrexato o ciclosporina (4). Del mismo modo a cómo actúan las mutaciones específicas en cada IDP, las terapias biológicos se dirigen selectivamente a células y vías del sistema inmunitario para lograr efectos terapéuticos específicos, pudiéndose comportar en ciertos casos como fenocopias de la IDP original.
Por ejemplo, el OKT3 (muromonab-CD3) es un anticuerpo monoclonal IgG2 murino que se une a la cadena CD3-epsilon del complejo receptor de células T-CD3 y produce una linfopenia rápida y profunda de las células T (4). Como cabría esperar, la inmunosupresión asociada provoca una mayor susceptibilidad a las infecciones, en particular por virus herpes y bacterias. Igualmente, Alemtuzumab (anti-CD52) es un anticuerpo monoclonal humanizado utilizado para la terapia de inducción del trasplante de órganos sólidos, depletor de células T.
Basiliximab es un monoclonal contra la cadena alfa del receptor de la interleucina (IL)-2 (CD25). La activación de las células T conduce normalmente a una regulación al alza del receptor de IL-2 de alta afinidad que implica la expresión de la cadena alfa del receptor de IL-2 (CD25) que se asocia con las cadenas beta y gamma del receptor de IL-2. Basiliximab inhibe la generación de células T citotóxicas antígeno-específicas.
Las células T necesitan dos señales para activarse. La primera implica la unión directa del receptor de antígeno de la célula T (TcR) con el complejo formado por el péptido antigénico y determinadas moléculas de superficie (moléculas HLA), presentado por las células presentadoras de antígeno (APC). La segunda señal implica vías coestimuladoras específicas. El CD28 de las células T se une a sus ligandos, el CD80 (B7-1) y el CD86 (B7-2), en las APC. La presencia de ambas señales proporciona una señal de activación a las células T. Por el contrario, la molécula CTLA-4 en las células T compite por la unión a las mismas moléculas CD80/CD86, y esta interacción provoca la supresión de la activación. Abatacept y Belatacept son proteínas de fusión del dominio extracelular de CTLA-4 humano unido a una porción Fc modificada de IgG1 humana (CTLA-4-Ig), que interfieren la activación de las células T interrumpiendo la coestimulación CD28. Abatacept no obstante tiene un perfil de seguridad bien establecido en diferentes ensayos y metanálisis. Belatacept por su parte, con mayor capacidad de unión a CD80/CD86, no debe administrarse a pacientes con serología de VEB negativa candidatos a trasplante de un donante con serología VEB positiva, por el mayor riesgo de desarrollar trastornos linfoproliferativos asociados a VEB (4).
Las Janus quinasas (JAK) son una familia de tirosina quinasas no receptoras, cruciales en el desencadenamiento de las señales generadas por el receptor de diversas citoquinas y transducidas aguas abajo a través de las proteínas STAT (transductoras de señales y activadoras de la transcripción). Las STAT fosforiladas se disocian de sus subunidades receptoras y se translocan al núcleo celular para regular la transcripción génica. La familia JAK se compone de cuatro miembros: JAK1, JAK2, JAK3 y tirosina quinasa 2 (Tyk2). Tofacitinib, inhibidor JAK aprobado para la artritis reumatoide que actúa principalmente sobre JAK1 y JAK3, se ha asociado con un mayor riesgo de infección por herpes zoster (4).
Con respecto a las células B, Ibrutinib es una pequeña molécula inhibidora de la tirosina quinasa de Bruton (BTK). El ibrutinib se une a la actividad de la BTK y la inhibe de forma irreversible, impidiendo así tanto la activación de las células B como la señalización mediada por éstas. La BTK es necesaria para la señalización del receptor de células B, desempeña un papel clave en la maduración de las células B. Se han descrito casos de neutropenia e hipogammaglobulinemia. Igualmente, Idelalisib interrumpe la señalización del receptor de células B, de forma similar a ibrutinib, aunque a través de la inhibición de la isoforma delta de la fosfatidilinositol 3-cinasa. Idelalisib se asocia a un aumento de las infecciones oportunistas (4). Belimumab por su parte, es un anticuerpo monoclonal humano que se une al BlyS humano soluble e inhibe su actividad biológica. Está aprobado para el tratamiento de pacientes con LES. La celulitis y la neumonía son las infecciones graves más frecuentes (4).
Pero sin duda, la familia de biológicos con más impacto en la casuística de las consultas de inmunodeficiencias son los anti CD20 y en particular, rituximab. Este anticuerpo monoclonal quimérico (Ig)G1 CD20 específico actúa sobre las células B desde la fase pre-célula B hasta la fase pre-célula plasmática. Rituximab agota las células B de la sangre periférica, y su normalización posterior suele requerir de seis a nueve meses o más, con una variabilidad significativa entre pacientes. Con las células B deplecionadas, la capacidad del paciente para responder a las vacunas, en particular de polisacáridos, se ve afectada. Además, es frecuente cierto grado de hipogammaglobulinemia transitoria, que en algunos pacientes es persistente y significativa clínicamente, dando lugar a infecciones que requieren profilaxis antibiótica y/o terapia sustitutiva (4).
Así, hasta un largo etcétera de terapias biológicas que actúan selectivamente sobre la vía de diferentes citoquinas (interleuquina 6, interleuquina 1, factor de necrosis tumoral alfa, interleuquinas 4 y 13, interleuquina 17), integrinas (alfa-4 integrinas, CD11 alfa), o proteínas del complemento, entre otros, bloqueando con una precisión quirúrgica el normal funcionamiento del sistema inmune.
Disponemos de evidencias y de herramientas para tratar de disminuir el riesgo de IDS asociado al uso de medicamentos biológicos. Este riesgo se debe prevenir con profilaxis antibiótica adecuada, y se debe prever mediante una planificación del programa de vacunación adaptada al tipo de defecto en la respuesta inmune descrito para el fármaco.
Igualmente, las recomendaciones en cuanto a vacunación de pacientes en grupos de riesgo, tanto centrales como de las comunidades autónomas, deberían estar actualizadas acorde a la evidencia disponible e integrar la opinión de expertos con conocimiento en el funcionamiento del sistema inmune y en el mecanismo de acción de estos fármacos.
REFERENCIAS
- Tangye SG, Al-Herz W, Bousfiha A, Cunningham-Rundles C, Franco JL, Holland SM, Klein C, Morio T, Oksenhendler E, Picard C, Puel A, Puck J, Seppänen MRJ, Somech R, Su HC, Sullivan KE, Torgerson TR, Meyts I. Human Inborn Errors of Immunity: 2022 Update on the Classification from the International Union of Immunological Societies Expert Committee. J Clin Immunol. 2022 Oct;42(7):1473-1507. doi: 10.1007/s10875-022-01289-3. Epub 2022 Jun 24. PMID: 35748970; PMCID: PMC9244088.
- Tuano KS, Seth N, Chinen J. Secondary immunodeficiencies: An overview. Ann Allergy Asthma Immunol. 2021 Dec;127(6):617-626. doi: 10.1016/j.anai.2021.08.413. Epub 2021 Sep 3. PMID: 34481993.
- Cannon L, Pan A, Kovalick L, Sarkissian A, Wu EY. Secondary immunodeficiencies and infectious considerations of biologic immunomodulatory therapies. Ann Allergy Asthma Immunol. 2023 Jun;130(6):718-726. doi: 10.1016/j.anai.2023.02.010. Epub 2023 Feb 18. PMID: 36801438; PMCID: PMC10247415.
- https://www.uptodate.com/contents/secondary-immunodeficiency-induced-by-biologic-therapies (acceso abril/2024).
JIACI vol 23 num 2
Disponible el último examen de evaluación on-line del programa de Formación Médica Continuada del Journal of Investigational Allergology and Clinical Immunology.
Actas de las últimas reuniones
![]() Contenido disponible sólo para socios.
Contenido disponible sólo para socios.
Programa preliminar SEAIC 2017
Ya se encuentra disponible el programa preliminar del Simposio Internacional de Aerobiología, Contaminación y Cambio Climático, que tendrá lugar en Murcia entre el 26 y el 28 de octubre de 2017.
![]() Programa preliminar SEAIC 2017 (3488 descargas )
Programa preliminar SEAIC 2017 (3488 descargas )
![]() Boletín de inscripción SEAIC 2017 (2256 descargas )
Boletín de inscripción SEAIC 2017 (2256 descargas )
![]() Boletín de alojamiento SEAIC 2017 (1993 descargas )
Boletín de alojamiento SEAIC 2017 (1993 descargas )
Debate «INTEGRA»

El pasado martes 28 de Septiembre tuvo lugar el evento de presentación del manuscrito correspondiente al proyecto INTEGRA, que contó con el aval de SEAIC. En él, los autores del manuscrito, todos ellos miembros de SEAIC y expertos en diagnóstico molecular, presentaron el proyecto y sus conclusiones y discutieron acerca del eje vertebrador de INTEGRA: la relevancia del uso las ratios de IgE en el diagnóstico alergológico. El evento fue seguido en directo por más de 220 profesionales del diagnóstico alergológico que enriquecieron el debate con diferentes preguntas respecto al uso de ratios.
Puede visualizar la grabación del debate en https://integradebateonline.com/grabacion.
El manuscrito se encuentra disponible para su descarga en https://onlinelibrary.wiley.com/doi/full/10.1002/clt2.12052.
ACTA REUNION COMITE HIMENÓPTEROS SALAMANCA 2014 (ACTA 19)
![]() Contenido disponible sólo para socios.
Contenido disponible sólo para socios.
ACTA REUNION COMITE DE HIMENOPTEROS 26 FEBRERO 2015 (ACTA 20)
![]() Contenido disponible sólo para socios.
Contenido disponible sólo para socios.
Acreditación docente del profesorado universitario
Seminario online.
Acreditación docente del profesorado universitario: ¿Por qué y cómo acreditarse por la ANECA?
 Grabación del seminario solo disponible para socios:
Grabación del seminario solo disponible para socios:
Si no lo ha hecho, identifíquese aquí
Fecha y hora: miércoles 22 de mayo a las 16 horas.
Duración estimada: 60 minutos.
Se puede hacer preguntas.
Impartido por:
María Alecha, Unidad de bibliometría, Universidad de Navarra.
Moderadores:
Dra. Marta Ferrer, catedrática. Decana de la facultad de medicina de la Universidad de Navarra.
Dra. Carmen D’Amelio, profesora colaboradora Universidad de Navarra.
- Para cualquier consulta diríjase a la secretaría técnica de la Fundación de la SEAIC: silvina.wenk@seaic.org
Para no perderte ninguna actualización, ¡recuerda inscribirte!
Acta Reunión CAH 21 octubre
Acta Comité de Humanidades 24/10/2019
Se adjunta el acta de la reunión del Comité de Humanidades, celebrada en Gran Canaria el 24 de octubre de 2019.
![]() Contenido disponible sólo para socios.
Contenido disponible sólo para socios.
Acta del II Curso de Metodología para un Plan de Calidad en Alergia
![]() Contenido disponible sólo para socios.
Contenido disponible sólo para socios.
Votación electrónica
Apreciados socios:
Desde hoy 5 de septiembre y hasta el domingo 5 de octubre (incluido), está abierto el sistema de votación electrónica para elegir la sede al congreso de la SEAIC de 2016. Para poder votar tenéis que acceder a la parte restringida a profesionales del portal Seaic y veréis un banner en el centro, superior, que os llevará a la página de la votación (enlace directo aquí). Podréis acceder antes de emitir vuestro voto a un documento de presentación y un vídeo de sendas candidaturas (Murcia y San Sebastián).
Os recordamos que, además, estará disponible la votación en sala el día de la Asamblea de socios en el congreso de Salamanca (viernes 24 de octubre), para aquellos que no hayan emitido su voto por vía electrónica.
Nos vemos en Salamanca.
Un cordial saludo,
Dr. Pedro Ojeda
Secretario de la Junta Directiva de la SEAIC
Acta Comité Aerobiología 25/10/2018
Se adjunta el acta de la reunión del Comité de Aerobiología celebrada en Valencia el 25 de octubre de 2018.
![]() Contenido disponible sólo para socios.
Contenido disponible sólo para socios.
JIACI Vol 24 num 4
Ya está disponible el último examen de evaluación on-line del Journal of Investigational Allergology and Clinical Immunology.
Convocatoria Asamblea de socios Ordinaria y Extraordinaria
![]() Contenido disponible sólo para socios.
Contenido disponible sólo para socios.
La SEAIC en redes sociales
La SEAIC ha retomado su actividad en el canal social Twitter, sumando así un nuevo escenario para el intercambio de información y diálogo sobre las actividades de la Sociedad.
Además, con motivo de la Semana Mundial de la Alergia, se ha abierto una página en Facebook que será la plataforma para el “consultorio online» disponible durante esta semana.
¿Te van a realizar unas pruebas cutáneas o a alguien de tu entorno? Eres enfermer@ y te han asignado el servicio de alergia, en algún momento nos podríamos ver en esta situación…
Aquí tienes unos tips que te servirán de ayuda
Las pruebas cutáneas son las pruebas de primera elección por ser:
– Simples
– Rápidas
– De bajo coste
– Altamente sensibles
– Seguras
– Indoloras
¿Cómo se realizan las pruebas cutáneas?
1. Se suelen realizar en el antebrazo, aunque si no hay posibilidad se pueden realizar en
la espalda u otras localizaciones, 5 cm por encima de la muñeca y 3 cm por debajo del
codo.
2. Piel previamente limpia.
3. Identificar cada zona en las que se aplica el extracto.
4. Aplicar en la piel una gota del extracto alergénico, separadas entre sí mínimo 2-3 cm.
5. Puncionar perpendicularmente con la lanceta con un ángulo de 90o.
6. La lectura de la reacción se realizará a los 15-20 minutos.
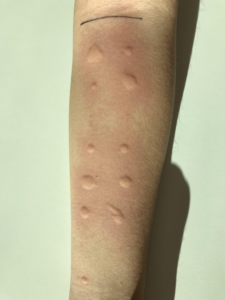
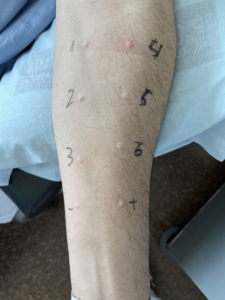
7. Dibujar el habón y eritema con un rotulador, colocar esparadrapo o cinta adhesiva de
tal forma que se transfiera a un papel.
Material
● Lancetas (metal o plástico) con una punta de 1 mm y topes laterales.
● Extracto alergénico.
● Rotulador.
● Contenedor de punzantes.
● Pañuelos de papel para secar el resto del extracto.
● Esparadrapo o cinta adhesiva.
Qué tener en cuenta
o No debe haber sangrado.
o Debe emplearse una lanceta por extracto.
o No realizar las pruebas en pacientes con síntomas alérgicos agudos.
o Tener cerca un equipo de urgencia con material y medicación disponible.
o Que la piel del paciente esté intacta.
o No deben realizarse en la piel tatuada.
o Asegurarnos que el paciente no haya tomado medicación que pueda alterar el
resultado de las pruebas.
Si soy paciente…
✔ Debo dejar de tomar los antihistamínicos entre 3-5 días para realizar las pruebas,
aunque algunos antihistamínicos necesitan más de 1 semana para su eliminación.
✔ Debe llevar por escrito la medicación habitual por si pudiera alterar los resultados.
Alergia al Látex
Publicado el documento de posición elaborado por el Comité de Alergia al Látex (2006-2010), disponible para socios registrados.
Webinar acreditación de sexenios de investigación
Webinar informativo sobre el proceso de acreditación de sexenios de investigación.
Organizado por la Comisión de Docencia de la SEAIC.
Fecha: martes 21 de enero a las 15:00 h (60 minutos de difusión). Se quedará grabado.
- Imparte Dña. María Alecha, Bibliotecaria en la Unidad de Bibliometría en Universidad de Navarra.
- Moderan las doctoras Carmen D’Amelio y Marta Ferrer (Clínica Universidad de Navarra. Universidad de Navarra).
- Enlace para la inscripción
![]() Vídeo del webinar y descarga de la presentación, disponible solo para socios:
Vídeo del webinar y descarga de la presentación, disponible solo para socios:
Si no lo ha hecho, identifíquese aquí.

