resultados de la búsqueda: asma/profesionales/wp-content/uploads/logos/wwwww/page/www.asocepa.org
Artículos de interés
Antolín-Amerigo D, Ruiz-León B, Boni E, Alfaya-Arias T, Alvarez-Mon M, Barbarroja-Escudero J, Gonzalez de Olano D, Moreno-Aguilar C, Rodriguez-Rodriguez M, Sánchez-González MJ, Sánchez-Morillas L, Vega-Castro A. Component-resolved diagnosis in hymenoptera allergy. Allergol Immunopathol 2017 Jul 21.
https://www.ncbi.nlm.nih.gov/pubmed/28739022
Alfaya-Arias T, Soriano Gomis V, Soto Mera T, Vega Castro A, Vega Gutierrez JM, Alonso LLamazares A, Antolin Amérigo D, Carballada González FJ, Domínguez Noche C, Gutierrez Fernández D, Marques Amat L, Martínez Aecediano A, Martínez San Ireneo M, Moreno Ancillo A, Puente Crespo Y, Ruiz León B, Sánchez Morillas L. Key Issues in Hymenoptera Venom Allergy: an update. J Investig Allergol Clin Immunol 2017;27(1):19-31.
https://www.ncbi.nlm.nih.gov/pubmed/28211342
Gutiérrez Fernández D, Moreno-Ancillo A, Fernández Meléndez S, et al. Insect Venom Immunotherapy: Analysis of the Safety and Tolerance of 3 Buildup Protocols Frequently Used in Spain. J Investig Allergol Clin Immunol. 2016;26(6):366-373.
https://www.ncbi.nlm.nih.gov/pubmed/27996943
Ruiz B, Serrano P, Moreno C. IgE-Api m 4 Is Useful for Identifying a Particular Phenotype of Bee Venom Allergy. J Investig Allergol Clin Immunol. 2016;26(6):355-361.
https://www.ncbi.nlm.nih.gov/pubmed/27996941
Armisén M, Guspi R, Alfaya T, et al. Cross-Sectional Validation of a Quality of Life Questionnaire in Spanish for Patients Allergic to Hymenoptera Venom. J Investig Allergol Clin Immunol. 2015;25(3):176-82.
https://www.ncbi.nlm.nih.gov/pubmed/26182683
Alfaya T, Vega A, Domínguez-Noche C, Ruiz B, Marqués L, Sánchez-Morillas L. Longitudinal Validation of the Spanish Version of the Health-Related Quality of Life Questionnaire for Hymenoptera Venom Allergy (HRQLHA). J Investig Allergol Clin Immunol. 2015;25(6):426-30.
https://www.ncbi.nlm.nih.gov/pubmed/26817139
Ruiz B, Serrano P, Verdú M, Moreno C. Sensitization to Api m 1, Api m 2, and Api m 4: association with safety of bee venom immunotherapy. Ann Allergy Asthma Immunol. 2015 Feb 27;114(4):350–2.
http://www.ncbi.nlm.nih.gov/pubmed/25736542
Armisén M, Guspi R, Alfaya T, Cruz S, Fernández S, Domínguez-Noche C, Alonso A, Gaspar D, Marqués L, Vega A. Cross-Sectional Validation of a Quality of Life Questionnaire in Spanish for Patients Allergic to Hymenoptera Venom. J Investig Allergol Clin Immunol. 2015 Jan;25(3):176–82.
http://www.ncbi.nlm.nih.gov/pubmed/26182683
Köhler J, Blank S, Müller S, Bantleon F, Frick M, Huss-Marp J, et al. Component resolution reveals additional major allergens in patients with honeybee venom allergy. J Allergy Clin Immunol. 2014 May;133:1383–9.
http://www.ncbi.nlm.nih.gov/pubmed/24440283
Golden DB. Advances in diagnosis and management of insect sting allergy. Ann Allergy Asthma Immunol. 2013;111:84-89.
http://www.ncbi.nlm.nih.gov/pubmed/23886224
Rueff F, Przybilla B, Bilo MB, et al. Predictors of side effects during the buildup phase of venom immunotherapy for Hymenoptera venom allergy: the importance of baseline serum tryptase. J Allergy Clin Immunol. 2010;126(1):105-11 e5.
http://www.ncbi.nlm.nih.gov/pubmed/20542320
Ruëff F, Przybilla B, Biló MB, et al. Predictors of severe systemic anaphylactic reactions in patients with Hymenoptera venom allergy: importance of baseline serum tryptase-a study of the European Academy of Allergology and Clinical Immunology Interest Group on Insect Venom Hypersensitivity. J Allergy Clin Immunol. 2009;124(5):1047-54.
http://www.ncbi.nlm.nih.gov/pubmed/19895993
Marques L, Vega A, Munoz E, Moreno-Ancillo A. Epidemiologic observations on Hymenoptera allergy in Spain: the Alergologica-2005 study. J Investig Allergol Clin Immunol. 2009;19 Suppl 2:51-55.
http://www.ncbi.nlm.nih.gov/pubmed/19530419
Bilo BM, Rueff F, Mosbech H, Bonifazi F, Oude-Elberink JN. Diagnosis of Hymenoptera venom allergy. Allergy. 2005;60(11):1339-1349.
http://www.ncbi.nlm.nih.gov/pubmed/16197464
Bonifazi F, Jutel M, Biló BM, Birnbaum J, Muller U. Prevention and treatment of hymenoptera venom allergy: guidelines for clinical practice. Allergy. 2005;60:1459-70.
http://www.ncbi.nlm.nih.gov/pubmed/16266376
Monsalve RI, Vega A, Marques L, et al. Component-resolved diagnosis of vespid venom-allergic individuals: phospholipases and antigen 5s are necessary to identify Vespula or Polistes sensitization. Allergy. 67(4):528-536.
Factores de riesgo para el desarrollo de asma en la edad escolar
Durante los últimos años, el estudio de los factores de riesgo que pueden influir en el desarrollo del asma ha sido un tema candente en esta enfermedad. No obstante, si hacemos una revisión exhaustiva de la literatura, los trabajos publicados hasta el momento sobre este tema en población pediátrica de nuestra área geográfica, son escasos. Es por este motivo, que desde la Unidad de Alergología Pediátrica del Hospital Universitario Vall d’Hebron, decidimos diseñar un estudio caso-control para determinar aquellos factores que podían influir en el desarrollo y la gravedad del asma. El trabajo ha sido recientemente publicado en la revista “Pediatria Catalana” (revista de libre acceso). A continuación expondré brevemente el contenido del artículo:
Los avances médicos durante las últimas décadas han permitido mejorar la clasificación etiopatogénica y el manejo clínico del asma. Pero a pesar de esto, su incidencia ha seguido en aumento, sobre todo en los países industrializados y en vías de desarrollo, convirtiéndose en un desafío médico mundial. Es obvio que un incremento de prevalencia en poblaciones genéticamente estables ha de ser consecuencia de cambios medioambientales. Por todo ello es necesario conocer aquellos factores que puedan influir en la patogenia de la enfermedad y desarrollar estrategias preventivas. De este modo, el objetivo del estudio presentado fue valorar la influencia de factores de riesgo conocidos del asma y su gravedad en una población pediátrica del área mediterránea, mediante un estudio caso-control.
Se incluyeron 107 pacientes asmáticos de edad media 9 años y predominio masculino [62,6% (n=67)] y 32 controles sanos de edad media 10 años y predominio también masculino [59,3% (n=19)]. El rango de edad fue entre 4 y 14 años en ambos grupos. Respecto a los resultados, destacar que no se encontraron asociaciones estadísticamente significativas entre el género, la edad o la gravedad del asma; pero sí que se objetivó que las edades de entre cinco y seis años fueron las que mostraron un mayor porcentaje de asma persistente.
La comparación de los factores de riesgo de desarrollo de asma con el grupo control mostró como única diferencia estadísticamente significativa el antecedente de sibilantes recurrentes los primeros 3 años de vida (p<0,001). También se objetivó una asociación estadísticamente significativa entre el asma persistente moderada o grave y los antecedentes de sibilantes recurrentes los primeros 3 años de vida (p<0,001), antecedentes de bronquiolitis por Virus Respiratorio Sincitial (VRS) (p<0,05) y antecedentes de criterios del Índice Predictivo de Asma (API) positivos (p<0,001). Estos resultados están en conjunción con otros trabajos publicados recientemente en los que relacionan las bronquiolitis y los sibilantes recurrentes el primer año de vida con estilos de vida modificables, como tener hermanos en edad escolar e ir a la guardería, del mismo modo que la guía Global Initiative for Asthma (GINA) sugiere que un niño con episodios de sibilantes recurrentes, de mayor duración e inducidos por el ejercicio, tienen una mayor probabilidad de tener asma. No obstante, estos datos contrastarían con algunos estudios publicados previamente que habían identificado las infecciones de repetición no específicas en la primera infancia como factor protector del asma.
Otro dato importante a considerar en este estudio es el peor control de la enfermedad en población asmática de 5-7 años, hecho que podría estar relacionado con una mayor repercusión de las infecciones víricas a esta edad. Del mismo modo, la sensibilización a ácaros del polvo y a epitelios se asoció también a un mal control de la enfermedad y la sensibilización a esporas de hongos se asoció a una forma más grave de asma (p<0,05). En conclusión, se debe prestar una especial atención a los niños con asma en edad escolar y antecedentes de bronquiolitis por VRS, sibilantes de repetición los tres primeros años de vida y a aquellos con sensibilización a esporas de hongos, ya que pueden presentar una forma más grave de asma que precise un seguimiento más estrecho y tratamiento más intenso.
Encontrarán el resumen del artículo en tres idiomas (catalán, español e inglés). El artículo original está íntegramente escrito en lengua catalana. Por este motivo y dada la relevancia de los datos que contiene para todos los profesionales especialistas que se dedican al campo de la alergia y el asma pediátricas y, como autora de correspondencia del mismo, he creído oportuno, hacer una traducción del artículo a lengua española para que pueda llegar a un mayor número de profesionales de la salud. Deseo pues que puedan sacar el máximo partido posible a la lectura de este artículo, desarrollado en población escolar del área del mediterránea, y, por tanto, extrapolable a buena parte de nuestro territorio.
Dra. Teresa Garriga Baraut, MD, PhD
Miembro del Comité de Alergia Infantil (CAI) de la Sociedad Española de Alergología e Inmunología Clínica (SEAIC). Facultativa Especialista Adjunta | Servicio de Pediatría/Sección de Alergia Pediátrica, Pneumología Pediátrica y Fibrosis quística/ Unidad de Alergología Pediátrica. Hospital Universitari Vall d’Hebron. Investigadora del grupo de investigación «Crecimiento y Desarrollo» VHIR Vall d’Hebron.
Estudio VAC-ASMA: percepción de la vacunación en pacientes con asma grave
El proyecto VAC-ASMA, busca conocer la actitud de los profesionales ante la vacunación en pacientes con asma grave desde las consultas de Alergología y Neumología de España.
Dirigido a especialistas que realicen labor asistencial en asma grave en hospitales españoles y cuenten con más de tres años de experiencia.
Participa: https://vacasma.gruposaned.com/
Código de acceso: ASMA
![]() Estudio VAC-ASMA (1529 descargas )
Estudio VAC-ASMA (1529 descargas )
Los inesperados riesgos del control del asma en niños.
El asma es una condición médica crónica muy común en niños y es especialmente susceptible a los cambios provocados por el COVID-19. Actualmente se dispone de poca información sobre el impacto que la pandemia COVID-19 puede tener en el control y manejo de los niños y jóvenes con asma bronquial.
El siguiente artículo “Oreskovic N, Bernard T, Aryee E, Kuhlthau K, Perrin J. The Unexpected Risks of COVID-19 on Asthma Control in Children. J Allergy Clin Immunol Pract.2020;8(8):2489-2491” revisa las influencias que han podido ser importantes o afectar en el control del asma en niños durante la pandemia de COVID-19 debido a los cambios sociales que estamos viviendo. Estos suponen cambios en el entorno, en la práctica clínica médica diaria y su gestión, y en el uso de medicación de esta enfermedad, cambios que tendrán repercusión a largo plazo en los resultados de control del asma. Además, desde nuestro Comité de Alergia Infantil se realizó una encuesta entre los especialistas para conocer cómo ha afectado la pandemia al manejo del asma pediátrico en España, que ha sido publicada en Sanchez-Garcia S, Ruiz-Hornillos J, Escudero C. Pediatric Asthma Management during the COVID-19 pandemic: Results of a national survey. Ped All Immunol Pulm. 2020 Dec; 33(4):199-203. https://doi.org/10.1089/ped.2020.1250
Los pacientes con asma tienen especial vulnerabilidad a los cambios provocados en el contexto de la pandemia COVID-19, con muchas vías y factores de riesgo compartidos, incluyendo la calidad del aire, el ambiente interior, la actividad física, el control del peso, la gestión de la medicación y la prestación de atención sanitaria.
El lugar donde los niños pasan mayor cantidad de tiempo, que ahora es en los interiores, los hábitos diarios (patrón de asistencia a clases), de viaje o transportes, y la actividad física que realizan, afectan al asma.
Además, ha habido cambios en la disponibilidad, la prestación y la utilización de la atención sanitaria que tienen importantes implicaciones para el asma y otras enfermedades crónicas que requieren atención médica continuada. Se han limitado las visitas a la consulta para el control del asma, tanto en atención primaria como especializada (Neumología y Alergología) y se han limitado las visitas a urgencias. Todo ello ha favorecido el formato de visita telefónica o videoconferencia. Estos cambios han ofreciendo nuevas oportunidades gracias a la denominada “telesalud”, que deberán ser valoradas y aprovechadas.
En cuanto a las visitas a Urgencias, se observó una importante disminución en la atención relacionada con el asma y el comienzo de la pandemia, que atiende seguramente el temor de las familias al contagio y/o las recomendaciones sanitarias del momento. Todo esto condujo además, a que la realización de las pruebas tempranas para un mejor control de la enfermedad, como las pruebas de función pulmonar, se viera afectada.
La COVID-19 también ha influido probablemente en la adherencia de los pacientes a los medicamentos controladores del asma. Los padres de los niños con asma pueden tener un mayor control y ser más vigilantes para que los niños tomen su medicación con regularidad y que una mayor adherencia a la medicación mejore el control del asma o, por el contrario, que otros dejen su medicación ante el temor de los posibles efectos de los corticoides, tanto orales como inhalados, en la infección por coronavirus.
Todos estos factores han podido influir de diferente manera en función del lugar en el que residiese el niño, de la situación socioeconómica de la familia, de las limitaciones para realizar actividad física al aire libre a causa de las restricciones particulares de cada zona, etc. En este sentido, los niños de familias de entornos urbanos con menores ingresos tienen un acceso más limitado a espacios seguros para la actividad física, tienen domicilios en los que la exposición a alérgenos/contaminantes de interior (hongos, roedores, cucarachas y el humo del tabaco, entre otros) es mayor, y pueden convivir además con adultos con menor posibilidad de teletrabajar y más expuestos a la infección por coronavirus.
Estos cambios en el entorno, en la práctica médica y en la gestión del tratamiento, tendrán probablemente un gran impacto en el asma infantil que tendremos que vigilar para evaluar su impacto final a medio y largo plazo.
Margarita Tomás Pérez. Médico Adjunto Alergología Hospital General Universitario La Paz. Madrid. Comité de Alergia Infantil SEAIC.
Comunidad Valenciana
Comunidad valenciana
Centros con actividad asistencial pública en Alergología
Alicante
Hospital de Alcoy "Virgen del los Lirios"
- http://www.a14.san.gva.es
- Polígono Caramanxell, s/n. 03804 Alcoy
- 965537400
Hospital de Orihuela "Vega Baja"
- http://www.dep21.san.gva.es
- Ctra. Orihuela-Almoradí, s/n (Ptda.S.Bart) 03314 Orihuela
- 965877500
Hospital de Villajoyosa "Marina Baixa"
- Sitio web no disponible
- Avda. Alcalde En Jaume Botella Mayor, 7. 03570 Villajoyosa
- 966859800
Hospital de Denia "Marina Salud"
- http://www.marinasalud.es
- Partida Beniadlá, s/n. 03700 Denia
- 966429000
Hospital del Vinalopó
- http://www.vinaloposalud.com
- Tónico Sansano Mora, 14. 03293 Elche
- 966 67 98 00
Hospital General de Elda "Virgen de la Salud"
- http://www.elda.san.gva.es
- Ctra. Elda-Sax. Ptda La Torreta. 03600 Elda
- 966989000
Hospital General Universitario de Alicante
- http://www.dep19.san.gva.es
- C/ Pintor Baeza, 12. 03010 Alicante
- 965933000
Hospital General Universitario de Elche
- http://www.dep20.san.gva.es
- C/ Camino de la Almazara, 11. 03203 Elche
- 966616900
Hospital de Torrevieja
- http://www.torrevieja-salud.com
- Ctra. CV-95 Torrevieja-S.Miguel de Salinas.Ptda Ceñuela. 03186 Torrevieja
- 965721313
Castellón
Hospital de La Plana
- http://www.laplana.san.gva.es
- Ctra. Villarreal-Borriana, km 0,5. 12540 Villarreal
- 964357600
Hospital Universitario General de Castellón
- http://www.castello.san.gva.es/
- Avda. Benicasim, s/n. 12004 Castellón de la Plana
- 964726500
Valencia
Consorcio Hospital General Universitario de Valencia
- http://chguv.san.gva.es
- Avda. tres Cruces, s/n. 46014 Valencia
- 961972000
Hospital Arnau de Vilanova – Valencia
- Sitio web no disponible
- C/ San Clemente, 12. 46015 Valencia
- 963868501
Hospital Clínico Universitario de Valencia
- Sitio web no disponible
- Avda. Blasco Ibáñez, 17. 46010 Valencia
- 963862600
Hospital La Ribera de Alzira
- http://www.hospital-ribera.com
- Ctra. Corbera, km. 1. 46600 Alcira
- 962458100
Hospital Lluís Alcanyís
- http://www.xativaontinyent.san.gva.es
- Crta. Xátiva-Silla, km 2. 46800 Xátiva
- 962289500
Hospital Universitario Doctor Peset
- Sitio web no disponible
- Avda. Gaspar Aguilar, 90. 46117 Valencia
- 961622300
Hospital Universitari i Politècnic La Fe
- http://www.hospital-lafe.com/
- http://www.alergialafe.org/
- Avda. Fernando Abril Martorell, 106. 46026 Valencia
- 961244083
¿Ha influido la Pandemia por Enfermedad de COVID-19 en el sueño de los pacientes pediátricos y adolescentes con asma alérgica?
Sin duda 2020 y 2021 han sido años sin precedentes debido a un hecho inesperado que descolocó por completo la vida de millones de personas: la rápida propagación del coronavirus SARS-CoV-2 por todos los continentes ocasionó la primera gran pandemia del siglo XXI, la cual tuvo un gran impactó social, económico y emocional de manera global en todo el mundo. La enfermedad por coronavirus 2019 (COVID-19), aparte de ocasionar muchos síntomas orgánicos graves como la neumonía bilateral con distrés respiratorio agudo, ha sido también la responsable de muchos síntomas neurológicos y cambios importantes en el sueño. A lo largo de estos intensos dos años, el estrés originado por la incertidumbre constante, el aislamiento social y, en definitiva, los cambios en la rutina diaria, se han acompañado de diversas alteraciones del sueño conocidas como “coronasomnia».
La Pandemia por Enfermedad de COVID-19 ha afectado a toda la población de manera global, con un impacto claramente negativo en la mayoría de los casos. Además, sabemos que hoy en día, la combinación Pandemia por Enfermedad de COVID-19 y asma es un problema vital al que nos enfrentamos tanto los profesionales de la salud como los pacientes y familiares de pacientes con asma alérgica. No obstante, el impacto que la Pandemia por Enfermedad de COVID-19 ha ocasionado en el descanso de los pacientes pediátricos y adolescentes con asma de nuestra área geográfica aún no ha sido estudiado. De aquí que hayamos estimado interesante presentar los datos del estudio realizado en la Unidad de Alergia Pediátrica del Hospital Universitario Vall d’Hebron, cuyo objetivo fue investigar cómo la Pandemia por Enfermedad de COVID-19 influyó en el sueño de pacientes pediátricos y adolescentes con asma alérgica residentes en el área mediterránea. Para lograr este objetivo se realizó un estudio piloto prospectivo que incluyó a pacientes pediátricos y adolescentes con asma alérgica persistente de entre 6 y 18 años.
Todos los participantes del estudio respondieron el Cuestionario BEARS y la Escala de Bruni. El cuestionario de BEARS1-4 es un cuestionario útil para el cribaje de trastornos del sueño en la infancia. Está dividido en cinco áreas principales del sueño, facilitando el cribado de los trastornos del sueño, en población pediátrica y adolescentes de entre 2 y 18 años. Cada área tiene una pregunta para cada grupo de edad. Una respuesta positiva en cualquiera de los aspectos obliga a una investigación más profunda. Las cinco áreas de estudio se detallan a continuación:
B= Problemas para acostarse (“bedtime problems”)
E= Excesiva somnolencia diurna (“excessive daytme sleepiness”)
A= Despertares durante la noche (“awakenings during the night”)
R= Regularidad y duración del sueño (“regularity and duration of sleep”)
S= Ronquidos (“snoring”)
Respecto a la Escala de Bruni5,6 de trastornos del sueño para población pediátrica y adolescente, decir que consta de 26 ítems valorados según una escala tipo Likert. Está diseñada para detectar trastornos del sueño divididos en seis categorías: problemas para iniciar o mantener el sueño, problemas respiratorios, desórdenes del despertar, alteraciones de la transición sueño-vigilia, excesiva somnolencia diurna e hiperhidrosis nocturna. En total, el paciente responde a 26 preguntas y proporciona una respuesta que puntúa del 0 al 4 según la clínica presente. El punto de corte a partir del cual se considera que el paciente puede presentar algún trastorno global del sueño es de 39. A continuación se define cada puntuación:
0=Nunca
1=Ocasionalmente (una o dos veces al mes o menos)
2=Algunas veces (una o dos a la semana)
3=A menudo (de tres a cinco veces a la semana)
4=Siempre (diariamente)
En total se incluyeron 77 pacientes con una edad media de 12 años. La mayoría eran pacientes del sexo femenino (62%, n=48) y veintisiete (35%) habían sido diagnosticados de Enfermedad de COVID-19. Con respecto al Cuestionario de BEARS, el 70% (n=54) de los pacientes tuvo como mínimo una respuesta positiva. Además, casi la mitad de los pacientes tenían problemas a la hora de acostarse [42% (n=32)], seguido de somnolencia diurna excesiva [34% (n=26)]. En cuanto a la Escala de Bruni, 52 de los 77 pacientes incluidos (67%) presentaban una puntuación superior a 39 puntos, hecho que indicaba trastornos del sueño entre la población de estudio. Los trastornos más prevalentes encontrados tras la evaluación utilizando la Escala de Bruni fueron los trastornos respiratorios del sueño [26 de los 77 pacientes estudiados (34%)], seguido de los trastornos de inicio y mantenimiento del sueño (30%, n = 23) y de la somnolencia diurna excesiva (24%, n=18). No se encontraron diferencias estadísticamente significativas entre los pacientes COVID-19 positivos y negativos ni en el cuestionario de BEARS ni en la escala de Bruni.
En conclusión, en este trabajo se encuentra una elevada prevalencia de trastornos del sueño en pacientes asmáticos pediátricos y adolescentes durante la pandemia debida a la Enfermedad de COVID-19. El trastorno más prevalente en esta población de estudio, evaluado mediante la Escala de Bruni, fue el trastorno respiratorio del sueño. Por tanto, es importante proporcionar a los pacientes un control óptimo de las enfermedades respiratorias para mejorar la calidad de su sueño.
La importancia del presente estudio radica en que es el primero que proporciona datos sobre la posible afectación del sueño debida al impacto de la pandemia por COVID-19 en población pediátrica y adolescente con asma alérgica en el área mediterránea. Debido a este hecho, es difícil poder comparar nuestros datos con los realizados por otros autores ya que, si bien sí que hay varios trabajos que evalúan los posibles trastornos del sueño asociados a la pandemia por COVID-19 en población de esta edad, la mayoría de ellos incluyen población sana o con trastornos neuroconductuales del sueño previos, pero sin especificar la posible concomitancia con otras patologías respiratorias asociadas, como el asma alérgica. No obstante, sí que es interesante comentar algunos trabajos que evalúan los posibles trastornos del sueño en población pediátrica y adolescentes, aunque sean poblaciones sin asma.
Ya antes de la pandemia debida a la Enfermedad de COVID-19, habían sido varios los estudios publicados que alertaban que el sueño insuficiente, la mala calidad del sueño, el insomnio, la apnea del sueño y las alteraciones de los horarios de sueño-vigilia eran manifestaciones típicas de morbilidad física y emocional en las pandemias. De este modo, no es de extrañar que los primeros estudios sobre trastornos del sueño asociados a la pandemia por Enfermedad de COVID-19 se publicaran en China, epicentro de esta enfermedad. En los inicios de la pandemia Huang y Zhao7 recopilaron información de una encuesta de 7236 voluntarios e informaron que el 18% de los individuos encuestados presentaban una mala calidad del sueño. Posteriormente, los trastornos del sueño en pacientes con COVID-19 también pasaron a estudiarse en otros países, encontrando una prevalencia mayor de trastornos del sueño que antes de la pandemia en la población general en la mayoría de los estudios. En Italia, en una encuesta realizada a 2291 italianos, el 57,1% de los individuos informó de una mala calidad del sueño relacionada con la ansiedad que les ocasionaba la Enfermedad por COVID-19. Los síntomas más prevalentes fueron pesadillas, astenia y apneas del sueño. Parece que la somnolencia y el trastorno del sueño en la fase REM podrían estar más relacionados con la Enfermedad de COVID-19 en sí misma, mientras que el insomnio estaría más relacionado con el aislamiento social, la ansiedad y otros factores psicosociales.
Uno de los trabajos más relevantes publicados hasta ahora en población pediátrica y adolescente es el de Sharma M. y sus colaboradores8, cuyo objetivo fue realizar una revisión sistemática y un metanálisis para estudiar la prevalencia y el patrón de trastornos del sueño en población pediátrica y adolescente durante la pandemia por COVID-19. Para ello, los autores realizaron una exhaustiva búsqueda bibliográfica en MEDLINE, EMBASE y Web of Science en busca de estudios originales que describieran anomalías del sueño en pacientes de esta edad, con o sin trastornos neuroconductuales preexistentes, durante la pandemia por COVID-19. Los autores analizaron un total de 371 artículos pero finalmente, únicamente incluyeron 16 estudios. De estos, cinco se realizaron en niños/niñas de edad preescolar, dos en pacientes con trastornos neuroconductuales preexistentes y el resto (nueve) en población pediátrica y adolescentes sanos en edad escolar. En esta revisión los autores hallan que la prevalencia combinada de cualquier alteración del sueño en los niños durante la pandemia fue del 54% (IC del 95%: 50-57%). Estos datos, aún siendo elevados, ya que indican que más de la mitad de la población de estudio presentaba algún tipo de trastorno del sueño, serían inferiores a los encontrados en nuestra serie en la que el 70% (n=54) de los pacientes presentaba al menos un ítem positivo en evaluar el Cuestionario BEARS y el 67% (n=52) de los pacientes presentaban puntuaciones superiores a 39 puntos en la Escala de Bruni. Curiosamente, en esta revisión de Sharma, la prevalencia de estos trastornos en los niños de edad preescolar, cuyo grupo no fue evaluado en nuestra población de estudio, fue menor que en los tiempos prepandémicos (RR = 0,87; IC del 95%: 0,58-1,30), aunque estos resultados no fueron estadísticamente significativos. Este dato concuerda con el trabajo publicado por Liu Z. y su equipo9, donde los niños en edad preescolar se comportaron de manera diferente en el contexto del sueño durante la pandemia en comparación con los niños escolares y los adolescentes. Liu Z. y su equipo encuentran que, de manera totalmente inesperada, los niños en edad preescolar confinados parecían tener menos trastornos generales del sueño en comparación con la muestra del 2018 (prepandemia).
En otra revisión reciente publicada por Panda PK. y su equipo10, encontraron que el 34,5% de los pacientes pediátricos y adolescentes estudiados sufrían ansiedad, el 41,7% depresión, el 42,3% irritabilidad y el 30,8% falta de atención debido a la pandemia por la Enfermedad de COVID-19. Además, el 79,4% de los pacientes se vio afectado negativamente por la pandemia y el confinamiento. El 22,5% de la población estudiada tenía un miedo significativo a la Enfermedad de COVID-19, el 35,2% de los pacientes pediátricos y adolescentes tenían aburrimiento y el 21,3% trastornos del sueño. Además, el 52,3% de los cuidadores/padres/madres/representantes legales desarrollaron ansiedad y el 27,4% depresión mientras estaban aislados con sus hijos/hijas. En esta revisión vemos que la prevalencia de trastornos del sueño también fue algo menor que la encontrada en nuestra población de estudio pero, en cualquier caso fue significativa.
Otro dato interesante que cabe considerar es que antes de la pandemia, diferentes estudios publicaban una prevalencia de trastornos del sueño en población pediátrica y adolescente diferente a la actual. De este modo, los datos publicados según grupos de edad oscilaban entre un rango del 25% al 50% en pacientes preescolares, del 6% al 37% en escolares y de entorno el 40% en adolescentes11-14. No obstante, esta prevalencia durante la pandemia se ha visto claramente incrementada15-19 y los datos publicados hasta el momento concuerdan, en la mayoría de los trabajos, con los encontrados en nuestra población de estudio, aunque no sean del todo comparables con nuestra serie ya que la mayoría de trabajos no especifican la inclusión de pacientes con asma.
Sea como sea, lo cierto es que la pandemia por COVID-19 ha dejado las economías devastadas y la gente asustada por sí misma y por sus seres queridos. Con esta situación sin precedentes, es injustificable no dar la debida importancia al sueño, ya que un sueño saludable es sin duda el mejor rejuvenecimiento, y no en vano está asociado a numerosos beneficios, como el bienestar físico y el correcto funcionamiento de nuestro sistema inmunológico. Además, es el principal determinante de la salud mental y emocional, ya que es conocido que un sueño correcto alivia la ansiedad, el estrés y la depresión y puede tener consecuencias diversas en el desarrollo20. Por contra, los trastornos del sueño inducen neuroinflamación, que promueve la alteración de la barrera hematoencefálica y la entrada de antígenos y factores inflamatorios en el cerebro21-26. De este modo, los trastornos del sueño relacionados con la Enfermedad de COVID-19 podrían contribuir a la apertura de la barrera hematoncefálica, actuando así como una puerta para la entrada del virus SARS-CoV-2 en el cerebro y producirse entonces una mayor inflamación en el sistema nervioso central. La deprivación/restricción del sueño, su fragmentación o la apnea del sueño inducen una inflamación sistémica de bajo grado caracterizada por la liberación de varias moléculas, como las citocinas como la interleucina 6, quimiocinas y proteínas de fase aguda, y todos ellos pueden promover cambios en componentes celulares de la barrera hematoncefálica, particularmente en las células endoteliales del cerebro27-30.
En definitiva, se deberían realizar estudios futuros que incluyan el análisis de los patrones del sueño mediante la realización de electroencefalogramas, la evaluación de marcadores de inflamación así como de la función inmunitaria, en relación con los parámetros del sueño. Estos procedimientos podrían ser revolucionarios para un mejor conocimiento de la “coronasomnia”, es decir, para el control de los trastornos del sueño asociados a la pandemia debida a la Enfermedad de COVID-199
Se puede consultar el documento completo en el siguiente enlace: Aquí : Trabajo_Final_Máster_Teresa_Garriga_Baraut.pdf
Teresa Garriga Baraut. Facultativa Especialista Adjunta, Unidad de Alergia Pediátrica. Hospital Universitario Vall d’Hebron. Comité de Alergia Infantil SEAIC.
Referencias Bibliográficas:
- Bastida-Pozuelo MF, Sánchez-Ortuño MM. Preliminary analysis of the concurrent validity of the Spanish translation of the BEARS sleep screening tool for children. J Psychiatr Ment Health Nurs. 2016 Oct;23(8):513-520.
- Owens JA, Dalzell V. Use of the ‘BEARS’ sleep screening tool in a pediatric residents’ continuity clinic: a pilot study. Sleep Med. 2005 Jan;6(1):63-9.
- Pin-Arboledas G. Sociedad Española de Pediatría Extrahospitalaria y Atención Primaria (SEPEAP). Anexo: cuestionarios y herramientas. Pediatría Integral. 2010; XIV (9):749-758.
- Ramírez-Vélez R, Huertas-Zamora L, Correa-Bautista JE, Cárdenas- Calderón EG. Confiabilidad y validez del cuestionario de trastornos de sueño BEARS en niños y adolescentes escolares de Bogotá, D.C., Colombia: Estudio FUPRECOL. Retos, número 34, 2018 (2o semestre).
- Bruni O, Ottaviano S, Guidetti V, Romoli M, Innocenzi M, Cortesi F et al. The Sleep Disturbance Scale for Children (SDSC). Construction and validation of an instrument to evaluate sleep disturbances in childhood and adolescence. J Sleep Res. 1996 Dec;5(4):251-61.
- Escala de Alteraciones del Sueño en la Infancia (avpap.org) [www.avpap.org/gtsueno/Bruni.pdf].
- Huang Y, Zhao N. Generalized anxiety disorder, depressive symptoms and sleep quality during COVID-19 outbreak in China: A web-based cross- sectional survey. Psychiatry Res. 2020; 288: 112954.
- Sharma M, Aggarwal S, Madaan P, Saini L, Bhutani M. Impact of COVID- 19 pandemic on sleep in children and adolescents: a systematic review and meta-analysis. Sleep Med. 2021;84:259-267.
- Liu Z, Tang H, Jin Q, Wang G, Yang Z, Chen H et al. J. Sleep of preschoolers during the coronavirus disease 2019 (COVID-19) outbreak. J. Sleep Res. 2021; 30(1):e13142.
- Panda PK, Gupta J, Chowdhury SR, Meena AK, Madaan P, Sharawat IK et al. Psychological and behavioral impact of lockdown and quarantine measures for COVID-19 pandemic on children, adolescents and caregivers: a systematic review and meta-analysis. J Trop Pediatr. 2021;67(1):fmaa122.
- Blader JC, Koplewicz HS, Abikoff H, Foley C. Sleep problems of elementary school children. A community survey. Arch Pediatr Adolesc Med. 1997;151(5): 473e80.
- Owens JA, Spirito A, McGuinn M, Nobile C. Sleep habits and sleep disturbance in elementary school-aged children. J Dev Behav Pediatr. 2000; 21(1): 27e36.
- Pagel JF, Forister N, Kwiatkowki C. Adolescent sleep disturbance and school performance: the confounding variable of socioeconomics. J Clin Sleep Med. 2007; 15;3(1):19e23.
- Vignau J, Bailly D, Duhamel A, Vervaecke P, Beuscart R, Collinet C. Epidemiologic study of sleep quality and troubles in French secondary school adolescents. J Adolesc Health. 1997; 21(5):343e50.
- Altena E, Baglioni C, Espie CA, Ellis J, Gavriloff D, Holzinger B et al. Dealing with sleep problems during home confinement due to the COVID- 19 outbreak: Practical recommendations from a task force of the European CBT-I Academy. J. Sleep Res. 2020;29:e13052.
- Wang J, Gong Y, Chen Z, Wu J, Feng J, Yan S et al. Sleep disturbances among Chinese residents during the Coronavirus Disease 2019 outbreak and associated factors. Sleep Med. 2020; 74:199-203.
- Gruber R, Gauthier-Gagne G, Voutou D, Somerville G, Saha S, Boursier J. Pre-pandemic sleep behavior and adolescents’ stress during Covid-19: a prospective longitudinal study. Child Adolesc Psychiatry Ment Health. 2021; 30:15(1):43.
- Zreik G, Asraf K, Haimov I, Tikotzky L. Maternal perceptions of sleep problems among children and mothers during the coronavirus disease 2019 (COVID-19) pandemic in Israel. J. Sleep Res. 2021; 30(1):e13201.
- Cerasuolo M, Malloggi S, Conte F, Albinni B, De Rosa O, Rescott ML et al. The Effects of the COVID19-Related Lockdown Are Modulated by Age: An Italian Study in Toddlers and Pre-Schoolers. Brain Sci. 2021; 9:11(8):1051.
- Spruyt K. A review of developmental consequences of poor sleepness in childhood. Sleep Med. 2019; Aug;60:3e12.
- Markuu P. Sleep research in 2020: COVID-19-related sleep disorders. Lancet Neurol. 2021; 20:15–1.
- Mazza, C.; Ricci, E.; Biondi, S.; Colasanti, M.; Ferracuti, S.; Napoli, C.; Roma, P. A nationwide survey of psychological distress among Italian people during the covid-19 pandemic: Immediate psychological responses and associated factors. Int. J. Environ. Res. Public Health. 2020; 17: 3165.
- Varatharaj A, Thomas N, Ellul MA, Davies NWS, Pollak TA, Tenorio EL et al. Neurological and neuropsychiatric complications of COVID-19 in 153 patients: A UK-wide surveillance study. Lancet Psychiatry 2020; 7:875– 882.
- Sharifian-Dorche M, Huot P, Osherov M, Wen D, Saveriano A, Giacomini P et al. Neurological complications of coronavirus infection; a comparative review and lessons learned during the COVID-19 pandemic. J. Neurol. Sci. 2020; 417:117085.
- Cellini N, Canale N, Mioni G, Costa S. Changes in sleep pattern, sense of time and digital media use during COVID-19 lockdown in Italy. J. Sleep Res. 2020; 29: e13074.
- Zhang C, Yang L, Liu S, Ma S, Wang Y, Cai Z et al. Survey of insomnia and related social psychological factors among medical staff involved in the 2019 novel Coronavirus disease outbreak. Front. Psychiatry. 2020; 11:306.
- Hurtado-Alvarado G, Becerril-Villanueva E, Contis-Montes OA, Domínguez-Salazar E, Salinas-Jazmín N, N, Pérez-Tapia SM et al. The yin/yang of inflammatory status: Blood-brain barrier regulation during sleep. Brain Behav. Immun. 2018; 69, 154–166.
- Cuddapah VA, Zhang SL, Sehgal A. Regulation of the blood-brain barrier by circadian rhythms and sleep. Trends Neurosci. 2019; 42: 500–510.
- Medina-Flores F, Hurtado-Alvarado G, Contis-Montes de Oca A, López- Cervantes SP, Konigsberg M, Deli MA et al. Sleep loss disrupts pericyte- brain endothelial cell interactions impairing blood-brain barrier function. Brain Behav. Immun. 2020; 89: 118–132.
- Benedict C, Cedernaes J, Giedraitis V, Nilsson EK, Hogenkamp PS, Vågesjö E et al. Acute sleep deprivation increases serum levels of neuron- specific enolase (NSE) and S100 calcium binding protein B (S-100B) inhealthy young men. Sleep. 2014; 37: 195–198.
Angioedema hereditario: no toda hinchazón es alergia
El angioedema hereditario (AEH) es una enfermedad rara que produce episodios recurrentes de hinchazón (edema) de algunas partes del cuerpo – piel o mucosas (gastrointestinal y de vía aérea superior). A diferencia del edema alérgico, es de instauración lenta, duro (sin fóvea), cursa sin urticaria (ronchas), sin picor y habitualmente la hinchazón dura más de 24-48 horas.
Es una enfermedad genética y en la mayoría de los casos se debe a una mutación en el cromosoma 11 de transmisión autosómica dominante (la posibilidad de transmisión de la enfermedad es de un 50%). Esta mutación conduce a un déficit enzimático – cuantitativo (AEH tipo I) o funcional ( AEH tipo II) del factor C1 inhibidor del sistema del complemento. Como consecuencia se produce hinchazón en diversas localizaciones a través de un mediador bioquímico denominado bradicinina. Existen algunos desencadenantes conocidos, como la manipulación de la cavidad oral o de la vía respiratoria superior, algunos fármacos (anticonceptivos orales que contengan estrógenos, antihipertensivos del grupo de los inhibidores de la enzima convertidora de la angiotensina), las infecciones y los traumatismos. En muchas ocasiones no se reconoce un precipitante concreto.
El AEH suele debutar en edad infantil y y se agrava a partir de la pubertad. Los ataques pueden afectar a cualquier órgano y pueden ser letales si afectan a la vía aérea superior. Sin embargo, el diagnóstico suele ser tardío debido a la inespecificidad de los síntomas:
- Edema en manos, brazos, piernas, labios, párpados, lengua, garganta o genitales
- Obstrucción de la vía aérea superior. Existe riesgo vital.
- Episodios recurrentes de dolor abdominal sin causa aparente. Puede llegar a ser grave, simular causa quirúrgica, ocasionar deshidratación y/o shock hipovolémico.
La frecuencia y la intensidad de los ataques son muy variables. Varían tanto en un mismo paciente, como en los familiares afectados por la misma mutación genética.
El diagnóstico se realiza a través de un análisis de sangre, donde se objetiva una disminución del C4 del complemento y del C1 inhibidor (actividad y/o cantidad). El estudio genético establece el diagnostico definitivo.
Tratamiento
Los ataques causados por esta enfermedad no responden al tratamiento antialérgico habitual -corticosteroides, antihistamínicos, adrenalina-. Se han de tratar con medicación específica, por lo que es fundamental establecer la sospecha en la crisis aguda. Los objetivos del tratamiento se basan en 3 principios:
- Tratar las crisis que aparezcan (tratamiento de las crisis)
El inhibidor específico de C1 es el tratamiento de primera elección para los ataques agudos, en los países en los que está disponible. Se recomienda su uso via intravenosa para el tratamiento de las crisis en niños. La dosis recomendada es de 20 U/kg. El icatibant (un antagonista del receptor B2 de bradicinina, subcutáneo) es una alternativa válida aprobada para su uso en niños mayores de 2 años.
- Prevención en situaciones de riesgo especial (prevención o profilaxis a corto plazo)
Se recomienda realizar profilaxis a corto plazo con inhibidor C1 purificado intravenoso ante procedimientos quirúrgicos o manipulaciones dentales/ en la cavidad oral (aplicable de 6 horas a 1 hora antes).
- Evitar o disminuir la aparición de crisis a lo largo del tiempo (prevención o profilaxis a largo plazo).
La necesidad de profilaxis a largo plazo deberá ser individualizada para cada paciente.
Dra. Krasimira Baynova. UGC Alergología, CSUR Angioedema hereditario. Hospital Universitario Virgen del Rocío, Sevilla. Comité de Alergia Infantil de SEAIC
Enlaces de interés:
- Asociación Española de Angioedema Familiar: https://angioedema-aedaf.haei.org/
- US Hereditary Angioedema Association – HAEA (Estados Unidos): https://es.haea.org/
Bibiliografía
- Frank MM, Zuraw B, Banerji A, Bernstein JA, Craig T, Busse P, et al. Management of children with hereditary angioedema due to C1 inhibitor deficiency. 2016;138:e20160575.
- Farkas and HAWK International consensus on the diagnosis and management of pediatric patients with hereditary angioedema with C1 inhibitor deficiency. Allergy.2017 Feb; 72(2): 300–313. PMID: 27503784.
- https://angioedema-aedaf.haei.org/wp-content/uploads/2019/03/GUIA- PACIENTE-NEW-V4.pdf
Captador de la semana: Córdoba
Hoy toca presentar el captador de Córdoba, pertenece a la red de captadores de pólenes de la SEAIC.
La Dra Cristina De Castro Gómez, alergóloga en el Hospital San Juan De Dios, así como actual secretaria del comité de Aerobiología, nos aporta los datos en www.pólenes.com desde 2019.
Aviso Legal
0. RECOMENDACIÓN PREVIA:
Por favor, lea todos los apartados del presente aviso legal y nuestra política de privacidad antes de utilizar este website. Las siguientes condiciones son vinculantes para cualquier usuario del mismo. Documento revisado el 28/06/2021.
En cumplimiento con el deber de información dispuesto en la Ley 34/2002 de Servicios de la Sociedad de la Información y el Comercio Electrónico (LSSI-CE) de 11 de julio, se facilitan a continuación los siguientes datos de información general de este sitio web.
La razón de este texto es explicarle de manera detallada las funcionalidades de esta web y aportarle toda la información relacionada con el responsable y la finalidad de los contenidos incluidos en ella.
1. INTRODUCCIÓN; DATOS IDENTIFICATIVOS y USUARIOS:
El presente aviso legal y política de privacidad regula el uso del servicio del PORTAL de Internet www.seaic.org informándole en cumplimiento de la Ley 34/2002, de 11 de julio lo siguiente:
- Titular: SOCIEDAD ESPAÑOLA DE ALERGOLOGIA E INMUNOLOGIA CLINICA (SEAIC). CIF/NIF: G-58318395
- Domicilio social: Calle Agustín de Foxá 25, 28036 Madrid
- Inscrita en el Registro en el Registro Nacional de Asociaciones, Sección 1, Número Nacional 3446.
- Correo electrónico: seaic@seaic.org Teléfono: 915 348 826
- Actividad social: Sociedad profesional y científica, sin ánimo de lucro, que desarrolla sus actividades en todo el territorio del Estado español y está constituida por profesionales que trabajan en el estudio de las enfermedades de mecanismo inmunológico, particularmente por hipersensibilidad.
- Finalidad de la página web: Dar a conocer sus actividades, contactar, suscripciones y realizar alta de asociados.
El presente documento tiene por objeto establecer los términos y condiciones generales de uso del PORTAL. Los términos y condiciones generales son de obligada aceptación y cumplimiento por parte de todos las personas, profesionales y empresas (en adelante el USUARIO), que deseen hacer uso de los mismos (actuales o nuevos servicios que SEAIC preste en el futuro a través del PORTAL).
2. OBLIGACIONES DE LOS USUARIOS, USO DEL SITIO WEB, SUS SERVICIOS Y CONTENIDOS;
El usuario se compromete a utilizar el portal, el contenido y servicios, sin contravenir la legislación vigente, los usos generalmente aceptados y el orden público. Queda prohibido, el uso del Web con fines ilícitos o lesivos contra SEAIC o un tercero, que, de cualquier forma, puedan causar perjuicio o impedir el normal uso del PORTAL.
SEAIC garantiza que los contenidos y servicios que ofrece el portal respetan el principio de dignidad de la persona, de protección de la juventud y la infancia, de no-discriminación por motivos de raza, sexo, religión, opinión, nacionalidad, discapacidad o cualquier otro aspecto personal y social. SEAIC se reserva el derecho de retirar todos aquellos comentarios y aportaciones que vulneren la ley o no respeten los principios señalados.
SEAIC es titular o se encuentra debidamente autorizada para su difusión por sus legítimos titulares, de los derechos de propiedad intelectual e industrial sobre las marcas, imágenes, textos, diseños, animaciones, o cualquier otro contenido o elementos de este portal. Cualquier acto de reproducción, distribución, comunicación pública, puesta a disposición, o transformación, así como cualquier otra forma de explotación de todo o parte de dichos contenidos o elementos, realizado bajo cualquier forma o mediante cualquier medio, requerirá el consentimiento previo y por escrito de SEAIC.
Las presentes Condiciones Generales de Uso del PORTAL no confieren al USUARIO ningún otro derecho de uso, alteración, explotación, reproducción, distribución o comunicación pública del Portal y/o de sus Contenidos distintos de los aquí expresamente previstos. Los contenidos (información, archivos de sonido y/o imagen, fotografías, diseños, etc.) recogidos en el portal, son propiedad de SEAIC o se encuentra debidamente autorizada para su difusión por sus legítimos titulares. SEAIC se compromete a no realizar publicidad engañosa y por tanto, queda prohibido:
- El uso para todo tipo de fines comerciales o publicitarios, distintos de los estrictamente permitidos.
- Su reproducción, publicación, distribución o modificación, total o parcial a menos que se cuente con la autorización previa y por escrito de sus legítimos titulares o resulte legalmente permitido.
- Cualquier vulneración de los derechos de SEAIC o de sus legítimos titulares sobre los mismos.
3. PROPIEDAD INTELECTUAL E INDUSTRIAL;
En todo caso, el USUARIO reconoce y acepta que todos los derechos de propiedad industrial e intelectual sobre los Contenidos y/o cualesquiera otros elementos insertados en el portal pertenecen a SEAIC o se encuentra debidamente autorizada para su difusión en el presente PORTAL. En el caso de que un usuario o un tercero consideren que se ha producido una violación de sus legítimos derechos de propiedad intelectual por la introducción de un determinado contenido en el Web, deberá notificar dicha circunstancia a SEAIC indicado:
- Datos personales del interesado titular de los derechos presuntamente infringidos, o indicar la representación con la que actúa en caso de que la reclamación la presente un tercero distinto del interesado.
- Señalar los contenidos protegidos por los derechos de propiedad intelectual y su ubicación en el Web, la acreditación de los derechos de propiedad intelectual señalados y declaración expresa en la que el interesado se responsabiliza de la veracidad de las informaciones facilitadas en la notificación.
4. ENLACES
El PORTAL proporciona enlaces a otros sitios web propios y contenidos que son propiedad de terceros. El único objeto de los enlaces es proporcionar al usuario la posibilidad de acceder a dichos enlaces. SEAIC no se responsabiliza en ningún caso de los resultados que puedan derivarse al usuario por acceso a dichos enlaces.
El usuario que se proponga establecer cualquier dispositivo técnico de enlace desde su sitio web al portal www.seaic.org deberá obtener la autorización previa y escrita de SEAIC. El establecimiento del enlace no implica en ningún caso la existencia de relaciones entre el PORTAL y el propietario del sitio en el que se establezca el enlace, ni la aceptación o aprobación por parte de www.seaic.org de sus contenidos o servicios.
5. MODIFICACIÓN UNILATERAL Y DURACIÓN;
SEAIC se reserva el derecho de modificar, en cualquier momento y sin necesidad de previo aviso, la presentación y configuración del PORTAL web www.seaic.org como el presente aviso legal.
6. EXCLUSIÓN DE GARANTÍAS Y RESPONSABILIDAD;
SEAIC no otorga ninguna garantía ni se hace responsable, en ningún caso, de los daños y perjuicios de cualquier naturaleza que pudieran acarrear a causa de:
- La falta disponibilidad, mantenimiento y efectivo funcionamiento del Web y/o de sus servicios o contenidos.
- La existencia de virus, programas maliciosos o lesivos en los contenidos.
- El uso ilícito, negligente, fraudulento, contrario a las presentes Condiciones Generales, a la buena fe, a los usos generalmente aceptados o al orden público, del sitio Web, sus servicios o contenidos, por parte de los usuarios.
7. TRATAMIENTO DE DATOS PERSONALES
SEAIC, tal y como recoge en su “POLITICA DE PRIVACIDAD” que puede consultar en nuestra web, ha adoptado los niveles de seguridad adecuados a los datos que trata y gestiona, incorporando todos los medios y medidas técnicas a su alcance para garantizar su confidencialidad, evitar su mal uso, pérdida, alteración, acceso no autorizado y robo.
8. LEGISLACIÓN APLICABLE Y JURISDICCIÓN;
Las presentes Condiciones Generales se regirán por la legislación española, sometidas a los juzgados y tribunales de la ciudad de Madrid (España) ante cualquier controversia derivada del acceso al PORTAL.
9. CONTACTO
En caso de que cualquier Usuario tuviese alguna duda acerca de este aviso legal o cualquier comentario sobre la web puede dirigirse a seaic@seaic.org
Angiodema hereditario
Seguimiento del angioedema hereditario
Requisitos
- Diagnóstico previo de angioedema hereditario confirmado por un especialista.
- Disposición de teléfono, sistema de videoconsulta y de envío de imágenes. Disposición de Internet. El paciente ha de entender el sistema de funcionamiento de la aplicación empleada.
- No sufrir ninguna discapacidad que impida usar ninguno de estos sistemas.
- El paciente menor de 16 años debe estar acompañado por un progenitor o persona responsable.
- Consentimiento verbal o escrito del paciente o tutor legal, que debe reflejarse en la historia clínica. Actualmente la normativa no exige el consentimiento por escrito.
- Aceptar unas condiciones de legales y de privacidad de datos acorde a la normativa vigente.
Fase de preparación
- Fecha y hora de la visita.
- Si precisa: cuestionarios de evaluación de calidad de vida para angioedema, con instrucciones para su cumplimentación y para disponer, en el momento de la consulta, de ellos ya cumplimentados.
- Valoración de pruebas complementarias, si estas han sido solicitadas en la visita anterior.
Esta fase puede estar dirigida a una visita de revisión ya programada o a una visita solicitada por el propio paciente para resolver dudas o abordar una reagudización de la enfermedad o preparar futuros momentos que supongan un aumento de riesgo, como intervenciones o viajes.
Consulta telemática
Se realiza mediante llamada telefónica o plataforma para videoconsultas. Se aconseja realizar consultas síncronas aunque la disposición de consultas asíncronas puede ayudar a mejorar la accesibilidad del sistema y su usabilidad para el paciente. Durante el desarrollo de la consulta se abordarán los siguientes aspectos:
Introducción
Presentación y recordatorio del motivo de la consulta de seguimiento.
Evaluación del estado actual
- Preguntar por la frecuencia de brotes, áreas afectadas y gravedad de las crisis desde la última consulta.
- Investigar si ha habido algún desencadenante identificable o pródromos en las crisis.
- Preguntar por la duración y respuesta al tratamiento de rescate de los episodios. Preguntar cuántos episodios precisaron tratamiento en algún centro médico y cuántos se resuelven en domicilio.
- Los episodios ¿han tenido repercusión en actividades diarias o laborales?
- Indagar sobre el uso correcto del medicamento de rescate: ¿qué intervalo temporal existió entre el inicio de los síntomas y la administración del medicamento de rescate?
Valoración de pruebas complementarias en caso de haberse solicitado previamente
Comentar los resultados de analíticas y pruebas de imagen, si estas se habían solicitado en anterior consulta.
Revisión de medicación de mantenimiento a largo plazo
- Confirmar la adhesión al tratamiento prescrito. ¿Ha olvidado alguna dosis del tratamiento de control a largo plazo?
- Preguntar por posibles efectos secundarios del mencionado medicamento, o por nuevas afecciones aunque a priori no tengan una relación causal aparente con el medicamento pautado. (Ante la supuesta aparición de efecto adverso por el medicamento empleado, comunicar a farmacovigilancia).
- Discutir cualquier cambio en la dosis o la necesidad de ajustes en la medicación.
Educación y asesoramiento
- Ofrecer consejos sobre medidas de autocuidado, identificación de desencadenantes y estrategias para evitarlos.
- Aclarar cualquier duda o preocupación del paciente sobre su condición y tratamiento.
Plan de manejo consensuado
- Establecer un plan de acción para manejar futuros ataques, incluida la instrucción en el uso del medicamento de rescate.
- Recordar las señales de alarma que requieren atención médica inmediata.
- Confirmar la disponibilidad de medicamentos y recursos en caso de nuevo episodio. Actualizar receta electrónica.
Seguimiento y programación de citas
- Programar la próxima consulta de seguimiento o cualquier prueba complementaria necesaria.
- Confirmar la disponibilidad de apoyo continuo de atención médica entre consultas, según disponibilidad de cada área (teléfono de contacto, consulta WhatsApp, consulta médico de primaria, etc)
Despedida
Fijar fecha de próxima cita y agendar.
Agradecer al paciente por su tiempo y colaboración.
Documentación adecuada de la consulta en la historia clínica electrónica del paciente.
Consultas asíncronas: Aunque se aconseja realizar consultas síncronas, la disposición de consultas asíncronas puede ayudar a mejorar la accesibilidad del sistema y su usabilidad para el paciente. En caso de optar por esta modalidad debe disponerse siempre de un correo electrónico seguro con dirección de correo electrónico corporativa. A través de esta vía pueden enviarse al paciente:
- Cuestionarios de calidad de vida para angioedema.
- Informes clínicos actualizados.
- Planes de tratamiento nuevos, copia de receta electrónica o receta de farmacia hospitalaria.
- Aplicaciones recomendadas.
- Copias de pruebas de imagen o de laboratorio si lo solicita el paciente.
Aplicaciones y páginas web
de apoyo a la consulta telemática en angioedema hereditario.
Recursos adicionales para pacientes
- Guía del paciente angioedema hereditario:
- Asociación española de angioedema familiar
- https://angioedema-aedaf.haei.org
Grupos de trabajo del Comité de Asma SEAIC
Los grupos de trabajo del Comité de Asma de la SEAIC abordan áreas clave de la enfermedad con el objetivo de avanzar en el conocimiento, mejorar la atención clínica y promover la formación e investigación en asma desde un enfoque multidisciplinar y colaborativo:
- Grupo de relación con Atención Primaria – Coordinadores Ibon Eguiluz y Manuel Pajarón
- Grupo de Asma Grave – Coordinadores Julio Delgado y Javier Domínguez
- Grupo de Comunicación: redes sociales, web y medios de comunicación – Coordinadoras Lorena Soto y Paula Galván
- Grupo de relación con Pacientes y Enfermería – Coordinadora Virginia Bellido
- Grupo de Asma Infantil – Coordinadoras Remedios Cárdenas y Alicia Habernau
- Grupo de Procedimientos en Asma – Coordinadora Mª del Mar Fenández Nieto
- Grupo de Inmunoterapia en Asma – Coordinadora Lorena Soto
- Grupo de relación con el Comité de Rinoconjuntivitis (especial interés en RSCcPN) – Coordinador Ismael García
- Grupo de Investigación y relación con PII de SEPAR – Coordinadores Juan Carlos Miralles e Ismael García
- Grupo Comisión Acreditación UAG – Coordinadora Alícia Habernau
- Grupo de Tos Crónica – Coordinadores Manuel Rial y Paula Galván
Captador de la semana: Ciudad Real
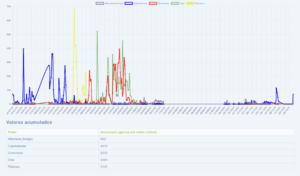
Desde el Hospital General Universitario de Ciudad Real, los doctores Alberto Palacios, Aranzazu Martin, Alba Extremera y Carmen García, nos proporcionan los datos a pólenes.com.
A continuación os dejamos un interesante video que han realizado donde podéis observar su captador y la recogida de muestras.
Video: ¿cómo se cuentan los pólenes?
Muchas personas sufrimos enfermedades respiratorias alérgicas causadas por pólenes, y durante los meses de primavera buscamos información sobre cómo de alto está ese día el polen que nos preocupa, de cara a protegernos, tomar medicación o planificar un viaje, pero, ¿cómo se realizan esos contajes?
El comité de Aerobiología cuenta con una red de colectores repartidos por todo el país, con el objetivo de potenciar el estudio de los pólenes y hongos ambientales. Se trata de captadores volumétricos que succionan el aire ambiente, impactando las partículas sobre una superficie que posteriormente se recoge, se prepara sobre un portaobjetos, y finalmente se realiza un contaje de manera manual utilizando un microscopio óptico.
Aquí un video publicado por Canal Sur el 26 de abril de 2023 en el que Manuel Alcántara, vocal de la Sociedad Española de Alergología e Inmunología Clínica, explica y muestra el proceso.
Dra. Alicia López Guerrero, Hospital Universitario de Jaén, Jaén. Comité Aerobiología Clínica.
Felicitación de Navidad
Estimados asociados, pacientes, entidades y personas afines a la Sociedad Española de Alergología e Inmunología Clínica:
La Junta Directiva de la SEAIC desea transmitiros sus mejores deseos para estas fechas tan especiales. La Navidad nos invita a reflexionar sobre los logros compartidos, renovar nuestras metas y reforzar el compromiso con nuestra labor científica y humana.
Que este espíritu inspire vuestra dedicación y os colme de serenidad, alegría y esperanza para afrontar los retos del próximo año.
Recibid nuestro más cordial saludo.
Acta Reunión Comité Alergia Cutanea Valencia 2018
![]() Contenido disponible sólo para socios.
Contenido disponible sólo para socios.
Homenaje al Dr. Conde
Una vida, una ilusión…
HISTORIA DE LOS INHALADORES
La administración o aplicación de los tratamientos inhalados se conoce desde hace 4000 años en China, India y Egipto. En aquella época se administraban plantas ricas en escopolamina y en atropina (como Datura stramonium o Atropa belladona) en forma de vahos, fumigaciones, pipas de agua e incluso “cigarrillos terapéuticos” por su efecto relajante en el músculo bronquial.
La terapia inhalada comienza en los balnearios en el s.XIX cuando empiezan a utilizar las nebulizaciones para tratar la tuberculosis. En 1856, el médico Sales-Girons desarrolló el primer inhalador portátil lo que permitió la administración en domicilio. Aunque estos aparatos tuvieron detractores que los consideraban ineficaces, se siguieron desarrollando nuevos modelos. Si bien, en la farmacología el interés de la vía respiratoria fue en aumento sobre todo cuando se aisló la molécula de adrenalina en 1901 por Thomas Aldrich y Jokichi Takamine y cuando Bullying desarrolló un nebulizador con motor eléctrico. Los siguientes avances se dieron en conseguir broncodilatadores con menos efectos adversos y aparatos más pequeños que generaran partículas inferiores a 5 micras.
De esta forma, gracias a los avances en farmacología se consiguió identificar los receptores α y β adrenérgicos en 1947 y posteriormente, los β1 y β2 lo que dio lugar al descubrimiento en 1969 de un broncodilatador específico con mínimos efectos cardiovasculares y musculares, el salbutamol.
En 1948 se comercializó una primera versión de los futuros dispositivos de inhalación Aerohaler®. Era un vial de vidrio donde se colocaba el principio activo en forma de polvo seco la cantidad que en cada situación se consideraba adecuada y el paciente aspiraba a través de una pieza desmontable, por la boca o por la nariz. Este dispositivo fracasó ya que las dosis administradas eran variables, cada persona utilizaba la dosis que le parecía bien, además los asmáticos que lo utilizaban no eran capaces de generar el flujo suficiente para mover el fármaco y quedaba casi todo en el vial. Cuando se inhalaba por la nariz, la función de filtro de las fosas nasales hacía que no llegara el fármaco hasta el árbol bronquial, por lo que desde entonces se desechó la aplicación nasal.
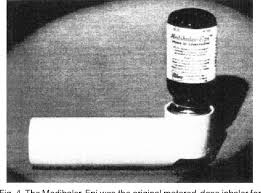
El primer inhalador de cartucho presurizado surgió en el año 1956, a raíz de la insistencia de la hija asmática del doctor George Maison que le solicitaba un inhalador cómodo y portátil. Éste tenía un mecanismo valvular para dispensación de fluidos por medio de un propelente. Con el tiempo sería empleado en medicina pero también en cosmética (desodorantes, espuma de afeitar, etc) le denominaron Medihaler. Su éxito fue inmediato. Era un aparato ligero, portátil y que siempre administraba dosis fijas que venían medidas de fábrica. Su inicio de acción era rápido y cómodo de usar en cualquier lugar. Su principal desventaja era la coordinación de la inspiración con la activación del aparato.
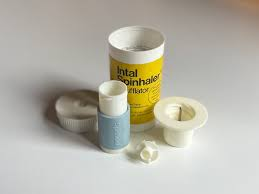
El origen de los inhaladores de polvo seco va unido al descubrimiento, por el médico Roger Altounyan, del cromoglicato disódico como protector del broncoespasmo por su acción relajante sobre el músculo liso. Debido a ello, en 1967 se lanzó al mercado el primer inhalador de polvo seco, Spinhaler® diseñado específicamente para administrar el cromoglicato disódico. Este dispositivo aportó dos grandes avances:a) administración de dosis fijas, por medio de una cápsula que se introducía en el dispositivo y se perforaba para liberar el polvo al inhalar; y b) no se planteaba como una medicación de rescate sino como una “profilaxis”. Spinhaler® ha dado lugar a toda la familia de inhaladores de polvo seco. Y además aportaba la ventaja frente al inhalador de cartucho presurizado de no tener que coordinar la inhalación con la función del aparato. Sus desventajas es que precisan mayor flujo inspiratorio y su uso puede ser complejo en personas mayores o con deformidad en las manos.
En los años 70 llegaron las cámaras espaciadoras/inhalatorias, permitiendo llevar los beneficios del cartucho presurizado a pacientes con dificultad para coordinar la maniobra.
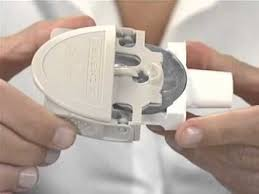
En los años 80 aparecieron los inhaladores de polvo seco multidosis, Diskhaler®. Esto reducía la complejidad y dificultad de la maniobra ya que las cápsulas con el polvo seco vienen integradas en el dispositivo y sólo hace falta cargarlas e inhalar. Aunque siguen precisando de alto flujo inspiratorio por parte del paciente y no se pueden acoplar a una cámara espaciadora al igual que los dispositivos de polvo seco unidosis.
A partir de estas familias de inhaladores, (cartuchos presurizados, inhaladores de polvo seco unidosis y multidosis) han ido surgiendo diferentes sistemas modernos que reutilizan la idea original y añaden mejoras como contadores de dosis, sistemas de feedback para que el paciente realice correctamente la técnica inhalatoria, etc.
Desde 1997 se conocen los inhaladores de vapor suave (Respimat®), en el que el fármaco en disolución es propulsado por un efecto de muelle, sin propelentes. Esto permite una maniobra inhalatoria sencilla, con una capacidad inspiratoria baja o muy baja, que unido a su producción de partículas muy pequeñas alcanza un gran depósito pulmonar. De todas maneras este sistema no llegó a España hasta 2010.
Otras variantes del cartucho presurizado clásico que han aparecido después han sido los sistemas Alvesco® y Modulite® donde el fármaco está disuelto, en vez de en suspensión, produciendo partículas muy finas y permitiendo una penetración pulmonar mayor. A su vez los sistemas accionados por la inspiración, Autohaler®, Easy Breath ® perciben el momento en que el paciente realiza la inspiración y se activan para propulsar el fármaco. Aunque este sistema no se ha comercializado en España.
BIBLIOGRAFÍA
- Las 4 reglas de la terapia inhalada.
- https://www.agefec.org/web/wp-content/uploads/2013/03/INFORMACI%C3%93N-ESCRITA-TALLER.pdf
- GEMA inhaladores. Terapia inhalada: fundamentos, dispositivos y aplicaciones prácticas. 2018
GEMA 5.4 Guía Española para el Manejo del Asma
Os presentamos la actualización del año 2024 de la Guía Española para el Manejo del Asma: GEMA 5.4
GEMA 5.4 es una guía de práctica clínica independiente basada en la evidencia, elaborada por un grupo multidisciplinar de expertos que representan a 18 sociedades científicas nacionales e internacionales. Es la guía de referencia en asma en todo el mundo de habla hispana. No se trata de una extensa monografía que aglutina todo el conocimiento científico sobre la enfermedad, sino de un documento conciso, que recoge lo esencial para que el profesional sanitario no experto en dicha patología pueda ofrecer una asistencia clínica de calidad a sus pacientes. Es por ello por lo que es breve, concreto y claro; elementos indispensables para que pueda ser aplicado con éxito.
- Está disponible, en diferentes formatos, en www.gemasma.com. En España incluso existe una aplicación de inteligencia artificial (iaGEMA) basada exclusivamente en la guía, que ha demostrado una gran agilidad para la ayuda de la toma de decisiones por el clínico en tiempo real.
 Disponible aquí el documento solo para socios de SEAIC:
Disponible aquí el documento solo para socios de SEAIC:
Los principales cambios de esta edición se pueden resumir en los siguientes:
- Identificación de nuevos factores de riesgo para la aparición de asma (sobrepeso u obesidad de la embarazada) o de desencadenantes de crisis o exacerbaciones (cambios climáticos extremos).
- Constatación ante la reciente y robusta evidencia del impacto que supone para el riesgo futuro de asma las crisis y exacerbaciones recurrentes, ocasionando una pérdida acelerada de función pulmonar y, en consecuencia, una potencial peor respuesta al tratamiento futuro.
- Incorporación de las principales conclusiones del reciente consenso REMisión en Asma (REMAS) efectuado por 120 expertos provenientes de la propia GEMA y del Foro de Asma de SEPAR, en donde se estableció en 3 años el periodo de tiempo para determinar la remisión completa y en donde se definió las características de un nuevo concepto de remisión, el de “remisión en asma y RSCcPN (vía respiratoria única)”.
- Descripción de los conceptos de transferencia y elementos para la transición entre los diferentes niveles asistenciales, de la atención médica infantil a la del adulto, en el paso del niño-adolescente a la del adulto asmático.
- Identificación (por el grupo de trabajo GEMA-POLINA) de ocho posibles escenarios de tratamiento combinado en pacientes con asma grave (controlada o no, con o sin anticuerpos monoclonales) y RSCcPN (operada o no previamente).
- Descripción de las posibles causas de respuesta subóptima al tratamiento biológico del asma grave no controlada (AGNC) y propuesta de actuación racional con cinco acciones secuenciales antes del cambio de anticuerpo monoclonal.
- Asunción de los nuevos criterios de tratamiento continuo con glucocorticoides orales (corticodependencia) en asma propuestos en el reciente consenso español sobre dicho tema.
- Actualización de los criterios diagnósticos y terapéuticos de la granulomatosis eosinofílica con poliangeítis (GEPA).
- Y como siempre, la incorporación de algunas citas bibliográficas relevantes concretas.
Canarias
Canarias
Centros con actividad asistencial pública en Alergología
Hospital Doctor José Molina Orosa (Lanzarote)
- http://www.gobiernodecanarias.org/sanidad/scs/hospitaldelanzarote
- Ctra. Arrecife-Tinajo, km 1,300. 35050 Arrecife
- 928595000
Hospital General de Fuerteventura
- http://www.gobiernodecanarias.org/sanidad/scs/hospitaldefuerteventura
- Ctra. del Aeropuerto, km 1. 35600 Puerto del Rosario
- 928862000
Hospital Universitario de Canarias
- http://www3.gobiernodecanarias.org/sanidad/scs/organica.jsp?idCarpeta=3da5f513-541b-11de-9665-998e1388f7ed
- Ctra. Ofra S/N La Cuesta 38320 La Laguna
- 922678000
Hospital Universitario de Gran Canaria Dr. Negrín
- http://www.gobiernodecanarias.org/sanidad/scs/hospitalnegrin
- C/ Barranco de la Ballena, s/n. 35020 Las Palmas de Gran Canaria
- 928450000
Hospital Universitario Insular Materno-Infantil de Canarias
- http://www.gobiernodecanarias.org/sanidad/scs/ComplejoHospitalInsular-MaternoInfantil
- Avda. Marítima del Sur, s/n. 35016 Las Palmas de Gran Canaria
- 928444000
Hospital Univesitario Nuestra Señora de La Candelaria
- http://www.hospitaldelacandelaria.com
- Ctra. del Rosario, 145. 38009 Santa Cruz de Tenerife
- 922602000
GEMA 5.5 Guía Española para el Manejo del Asma
ACTUALIZACIÓN 2025. GEMA 5.5
Presentación GEMA 5.5
GEMA es una guía clínica independiente basada en evidencia científica y elaborada por un equipo multidisciplinario de especialistas pertenecientes a 18 sociedades científicas nacionales e internacionales. Constituye la referencia principal sobre asma para el mundo hispanohablante.
No se trata de una extensa recopilación del conocimiento científico sobre el asma, sino más bien de un documento breve y preciso, que contiene la información esencial para que los profesionales de la salud, incluso aquellos no especializados en esta patología, puedan ofrecer a sus pacientes una atención clínica de calidad. Su brevedad, concreción y claridad son elementos clave para una aplicación efectiva.
Está disponible en distintos formatos en www.gemasma.com.
Una de las principales fortalezas de GEMA radica en su actualización anual. Esta labor es exclusiva del Comité Ejecutivo GEMA, asistido por una comisión de cuatro expertos (proGEMA), encargados de revisar los artículos sobre asma publicados en revistas indexadas durante el año anterior.
Esta comisión está formada por los doctores Astrid Crespo (Neumología), Miguel Ángel Lobo (Medicina Familiar), Lorena Soto (Alergología) y Álvaro Gimeno (Pediatría).
La selección de los artículos más relevantes es fundamental para determinar los cambios significativos en cada actualización anual.
Novedades Edición 2025
Los principales cambios de esta edición (destacados en azul para facilitar su identificación) incluyen:
• Nuevos factores de riesgo identificados para el desarrollo de asma, como el peso muy bajo al nacer (<1500 g).
• Actualización del objetivo terapéutico principal del tratamiento del asma, orientado a lograr y mantener la remisión clínica rápidamente, previniendo exacerbaciones, controlando síntomas y optimizando la función pulmonar.
• Revisión del uso de anticuerpos monoclonales en pacientes con exacerbaciones graves atendidos en servicios de urgencias, área donde la evidencia sigue siendo limitada, aunque se han publicado nuevas investigaciones.
• Nuevas evidencias sobre la terapia MART en mayores de 12 años y recomendaciones actualizadas sobre el uso de salbutamol en población pediátrica.
• Actualización del apartado sobre biológicos en población pediátrica con asma grave, incluyendo una nueva tabla resumen.
• Nuevas evidencias sobre el uso de anticuerpos monoclonales en el tratamiento de la rinosinusitis crónica, con o sin pólipos, así como la incorporación de nuevos fárma- cos biológicos.
• Evidencias actualizadas respecto al uso de fármacos biológicos para el tratamiento del asma grave no controlada (AGNC) y actualización del algoritmo terapéutico según el fenotipo.
• Actualización del apartado sobre aspergilosis broncopulmonar alérgica siguiendo las recomendaciones del grupo de trabajo ISHAM-ABPA 2024 sobre diagnóstico, clasificación y tratamiento.
• Nuevas evidencias sobre tratamientos biológicos para la granulomatosis eosinofílica con poliangeítis (GEPA), incluyendo benralizumab como nuevo tratamiento aprobado por agencias reguladoras sanitarias.
• Incorporación habitual de referencias bibliográficas relevantes específicas.