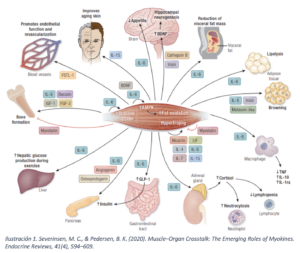
El músculo esquelético ha sido tradicionalmente reconocido por su papel considerado exclusivamente mecánico. Sin embargo, el paradigma actual lo posiciona como órgano endocrino que produce su acción mediante la secreción citoquinas que se han denominado mioquinas. Las mioquinas se producen y se liberan junto con otros péptidos por fibras musculares de forma para/auto/endocrina. Son las moléculas responsables de comunicación músculo-órganos. Gracias a ellas, el músculo modula la homeostasis metabólica y el sistema inmunitario. Una de las citoquinas más conocidas en este ámbito es la IL-6. La IL-6 en una interleucina con una función dual; modula la diferenciación de los linfocitos naive, pudiendo tener implicaciones en algunas enfermedades alergológicas como el asma, la urticaria o la dermatitis atópica.
SEÑALIZACIÓN POR LA VÍA CLÁSICA
La IL-6 que se produce durante el ejercicio señaliza predominantemente por la denominada “vía clásica”, actuando como una “hormona de esfuerzo” y ejerciendo funciones antiinflamatorias. Esta vía se activa cuando la IL-6 se une a su receptor de membrana (mIL-6R) en la célula objetivo. El receptor de IL-6 en la membrana celular está compuesto por dos subunidades:
- Receptor de IL-6 (IL-6R o CD126): Subunidad que se une a la IL-6 y la glicoproteína 130 (gp130): Subunidad transductora de señal que es esencial para que el efecto biológico de la IL-6 se lleve a cabo, formando un complejo IL-6-mIL-6R (en célula transmisora)
- Proteína gp130 (en célula receptora vecina).
De esta forma la IL6 es capaz de señalizar a las células que expresan el Receptor de Membrana (mIL-6R), entre los que se encuentran fundamentalmente:
- Hepatocitos: producción proteínas de fase aguda (reparación muscular)
- Linfocitos B: estimula su diferenciación en células plasmáticas y aumenta producción de inmunoglobulinas.
- Linfocitos T: induce respuestas antiinflamatorias a través de la producción de IL-1rα e IL-1.
- Neutrófilos y Macrófagos: ven modulada su activación por citoquinas antiinflamatorias
La IL6 señalizando por esta vía, realiza una función sistémica protectora (ej. inducción de proteínas de fase aguda en el hígado para reparación muscular) opera en condiciones dónde su concentración es baja o moderada, por lo que la IL-6 producida actúa localmente o activas células con alta expresión de mIL-6R (activando la señalización por la vía clásica). Además, existe un sistema tampón o “buffer” formado la proteína soluble gp130 (sgp130) que se escinde de las membranas celulares, en el plasma sanguíneo. En condiciones no inflamatorias, el sistema tampón permite la señalización homeostática local principalmente en células inmunitarias y hepatocitos, pero neutraliza la IL6 antes de que pueda activar su vía patológica (neutralizando el complejo IL6-sIL6R) evitando que se activen otras células como las células musculares lisas y células endoteliales, que no son las células con alta expresión de receptor de membrana de IL-6. Este mecanismo funciona porque el complejo IL6-sIL6R se une con mayor afinidad a la versión soluble de la proteína gp130, que a su versión de membrana, al unirse el sgp130, el complejo IL-6-sIL6R-sgp130 queda inactivado y secuestrado en el plasma, impidiendo que la IL-6 provoque efectos proinflamatorios a través de la señalización patológica o trans-señalización
Un nivel bajo de IL-6 y el sistema tampón previenen la señalización sistémica patológica de IL-6. En condiciones inflamatorias agudas y crónicas, el sistema tampón se sobrecarga y permite la trans-señalización sistémica de IL-6.
SEÑALIZACIÓN POR LA VÍA “TRANS”
La obesidad crónica causa que los adipocitos hipertrofiados se vuelvan disfuncionales y entren en apoptosis. Esto atrae a los macrófagos para eliminarlos. Estos macrófagos proinflamatorios forman estructuras llamadas «coronas» alrededor de estos adipocitos. Estos macrófagos liberan citoquinas altamente proinflamatorias, que incluyen IL-6, y también TNF−α e IL−1β. La IL-6 en estas circunstancias amplifica la señalización proinflamatoria. El tejido adiposo inflamado y los macrófagos liberan grandes cantidades del receptor soluble de IL-6 (sIL-6R) a la circulación. Al haber gran concentración de sIL-6R, la IL-6 se une a él y forma un complejo (sIL-6R-IL-6) que activa la señalización por la vía trans. Esta vía activa de forma patológica las células que normalmente no responden a la IL-6 (como las células endoteliales y las células musculares), generando entre otros efectos crónicos, resistencia a la insulina y disfunción endotelial. En estas circunstancias, la liberación de IL-6 visceral en la obesidad y en otros transtornos inflamatorios, es crónica y sostenida, agotando el mecanismo de neutralización (buffer).
IL-6 Y EJERCICIO FÍSICO
El músculo esquelético puede aumentar la concentración de IL-6 plasmática hasta x1000 durante el ejercicio. La magnitud de esta respuesta viene determinada por las características del ejercicio. Esto ocurre porque disponemos de dos tipos de fibras musculares:
- Fibras Tipo I: Fibras de contracción lenta, oxidativas, resistentes a la fatiga.
- Fibras Tipo II: fibras de contracción rápida, glicolíticas, utilizadas para fuerza y potencia.
Duración e intensidad del ejercicio
La duración del ejercicio se relaciona de forma directa con la concentración de IL-6 muscular, lo que supone el estímulo más importante para el aumento de IL-6 plasmática. La concentración de IL-6 dentro de las fibras musculares aumenta más que la concentración plasmática, ya que el músculo actúa como reservorio. Las fibras musculares de tipo I son la principal fuente de IL6 plasmático. Este tipo muscular es el tipo reclutado en ejercicio de larga duración y moderada intensidad. La concentración de IL-6 es proporcional a la duración del ejercicio, aumentado de forma exponencial. También cae exponencialmente poco después de finalizar
La producción de IL6 se amplifica en ejercicio de mayor intensidad ante igual duración. Aparentemente se requiere un mínimo de intensidad para inducir la respuesta de I-L6, al menos en las actividades de baja duración.
La interacción tanto de la intensidad como de la duración del ejercicio son importantes para determinar la respuesta de IL6 plasmática con respecto al ejercicio
TIPO DE EJERCICIO Y ESTADO DE ENTRENAMIENTO
Tipo de ejercicio: Estudios longitudinales sugieren que las personas entrenadas pueden producir más cantidad de IL-6 que las no entrenadas incluso cuando trabajan a la misma intensidad. Este efecto es menor en comparación con intensidad y duración del ejercicio en general. Algunos tipos de ejercicio producen concentraciones plasmáticas superiores a otros (p. ej: más IL-6 plasmática en carrera Vs bicicleta, probablemente debido a que se produce contracción excéntrica y más daño muscular en la carrera, por lo que se produce fuga de IL-6 a la circulación, y reclutamiento de leucocitos que también aumentan la producción de IL-6).
Estado de entrenamiento: La concentración de IL-6 en reposo no reflejan la liberación muscular sino la producción por otras vías, inflamatorias a través de leucocitos, adipocitos disfuncionales y su acumulación, por lo que es indicativa del estado de inflamación del individuo, de hecho es inversamente proporcional a la actividad física habitual. Los programas de entrenamiento han demostrado disminuir la IL-6 en reposo de población inactiva o con inflamación crónica, acompañado de la disminución de otros marcadores inflamatorios (PCR, TNFα). Además, en atletas de élite con concentraciones de IL-6 plasmáticas muy inferiores a población con enfermedades crónicas, aumentando la cantidad de entrenamiento no se produce mayor disminución de concentración de IL-6 con respecto a sus valores en reposo, por lo que es posible que los atletas de élite con altas cargas de entrenamiento, no puedan disminuir AUN MÁS su concentración de IL-6.
Además, se ha sugerido que el sobre-entrenamineto puede producir un aumento de la concentración de IL-6 basal y un estado inflamatorio. Se ha observado este efecto en personas con periodos cortos de entrenamiento de muy alta intensidad y en deportistas con sobre-entrenamiento.
Se hipotetiza entonces que la curva que relaciona la concentración de IL-6 y carga de entrenamiento tiene forma de U, tanto en individuos sedentarios como en entrenados. De esta forma, encontramos valores altos de IL-6 en reposo en pacientes sedentarios debido al estado inflamatorio, y en deportista sobreentrenados, encontrando menores niveles de IL-6 basal en pacientes con altas cargas de entrenamiento, que no han llegado al sobre-entrenamineto.
En este sentido, en estudios experimentales en ratones se ha observado que Tozilizumab deteriora el aumento de la masa del VI tras 12 semanas de entrenamiento aeróbico en comparación con placebo, y que las infusiones de IL6 recombinante junto con un programa de ejercicio, condujeron en modelos murinos, a un aumento del rendimiento en comparación con el mismo programa sin IL6.
Por este motivo, hay que entender el músculo esquelético como un órgano endocrino dinámico, capaz de modular el estado inflamatorio sistémico a través de la secreción de IL-6. La clave de su impacto no reside en la molécula en sí, sino en el contexto de su señalización. Mientras que la obesidad y el estado proinflamatorio saturan el mecanismo de neutralización de la IL-6 (buffer de sgp130), permitiendo una trans-señalización patológica que daña el endotelio y el metabolismo, el ejercicio físico favorece la señalización por la vía clásica, transformando a la IL-6 en una hormona de esfuerzo esencial para la reparación muscular y efecto antiinflamatorio.
El ejercicio regular de intensidad moderada actúa como el estímulo idóneo para favorecer la inmunomodulación en la inflamación crónica, subrayando que la IL-6 muscular no es solo un subproducto del esfuerzo, sino una señal biológica indispensable para la homeostasis del organismo.
INMUNOMODULACIÓN VÍA IL-6
La IL-6 desempeña un papel crítico en la modulación del sistema inmune adaptativo. En los linfocitos B es esencial para la diferenciación hacia cél. plasmáticas productoras de inmunoglobulinas. En los linfoctios T influye en el equilibrio de subpoblaciones, promoviendo la diferenciación de los linfocitos T naive hacia Th17, y limitando la diferenciación hacia linfocitos T reguladores al limitar la expresión Foxp3 (interruptor genético Treg)
Al promover TH17 e inhibir Treg, desplaza el equilibrio inmune hacia un estado pro-inflamatorio y autoinmune. Los Treg actúan para suprimir la actividad de todas las células T efectoras (IL10 suprime Th1, Th2 y Th17), manteniendo así la homeostasis y evitando respuestas inmunes inapropiadas. Si los T reguladores funcionan adecuadamente suprime la actividad de las células T efectoras, incluyendo T2, favoreciendo la tolerancia a los alérgenos, reduciendo la intensidad de la respuesta alérgica y la producción de IgE. Por este motivo el ejercicio moderado y crónico disminuye de forma indirecta respuesta T2 promoviendo un ambiente antiinflamatorio sistémico.
En enfermedades como el asma o la dermatitis atópica grave, la IL-6 actúa como un puente entre la inflamación T2 y la inflamación Th17 donde la liberación de IL6 e IL−1β (ambiente inflamatorio) favorecen la supresión T reguladoras y la diferenciación hacia Th17 con una inflamación predominantemente neutrofilica que se añade a la inflamación T2 preexistente, resultando en un aumento de complejidad de la enfermedad y confiriendo resistencia a tratamiento con T2 como diana. En algunos estudios, por este motivo, se propone IL6 como biomarcador de un endotipo de asma no-T2.
De forma paralela se ha observado un desequilibrio Th17/Treg en la urticaria crónica espontanea mal controlada, por lo que parece ser un marcador relevante de la gravedad UCE, (asociándose a más prurito, peor calidad de vida y mayor actividad de la enfermedad), encontrando que el ejercicio a corto plazo mejora los síntomas, mientras los programas de ejercicio regular a largo plazo reducen los síntomas y mejoran las puntuaciones UCT y la calidad de vida.
Estos paralelismos también los encontramos en otras enfermedades atópicas como la dermatitis atópica (DA): En células mesenquimales de la piel de pacientes con dermatitis atópica se ha observado un perfil inflamatorio alterado en comparación con pacientes sanos, con sobreexposición de IL6 de forma significativa, y en modelos murinos con eccema tipo DA el ejercicio aeróbico de intensidad moderada atenúa los síntomas de DA modulando los mediadores inflamatorios. Estos resultados sugieren que el ejercicio puede ser una terapia complementaria eficaz y práctica en DA al reducir los mediadores inflamatorios.
CONCLUSIONES
- El músculo esquelético debe ser considerado un órgano endocrino.
- Se comunica con el resto de órganos y células mediante la secreción de mioquinas
- La IL-6 es una de las mioquinas más descritas. La función que ejerce depende el contexto
- El ejercicio actúa como un modulador inmunológico al influir en la IL-6 y por tanto linfocitos T y B
- El ejercicio regular puede ayudar a mitigar la disregulación inmunitaria característica de las enfermedades alérgicas y autoinmunes al modular el eje Treg/TH17 y reducir la inflamación crónica basal.
- La prescripción de ejercicio debe verse como una intervención terapéutica complementaria en el manejo de enfermedades alérgicas e inflamatorias.
- No todo el ejercicio es igual: Para lograr el efecto antiinflamatorio sistémico y la modulación inmune óptima, la duración, intensidad y tipo de actividad física son consideraciones clave para futuras investigaciones y recomendaciones clínicas.
BIBLIOGRAFÍA
- Severinsen, M. C., & Pedersen, B. K. (2020). Muscle–Organ Crosstalk: The Emerging Roles of Myokines. Endocrine Reviews, 41(4), 594–609.
- Nash D, Hughes MG, Butcher L, Aicheler R, Smith P, Cullen T, Webb R. IL-6 signaling in acute exercise and chronic training: Potential consequences for health and athletic performance. Scand J Med Sci Sports. 2023 Jan;33(1):4-19.
- Rose-John S, Jenkins BJ, Garbers C, Moll JM, Scheller J. Targeting IL-6 trans-signalling: past, present and future prospects. Nat Rev Immunol. 2023 Oct;23(10):666-681. doi: 10.1038/s41577-023-00856-y
- Tanaka T, Narazaki M, Kishimoto T. IL-6 in inflammation, immunity, and disease. Cold Spring Harb Perspect Biol. 2014 Sep 4;6(10):a016295. doi: 10.1101/cshperspect.a016295. PMID: 25190079
- Luan, D., Dadpey, B., Zaid, J., Bridge-Comer, P., DeLuca, J., Xia, W., … & Reilly, S. (2022). Adipocyte-secreted il-6 sensitizes macrophages to il-4 signaling.. https://doi.org/10.1101/2022.07.19.500620
- Namakanova, O. A., Горшкова, Е. А., Зварцев, Р. В., Nedospasov, S. A., Drutskaya, M. S., & Gubernatorova, E. O. (2022). Therapeutic potential of combining il-6 and tnf blockade in a mouse model of allergic asthma. International Journal of Molecular Sciences, 23(7), 3521.
- Rose-John S, Jenkins BJ, Garbers C, Moll JM, Scheller J. Targeting IL-6 trans-signalling: past, present and future prospects. Nat Rev Immunol. 2023 Oct;23(10):666-681. doi: 10.1038/s41577-023-00856-y
- Gupta, D., Orehek, S., Turunen, J. J., O’Donovan, L., Gait, M. J., Andaloussi, S. E., … & Wood, M. J. A. (2023). Modulation of pro-inflammatory il-6 trans-signaling axis by splice switching oligonucleotides as a therapeutic modality in inflammation. Cells, 12(18), 2285.
- Chen W, Jin W, Hardegen N, Lei KJ, Li L, Marinos N, McGrady G, Wahl SM. Conversion of peripheral CD4+CD25- naive T cells to CD4+CD25+ regulatory T cells by TGF-beta induction of transcription factor Foxp3. J Exp Med. 2003 Dec 15;198(12):1875-86
- Lee J, Lozano-Ruiz B, Yang FM, Fan DD, Shen L and Gonzá lezNavajas JM (2021) The Multifaceted Role of Th1, Th9, and Th17 Cells in Immune Checkpoint Inhibition Therapy. Front. Immunol. 12:625667
- Ryba‐Stanisławowska, M., Skrzypkowska, M., Myśliwska, J., & Myśliwiec, M. (2013). The serum il-6 profile and treg/th17 peripheral cell populations in patients with type 1 diabetes. Mediators of Inflammation, 2013, 1-7.
- Kong et al. «Antigen‐specific transforming growth factor β–induced Treg cells, but not natural Treg cells, ameliorate autoimmune arthritis in mice by shifting the Th17/Treg cell balance from Th17 predominance to Treg cell predominance» Arthritis & rheumatism
- Huss et al. «TGF-β Enhances Effector Th1 Cell Activation but Promotes Self-Regulation via IL-10“ The Journal of Immunology, vol. 184, no. 8, 2010.
- Palomares, O., et al. (2010). T regulatory cells and allergic disease. European Journal of Immunology, 40(5), 1266–1271.
- Lindsley AW, Lugogo N, Reeh KAG, Spahn J, Parnes JR. Asthma Biologics Across the T2 Spectrum of Inflammation in Severe Asthma: Biomarkers and Mechanism of Action. J Asthma Allergy. 2025 Jan 14;18:33-57. doi: 10.2147/JAA.S496630. PMID: 39830595; PMCID: PMC11742565.
- Son WK, Yoon W, Kim S, Byeon JH, Lee JS, Kim D, Jaehoon L, Chae Y, Yoon SJ, Yoo Y. Can moderate-intensity aerobic exercise ameliorate atopic dermatitis? Exp Dermatol. 2020 Aug;29(8):699-702. doi: 10.1111/exd.14138. Epub 2020 Jul 20. PMID: 32614478.
- Campanati A, Orciani M, Marani A, Di Vincenzo M, Magi S, Gregoriou S, Diotallevi F, Martina E, Radi G, Offidani A. Mesenchymal Stem Cells Profile in Adult Atopic Dermatitis and Effect of IL4-IL13 Inflammatory Pathway Inhibition In Vivo: Prospective Case-Control Study. J Clin Med. 2022 Aug 15;11(16):4759. doi: 10.3390/jcm11164759. PMID: 36013001; PMCID: PMC9409772.